多金属氧酸盐材料在环境催化转化中的应用
王梦舟,许嘉谦,张庆瑞,孙奇娜,∗
(1.燕山大学 河北省水体重金属深度修复与资源利用重点实验室,河北 秦皇岛 066004;2.燕山大学 环境与化学工程学院,河北 秦皇岛 066004)
0 引言
多金属氧酸盐(Polyoxometalates,POMs)是一类多核配位聚合物,又称多酸盐,迄今已有200 余年的历史[1-2]。1826 年,Berzerius 等将七钼酸铵加入到磷酸中,得到了结构不明确的黄色沉淀,这种物质就是后来为人熟知的(NH4)3PMo12O40。而POMs 真正的研究开始于1864 年,Marignac 等发现并通过仪器表征了第一个杂多钨酸盐,在接下来的70 年里,科研人员对此类多金属氧酸盐进行了系统研究,借助化学分析法获得了明确组成,并于1935 年发表了对此类化合物的具体描述。1929 年Pauling 提出了1 ∶12 系列POMs 结构的三维模式,推动POMs 化学进入快速发展的新时代。此后,相关研究由理论向应用拓展,POMs 作为催化剂为化学合成提供更温和的反应条件和更高的反应效率,迅速在此领域迎来发展高峰。同时,研究人员不断合成新型POMs,开发医学、磁学、电学等新的应用领域;并且随着学科间交叉发展,POMs 逐渐在环境领域,尤其是生物质和污染物催化转化上引起了关注。
然而,与有机合成等传统催化领域的产业化程度相比,POMs 在环境领域中的应用研究总体上还处在探索阶段。生物质及污染物的转化、降解体系中,往往组分复杂、共存物浓度高、反应物浓度低,这些特点造成了环境催化转化与化学催化合成,特别是绿色化学生产应用间的区别,进而影响了POMs 在环境领域的适用性[3]。为了解决这些问题,近年来研究者将POMs 与其他材料结合,构建POMs 复合材料,为环境体系提供多功能的、针对低浓度目标污染物具有特异性的催化剂,以此拓宽POMs 在环境领域的应用前景。在此过程中,POMs 化学作为理论基础指导着复合材料设计及其特性研究。因此,本文首先总结了POMs 的基本结构、合成方法和理化特性,在此基础上综述了POMs 材料在环境催化转化中的研究热点——生物质和污染物的催化转化,以期进一步推动POMs 材料在环境领域中的应用。
1 多金属氧酸盐的结构
早期多酸化学认为无机含氧酸通过缩合反应可以制得缩合酸,并且根据多酸是否由同种含氧酸盐缩合而得将其分为同多酸(盐)和杂多酸(盐)两类[4]。当POMs 骨架只含有附加金属M 和氧时,这些簇合物称为同多金属酸盐,例如阴离子[M6O19]2-,其中附加原子M(M=Mo,W,V,Nb,Ta等)又称为配原子。而当溶液酸化时,上述阴离子多面体围绕杂原子X 缩合,形成包括X、M 和氧的簇合物,即杂多配合物,因此X(X=P,Si,B,Ni,Zn,Cd,Mn 等)又称中心原子。
{MO6}八面体和{XO4}四面体是POMs 的基本构筑单元,通过共角、共边或共面相连成金属氧簇,形成具有各种不同尺寸和形状的坚固结构,包括封闭的笼、球壳以及篮、碗、桶形和带状等,其类型可归纳为Keggin 型、Dawson 型、Silverton 型、Lindqvist型、Anderson 型、Waugh 型6 种,如图1 所示。饱和的POMs 结构可失去阴离子骨架上的八面体从而得到相应的缺位结构。配原子元素种类也由传统的Mo、W、V、Nb、Ta 等第Ⅴ、Ⅵ主族元素进一步扩展;目前已知的杂原子元素种类有70 多种,包括第一系列过渡金属,第二、三系列过渡金属元素的绝大部分,以及Si、S、As、Na、Ti、Cr、Hf、Ln 等[5-7]。

图1 多金属氧酸盐常见的6 种结构Fig.1 Six common structures of polyoxometalates
1.1 Keggin 结构
Keggin 结构通式可表示为[XM12O40]n-,X=B、Si、P、As 和 Ge 等,M=W、Mo 和 V 等,例如H3PW12O40[8]。它是由1 个中心四面体和4 组三金属簇(3 个杂原子八面体{MO6}共边)构成,具有Td 对称性。Keggin 结构作为最早被发现且较为常见的结构类型,对多金属氧酸盐结构的研究具有重大意义。它具有5 种异构体:α、β、γ、δ、ε型,其中最为常见也是最稳定的为α 型,由中心四面体和与其4 个顶点共顶点的4 组三金属簇相连构成,整个阴离子呈Td 对称性[9],如图2 所示。作为典型的POMs 结构,Keggin 结构不但具有温和条件下的可逆多电子氧化还原性,还可以通过外部修饰剂和堆积模式调整其氧化还原行为,这使它们广泛应用于各催化领域[10-12]。此外,Keggin类型的POMs 表现出良好的光学性能和光敏活性,可媲美二氧化钛(TiO2)半导体光催化剂。因此,可以应用Keggin 结构的POMs 为构筑单元,制备具有光/电催化活性的POMs 基超分子材料和负载型POMs 催化剂[13],并已广泛用于催化酯化、Friedel-Crafts 烷基化和酰基化、选择氧化、不对称催化、异构化、缩合、裂解、水合、脱水、水解、重排、Diels-Alder 及醚化等有机合成反应[14-15]。

图2 α-Keggin 结构图Fig.2 The α-Keggin structure
1.2 Dawson 结构
饱和的 Dawson 结构通式表示为[X2M18O62]n-,X=P、Si、As、Ge 等,M=Mo、W 等,例如 H6[P2W18O62][16]。它是由18 个{MO6}八面体通过共角或共边相连,并围绕2 个{XO4}四面体而形成,具有D3h 对称性。Dawson 结构由Keggin 结构衍生,可视为由2 个Keggin 结构失去1个共边三金属簇生成{XM9}单元而形成,X 在以上两种结构中都被称为内部元素,并且拥有中心杂原子。1970 年,Baker 和Figgis 预测了Dawson结构6 种可能的异构体,命名为α,β,γ,α∗,β∗和γ∗。2011 年Zhang 等[17]通过密度泛函理论计算推测出Dowson 结构6 种异构体(图3)。饱和的Dawson 结构{P2W18}内部存在巨大的张力,并将这6 种异构体分为交错带(α∗、β∗和γ∗)和蚀变带(α、β 和γ)组,进一步预测前者总是比后者更不稳定(α∗<β∗<γ∗<γ<β<α)。目前,通过核磁共振检测得到验证的结构只有α 和β 两种异构体[18],即K6[α,β-P2W18O62]·xH2O。
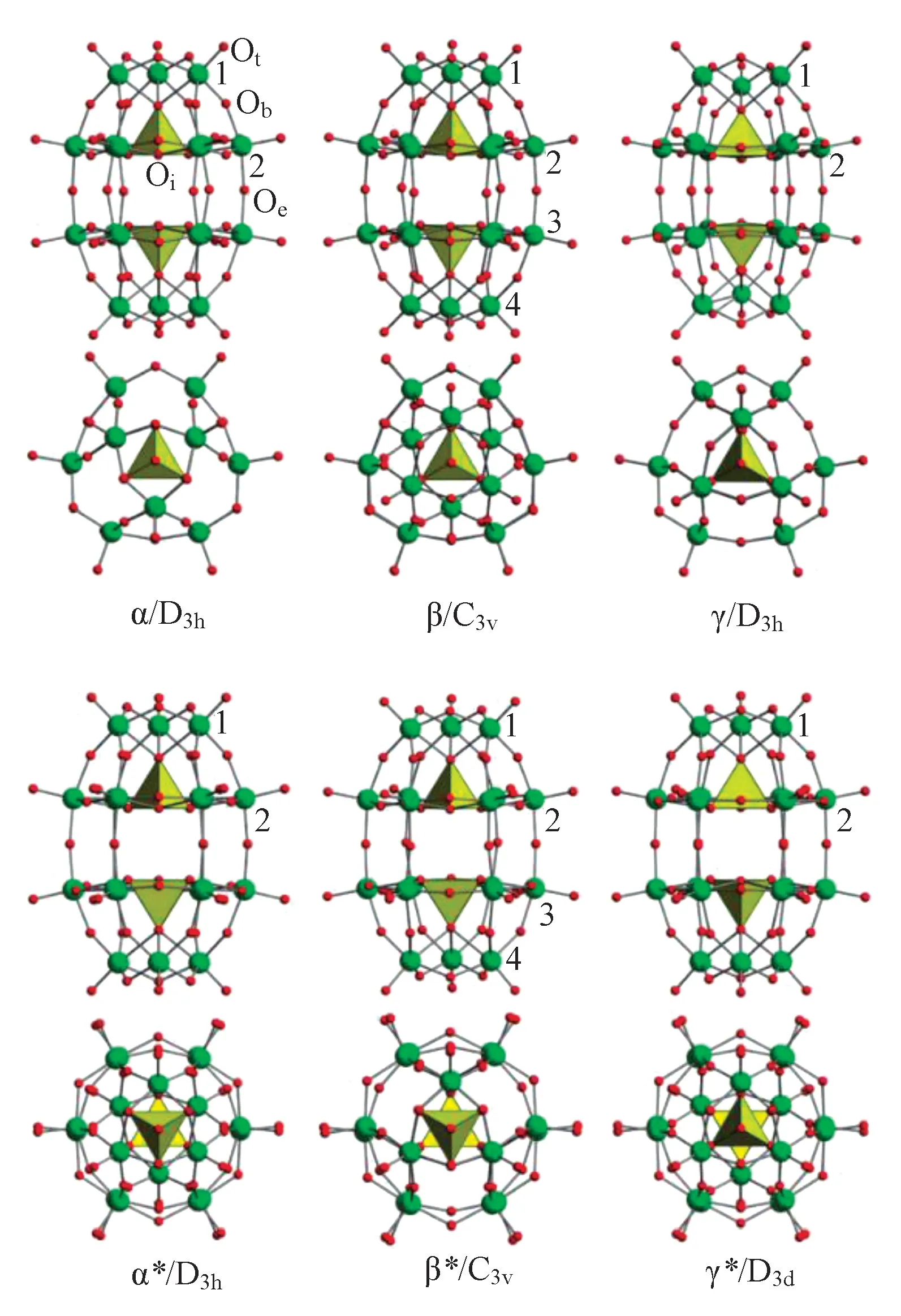
图3 Well-Dowson 结构6 种同分异构体Fig.3 Six isomers of Well-Dowson structure
1.3 Silverton 结构
Silverton 结构通式为[XM12O42]n-,X=Ce、Np、Th、U 和 Gd 等,M=Mo 和 W 等,例如Mn7(MnW12O42(OH)4)·8H2O。在Silverton 结构中,6 组共面双八面体共顶点连接,围绕相同中心形成金属簇,具有Oh 对称性。Dexter 和Silverton等[19]首次合成了Silverton 型POMs——杂多钼酸盐(NH4)H6(CeMo12O42) ·12H2O,属于立方晶体,与常见的Keggin 结构不同,它是由罕见但高度有序的6 对共面{MO6}二聚体排列形成了{XO12}的12 个配位体[20],例如十二胺钼杂多酸是由6 个共面的{Mo2O9}二聚体,通过共用面氧原子与中心杂原子{CeO12}共角连接形成的二十面体[21]。另外,与其他几种结构相比,Silverton 型POMs 中心X—O 键长在0.24~0.28 nm,大于Na、Ru 等碱金属与氧形成的键长,为将碱金属引入POMs 作为中心杂原子提供了可能,如图4[22]。
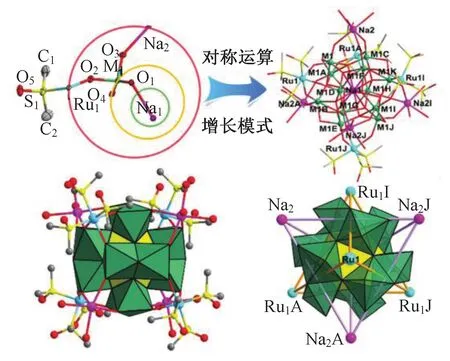
图4 引入碱金属Silverton 结构多金属氧酸盐阴离子示意图Fig.4 Schematic diagram of the introduction of alkali metal Silverton structure polyoxometalate anions
1.4 Lindqvist 结构
Lindqvist 结构通式可表示为[M6O19]n-,M=W、Mo、Ta 等,例如[Cu2(phnz)3] (Mo6O19)[23-24](phnz=phenazine)。从其组成可知,此结构为相同阴离子构成的多酸,由6 个八面体相连构成,具有Oh 对称性,见图5[25]。与Keggin 结构相比,Lindqvist 结构通常具有更小的摩尔质量。Lindqvist 结构呈二维非交织骨架,具有标准的蜂窝状空腔,由Lindqvist 型POM 阴离子占据,如[Cu2(phnz)3] (Mo6O19) 由 [Mo6O19]2-和[Cu2(phnz)3]2+塔式阴离子组成,其中阴离子簇内存在3 种氧原子,即末端氧Oa,双桥氧Ob和中心氧Oc。另外,Lindqvist 型POMs 的有机金属衍生物可以通过用有机金属M′L(其中M′为六价或低价金属,L 为配体,如RO-,O2-等)取代MOa制得[26],这使得POMs 在有机金属化学方向迅速发展。

图5 Lindqvist 阴离子化合物结构示意图Fig.5 Schematic diagram of the structure of Lindqvist anion compounds
此外,在Lindqvist-POMs 中,当Mo 或W 原子被低价金属原子V、Nb 和Ta 取代时,电子密度增加,可获得额外的稳定性[27-28],在这些多金属有机化合物中,含钒多金属有机化合物研究最为广泛[29]。
1.5 Anderson 结构
Anderson 型POMs 是盘状的一维结构多酸(如图6),结构通式表示为[XM6O24]n-,X=Cu、Mo、Co、Al 和 I 等,M=Mo 和 W 等,例如[IMo6O24]5-。与典型的Keggin 结构和Dawson 结构相比,对Anderson 型POMs 的研究还未十分深入。它由6 个八面体共边围绕中心八面体构成,具有D3d 对称性[30]。Anderson 型POMs 阴离子具有平面结构,每个配原子都有两个高活性末端氧,因此,这种多齿配体可以连接过渡金属或稀土金属配合物,有助于有机-无机杂化化合物的构建。这一高度灵活的多金属氧簇允许不同角度的修饰(图6(a)): 1)可以结合大量不同大小和氧化状态的不同杂原; 2)可以结合无机和有机阳离子以及具有不同配位基序的分子;3)与三(羟甲基)甲烷配体的共价连接使其能够与特定的有机基团结合[31]。例如,当中心八面体的氧原子被三配体取代时,可成为构建多功能杂化POMs 化合物的高效平台,由一维扩展到二维和三维(图6)[32]。
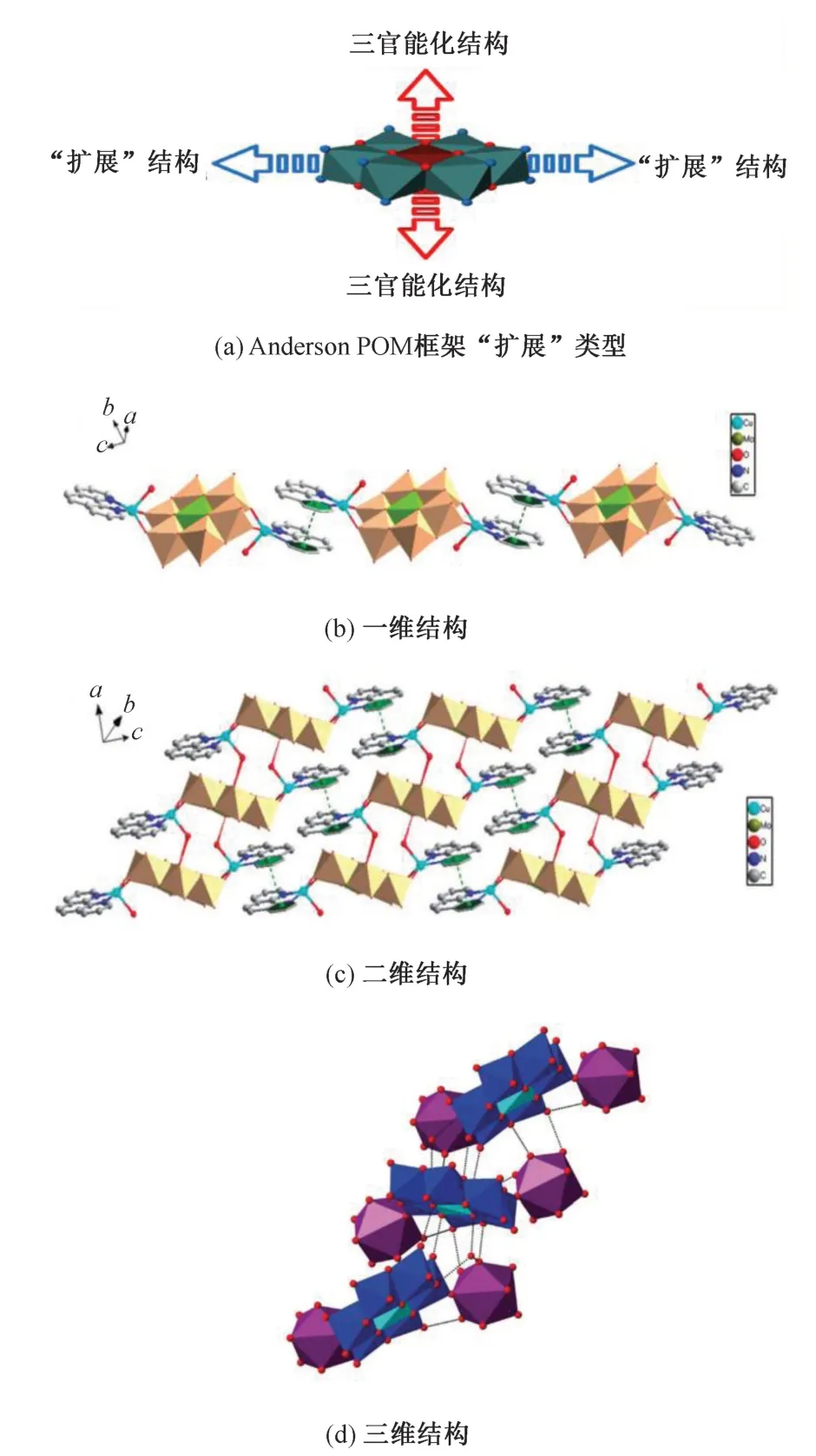
图6 Lindqvist 阴离子化合物的结构示意图Fig.6 Schematic diagram of the structure of Lindqvist anion compounds
1.6 W augh 结构
Waugh 结构POMs 最早由Hall 在1907 年以其钾盐和钡盐的形式制得[33],1954 年Waugh 确定了其具体结构并首次合成了(NH4)6[XMo9O32](X=Ni、Mn),如图7(a)。Waugh 结构通式为[XM9O32]n-,X=Mn 和Ni 等,M 一般为Mo,例如[CoMo9O32]6-。Waugh 型多金属氧酸盐由9 个八面体围绕1 个中心杂原子八面体构成,同时两组共边的三金属簇位于4 个八面体中间层的上方和下方,使多金属氧酸盐阴离子具有理想的D3 点对称性,并且具有旋光性质。Waugh 型化合物可由结构灵活的Anderson 型多酸阴离子通过中心杂原子修饰衍生而来:1)将Anderson 平面六方α-异构体化为蝶状β-异构体;2)引入四面体构筑单元用以封在蝶形拓扑结构之上,起稳定作用,并最终合成Waugh 型杂多阴离子(图7(b))[34]。Waugh 型多阴离子的杂原子处于高氧化态,可以利用强氧化剂(如过氧二硫酸盐、溴酸盐、次氯酸以及过氧化氢等) 氧化低价的杂原子锰和镍来制备。[CoMo9O32]6-和[NiMo9O32]6-等Waugh 型POMs合成成本高、产率低且稳定性差,因此目前对Waugh 结构研究较少。
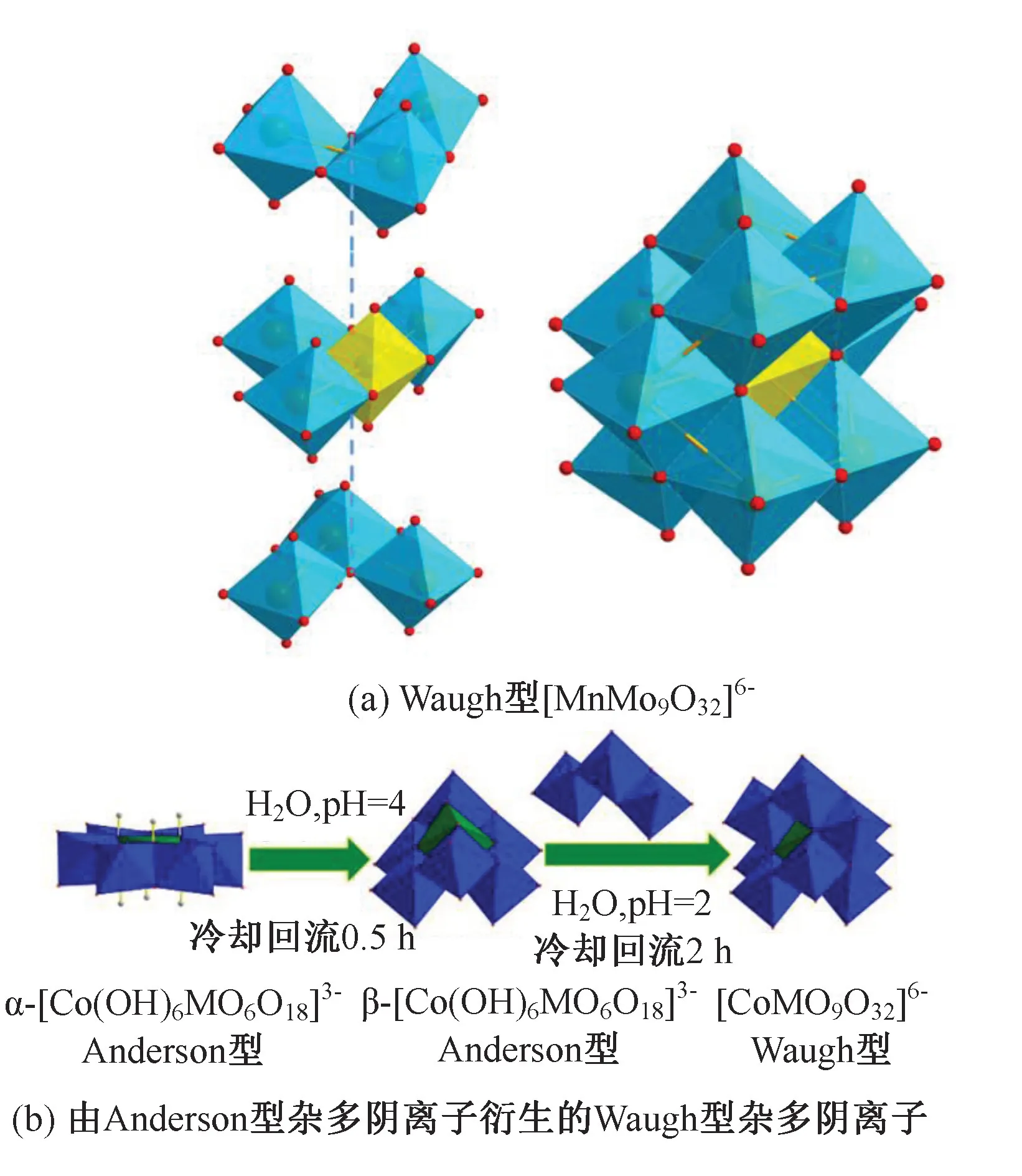
图7 Waugh 阴离子化合物的结构示意图Fig.7 Schematic diagram of the structure of Waugh anion compounds
2 多金属氧酸盐的合成
POMs 结构类型各有不同,其合成方法也多种多样。目前,成熟常用的方法有常规合成法、水热合成法和离子液体法,其他方法在研究中也有涉及,如固相反应法、乙醚萃取法、微波法、光化学法、控制电位法、电流电解法、光还原法等。
2.1 常规合成法
在常规合成法中,用无机酸将含有前体的溶液酸化后,严格按照反应物比例及顺序引入所需杂原子,并调节pH 值范围后,在室温条件下即可得到目标产物,一个典型的例子如图8 所示。常规合成法是一种均相合成方法,根据溶剂类型不同又可分为水溶液法与有机溶液法。常规法反应条件易满足,产率高、重复性好,产物晶体大小及形态易受合成条件影响敏感,如pH 值、温度、搅拌速度等,较适于合成溶解度大或者结构复杂的POMs 多核多酸聚合物[35]。
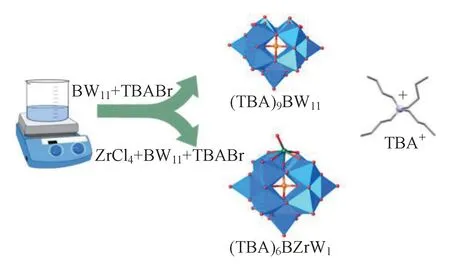
图8 常规法合成多金属氧酸盐示意图Fig.8 Schematic diagram of conventional synthesis of polyoxometalates
2.2 水热合成法
水热法合成POMs 属于非均相化学反应,在水溶剂或矿化剂存在下,利用水热反应釜加热前驱体与溶剂,通过溶解重结晶得到POMs。水热法合成的POMs 结晶度高,生长取向好,晶体粒度可控,特别有利于合成纳米尺度材料。此外,水热合成中通常采用的“一锅法”能够直接合成一维至三维结构化合物,避免了中间体的分离,简化了操作步骤,最大限度地减少了化学废物的产生,很大程度上丰富了多酸化学[36]。Sun 等[37]利用“一锅法”合成POMs 复合材料(图9),通过循环实验得出结论:“一锅法”对氧化缩合反应具有高催化活性,且催化活性能在多次循环中不损失。然而由于反应条件对温度、压力要求较高,因此产率低重复性差,以及存在安全隐患等问题也有待进一步解决。

图9 水热合成法示意图Fig.9 Schematic diagram of the hydrothermal synthesis method
2.3 离子液体法
离子液体法与水热法同属于非均相反应制备方法,但其过程是以离子液体为介质、借助离子交换实现POMs 制备的一种非均相反应,适用于合成原料在水中溶解度较低的多金属氧酸盐。离子液体完全由离子组成,与水或有机溶剂相比,离子液体不易挥发,热稳定性好,结构多样,配位能力弱,可为晶体的自组装反应提供良好的溶剂环境,被称为“绿色反应介质”[38]。在离子液体中,无机前驱体可以获得更大的溶解度,从而极大地提高反应活性,另外,离子液体中的微量水合卤素离子可以促进POMs 生长及结晶。更为有利的是离子液体的酸性可调节,能够满足不同种类POMs 合成所需的pH 值条件[39]。Lin 等[40]采用常温下的离子液体法合成了新型α-Keggin 结构POMs—[EMIM]4[SiMo12O40]·12H2O,在这一过程中离子液体既是溶剂又是电荷补偿物。离子液体法也可在高温条件下使用,称为离子热合成法,Fu等[41]则应用了离子热合成法,在高温条件下借助离子液体合成了3 种Dawson 结构POMs,这也是首次采用此法合成POMs 基金属有机框架。这些研究都说明了离子液体法在拓展POMs 种类上的独特作用,与水热合成法相比离子液体法的重复性更高,在合成新型POMs 复合材料中极具应用前景。
3 多金属氧酸盐的性质
作为金属氧化物簇合物,POMs 丰富的拓扑结构使其具有多种物理化学特性。
3.1 酸性
POMs 是一种固体酸,根据Hammett 酸性函数计算结果可知,它比一般无机酸的酸性更强[42],可以用作酯化、水解以及Friedel-Crafts 烷基化等反应的高效酸性催化剂[43],Keggin 型POMs 在催化餐饮废油脂的酯交换反应中作为酸性催化剂高效催化棕榈酸的酯化反应,转化率高达97%并且易于分离重复利用[44]。POMs 的结构多样性使其具有可调控的Brønsted 酸性和Lewis 酸性,相应的阴离子具有弱的Brønsted 碱性,比硝酸盐和硫酸盐阴离子要软,这使POMs 材料腐蚀性小,便于应用。POMs 酸性的主要来源包括:1)直接由质子提供;2)制备过程中阴离子水解;3)金属离子配位水分子酸式解离。当中心杂原子相同时,可通过其价态高低来判断POMs 酸性强弱,通常杂原子价态越高酸性越强,例如,一些POMs 在丙酮中的酸性强弱顺序为PW12> PW11V>PMo12≈SiW12>PMo11V≈SiMo12[45]。
3.2 氧化性
通常,POMs 中的配原子以最高氧化态形式存在,因而具有较强的氧化性,可以被多电子还原而不影响其结构,并且这种还原状态是可逆的。影响POMs 氧化性的因素主要有杂原子、配原子和结构类型:1)中心杂原子种类及数量不同时,POMs 阴离子所带的负电荷数量不同,且与氧化性成反比,通常P>As>Si;2)配原子自身氧化性差异,通常V>Mo>W;3)不同结构POMs 氧化性不同,其中Keggin 型和Anderson 型结构在催化氧化领域应用最为广泛。Povarnitsyna 等[46]以Keggin型POMs 实现了对ferulic 酸的高效催化氧化,具体原理见图10,证明了与传统催化剂相比,POMs具有更强的催化活性及选择性。Rajendran 等[47]研究表明POMs 催化剂能够通过产生金属过氧化物来活化过氧化氢从而催化氧化燃油中苯并噻吩、二苯并噻吩等含硫化合物转化为相应的砜类以达到高效脱硫的目的。
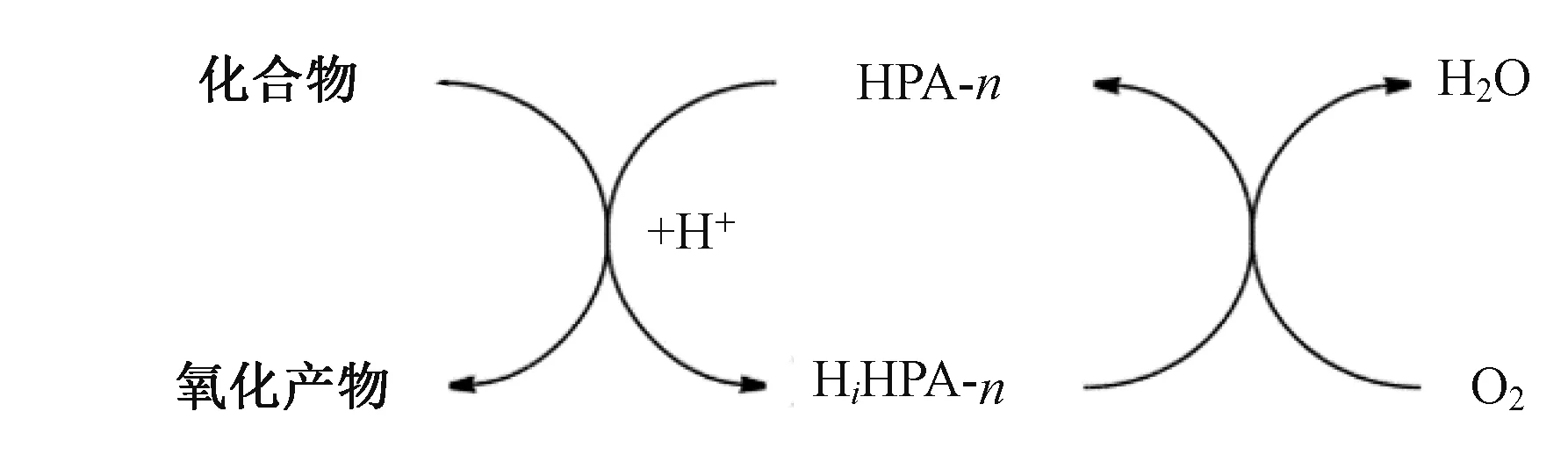
图10 多金属氧酸盐催化氧化示意图Fig.10 Schematic diagram of catalytic oxidation of polyoxometalates
3.3 热稳定性
POMs 的热稳定性与{MO6}八面体的配原子与氧原子之间的键强有关,以Keggin 结构为例,M-Oc-M 振动频率越高,POMs 热稳定性越好。另外,POMs 热稳定性还与其是否处于水合状态有关。POMs 水合状态下存在三种形式的水分子,即结合水、结晶水和结构水,反映在失水过程包含三个拐点,分别对应以下三个反应:
可以看出,POMs 酸性越弱,质子离域性越小,键强越弱与水分子结合能力越弱,相应的失水温度也越低,即热稳定性越差,而通常情况下无结晶水的POMs 通常可在400 ℃以下保持稳定[48]。值得注意的是,由于静电作用在POMs 键合中起主要作用,因此得出POMs 热分解温度的经验公式:
其中,T为热分解温度,f(X)为杂原子作用函数,f(M)为配原子作用函数,K为常数,其数值与电负性、主量子数、原子半径等相关[49]。
良好的热稳定性使得POMs 与传统催化剂相比能够适应更广的温度范围,在25 ℃~140 ℃都能够稳定高效催化有机污染物降解,不易因分解变性导致失活[50-51]。
3.4 溶解性
大多数POMs 在极性和非极性有机溶剂中的溶解度较高,这主要是由于POMs 能够通过静电力、氢键以及共价和非共价键与溶剂相互作用,这些特殊的键合方式促进了研究人员采用Langmuir-Blogdet、单层膜自组装技术以及逐层设计等方法制备POMs 复合材料。
另外,POMs 属于纳米团簇,其结构类似于一定尺寸和形状的金属氧化物的组合体,除了结构组分可调外,还具备优良的接枝特性,接枝单分子尺寸可由零点几到几十纳米[52-53],进而构建POMs基无机/有机复合材料,进一步将POMs 独特的物理化学性质拓展至更宽广的应用场景,如环境领域等。
POMs 所具有的出色的物理化学性质使其在医学、磁学、电学等领域已经得到了广泛应用,Chermann 等[54]研究生物活性多金属有机化合物,发现硅钨酸对小鼠白血病和肉瘤病毒的抑制作用,推进了对多金属氧酸盐化合物的抗病毒作用的系统研究,进一步研究发现它可模拟胰岛素、抗癌以及具有抗生素活性。另外POMs 也具有一系列有利的化学结构和电子特征使得它们能够适用于磁学以及电学的相关问题:1)稳定性较好,在固体核溶液中都能够保持结构完整;2)能够在特定的位置容纳磁性离子或磁性离子群从而产生具有特定拓扑结构和高度对称环境的磁性分子和大的磁性团簇;3)可以接受不同数量的电子,同时保持其结构完整,形成混合价系统[55]。近年来随着各学科交叉发展,多酸化学也渐渐被应用于解决环境问题。
4 多金属氧酸盐在环境催化转化中的应用
基于POMs 在化学合成,特别是催化氧化中表现出的反应条件温和、高效、“绿色”等优势,POMs 材料开始被用于解决环境问题。近年来,POMs 在环境领域的研究热点主要集中在“碳中和、碳达峰”和污染物降解转化两大方面,并逐渐成为本领域的研究热点之一(表1)。

表1 多金属氧酸盐及其复合材料在环境领域的应用Tab.1 Polyoxometalates and their composites for environmental applications
4.1 POM s 与“碳中和、碳达峰”
进入21 世纪以来,石油、天然气等化石能源的过度开采利用导致二氧化碳排放量超出环境负荷能力,随之而来的温室效应等问题日益严重,促进了清洁能源开发利用力度的加大。在各种清洁能源中,生物质被认为是碳中性的,因为它在使用过程中释放的CO2来源于自然界,已经是碳循环的一部分。并且,与传统化石燃料相比,生物质碳循环速度更快,是一种良性可再生清洁能源,被越来越多地用于化工原料及燃料生产。因此,利用包括生物质转化生产清洁能源和生物制品,可有效促进“碳中和、碳达峰”,符合我国的可持续发展战略[61]。
在各种生物质资源中,木质素及纤维素广泛存在于秸秆、枝叶、木材等农、林、牧业废物及城市园林、餐厨垃圾中,是自然界中含量最丰富的芳香类化合物。在传统工业中,仅造纸业每年就产生数百万吨工业级木质素,是目前最受研究关注的生物质[62]。但是,直接燃烧法、发酵/厌氧消化法、热化学转化法这三种传统的生物质转化技术均存在不同程度的利用率低、能耗高、产品附加值低等弊端。常规解决思路是通过高温处理、无机酸水解、生物酶降解等方式将多聚糖转化为单糖或醇类等附加值高的化学品及平台化合物,但依旧存在产率低、无机酸腐蚀、成本高、限制多等问题。在上述背景下,POMs 材料催化剂成为这类生物质转化利用的新途径。
4.1.1 催化转化木质素
Zhao 等[63]以POMs 作为光催化剂及电荷载体,无需另外化学处理常温下直接从木质素中产出电流。与传统的质子交换膜燃料电池相比,POMs 的引入使其可以直接使用木质素等聚合物生物质作为燃料且能够在常温下氧化,促使电子和质子从木质素转移到氧原子中,从而将生物能转化为电能。如图11,在阳极室中,木质素被POMs 氧化,电子和H+从木质素转移到POMs 如(5)式,被还原的POMs 重新被外部提供的O2氧化,释放的H+可通过质子交换膜进入阴极室,在Pt 的催化下与O2反应生成还原产物H2O 如(6)式。
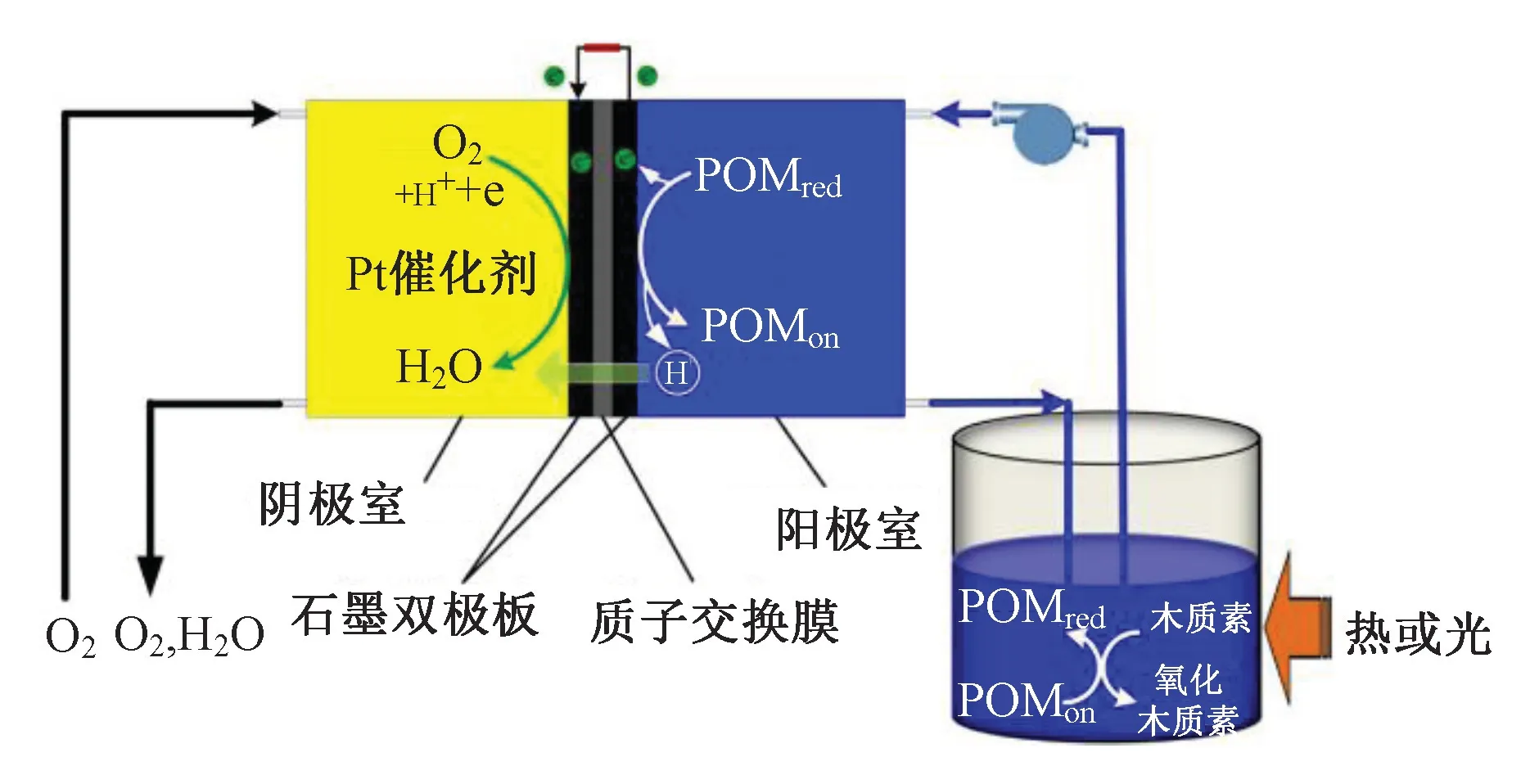
图11 POMs 催化木质素转化示意图Fig.11 Schematic diagram of lignin conversion catalyzed by polymetallic oxygenates
4.1.2 催化转化纤维素
平台化合物指可作为基本结构单元或元素、以工业规模合成化工中间体和产品的一类化合物。在温和条件下,将纤维素催化转化为葡萄糖、5-羟甲基呋喃、山梨醇或葡萄糖酸等平台化合物是其转化利用最理想的路线。这些平台化合物的生成都涉及纤维素的糖苷键断裂,在此过程中,酸催化解聚起着至关重要的作用。
Deng 等[64]通过实验证明POMs 能够高效催化降解纤维素或纤维二糖转化为葡萄糖、羟甲基纤维素钠、烷基葡萄糖苷、山梨醇、甲酸和葡萄糖酸等多种平台化合物。POMs 能够与酸化或氧化催化剂结合形成双功能催化剂,催化纤维素或纤维二糖。在这一过程中POMs 的强Brønsted 酸性起着关键作用,使其能够更有效地裂解纤维素中的β-1,4-糖苷键。与盐酸溶液、氢氧化钠等常规催化剂相比,POMs 及其双功能催化剂拥有更高的降解速率,且能够重复利用。
4.2 POM s 与污染物降解转化
4.2.1 工业染料降解
染料废水处理是工业水污染控制的主要任务之一。许多工业生产过程都涉及合成染料应用,如光电化学电池制造、纺织、皮革、造纸、食品工业等。常用的工业染料包括偶氮类、蒽醌类、吲哚类、三苯甲基(三苯基)和酞菁类,其中以偶氮类染料应用最为广泛。工业染料废水具有染料浓度低、结构稳定、生物降解难等特点,难以通过常规一、二级污水处理工艺完全降解。而采用高级氧化技术原位生成高活性羟基自由基·OH 作为氧化剂,可有效降解有机染料。Fe(II)和H2O2构成的芬顿试剂是典型的高级氧化体系,但是其成本高,降解效率受pH 值等条件影响极大。POMs 复合材料可以很好地解决上述问题。POMs 具有类似二氧化钛等半导体的光催化特性,在紫外及可见光作用下,进入激发态成为一种强氧化剂,氧化能力大于标准氢电极的激发状态,能够直接或通过·OH 自由基介导的氧化作用降解矿化有机污染物[65]。在这一体系中,偶氮类等难降解的工业有机染料断链降解,最终矿化为二氧化碳和水等无害物质,反应过程稳定,处理效果好,无二次污染[66]。
Li 等[67]制备了POM/TiO2复合材料,由于PW11O397-催化电子由TiO2的导带向分子氧转移,这一过程能够很好地抑制高活性空穴与电子结合,这使得催化性能在协同作用下进一步提高。
Ghali 等[68]采用光聚合技术将POMs 引入到光敏树脂中,制备了SiMo12O40(IPh2)4复合材料用以去除曙红染料,可知光敏树脂在光聚合后仍然保持POMs 的光催化性能,POMs 使得杂化材料在近紫外光照射下对乙腈和水溶液中的曙红-Y 具有高效的光催化活性。与传统光催化材料二氧化钛粉体相比,SiMo12O40(IPh2)4具有易回收利用的优势,电子顺磁共振波谱表明SiMo12O40(IPh2)4复合材料可通过空气接触再生,为强化光催化去除工业废水中的有机污染物提供了新的可能性。
Yi 等[69]合成了4 种新型LnCu-POMs 复合材料,用以净化水中的亚甲基蓝,实验表明,复合材料不仅能够有选择性地高效快速地去除阳离子染料亚甲基蓝,而且可重复利用率高,这也证明了多金属氧酸盐复合材料作为一种有效、经济的分离材料的巨大潜力,构建的新型材料拥有大量表面电荷,提高了对废水中染料的选择性处理能力。
4.2.2 燃料深度脱硫
煤和石油等化石燃料中的含硫化合物在燃烧过程中会转换为SO2等酸性污染物,可导致全球气候变暖、光化学烟雾、酸雨、腐蚀和水体富营养化等问题;此外,这些含硫化合物还会影响燃油中其他残留物的催化去除效果[70]。因此,化石燃料脱硫对于环境保护和燃料高效利用都是十分必要的。
化石燃料中的硫大多以硫醇、二硫化物、噻吩、硫醚等有机硫化合物的形式存在,这些物质热稳定性好且无酸性,常规脱除无机硫的沉淀法难以奏效[71]。目前的对化石燃料脱硫方式大致分为两种:加氢脱硫(Hydrodesulfurization,HDS)和非加氢脱硫(Non-hydrodesulfurization,NHDS),其中HDS 被广泛应用于脱除燃料中的硫醇、硫化物和二硫化物,但对苯并噻吩及其衍生物等含有芳香族硫化物的化合物脱硫效果不佳,往往不能满足深度脱硫的要求,而NHDS 工艺如氧化脱硫,可以在室温和常压的温和条件下脱硫,特别是对于燃料HDS 中难以脱除的二苯并噻吩苯的脱除效率要高得多。研究人员用POMs 对噻吩化合物进行氧化脱硫,实验结果说明多金属氧化物是一种出色的脱硫催化剂,在氧化过程中,二苯并硫苯可以被氧化成砜,然后可以通过传统的分离操作(如溶剂萃取、吸附等)除去[72]。
Khenkin 等[73]发现H5PV2Mo10O40复合材料可以吸附如苯并噻吩类、二苯并噻吩类和4,6-二甲基二苯并噻吩类等杂芳烃化合物,从而可以在温和的条件下将低浓度难降解的芳香族硫化物从碳氢化合物中去除,反应式为

这种复合材料具有很好的重复利用率,能够通过300~350 ℃湿氧下裂解12 h 再生,并且循环5 次仍然保持吸附活性。
Fu 等[74]利用静电纺丝法制备了一种新型Lindqvist 结构POMs 基钛纳米纤维两性催化剂DTA-MoO-TiO2,DTA 代表CH3(CH2)11(CH3)3N,MoO 表示Mo6O2-19。这种复合材料在333 K 下40 min 内对DBT 模型油的脱硫率达到100%,其机理如图12 所示。与传统催化剂相比,DTAMoO-TiO2两性催化剂具有更高的H2O2利用率以及催化活性,不仅大大提高了处理效率,而且其循环催化次数达到7 次。
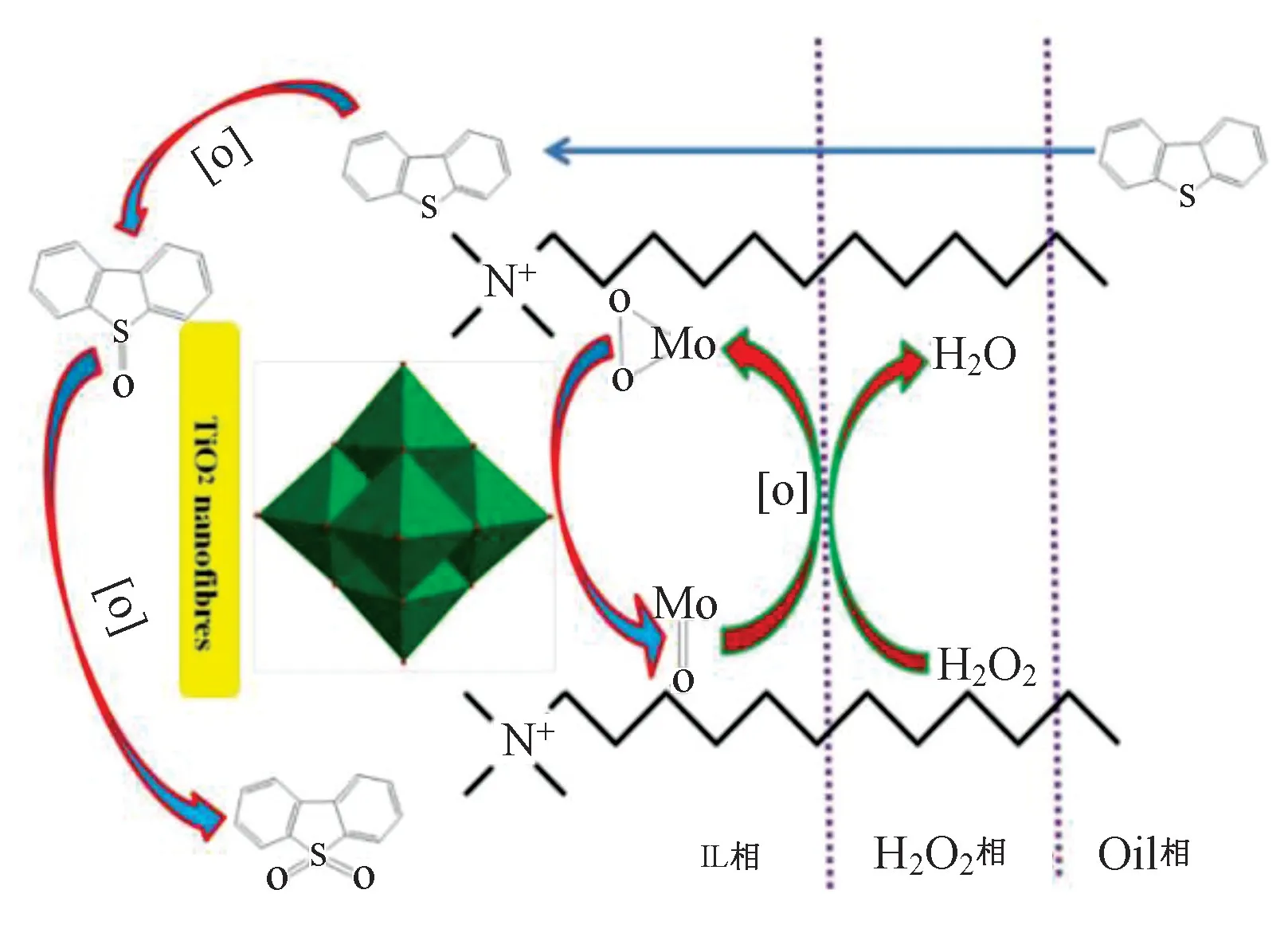
图12 DTA-MoO-TiO2 脱硫机理示意图Fig.12 Schematic diagram of the desulfurization mechanism of DTA-MoO-TiO2
4.2.3 重金属转化
重金属是一类在环境中广泛存在的污染物,Cd(I)/Cd(II)、Pb(II)以及Cr(VI)等重金属会引起人的心血管疾病、神经紊乱,癌症等疾病,动物实验已经证明Hg(II)、Pb(II)等重金属甚至可能诱发或加重自身免疫性疾病。重金属在水体中以阳离子或含氧阴离子形式存在,即使微量也会通过食物链富集,导致对生物圈及人类健康的极大威胁。
铬是工业废水中常见的重金属污染物,一般以三价和六价的形式存在,Cr(III)易水解以氢氧化物的形式沉淀而分离,但六价铬在水体中常以CrO42-、Cr2O72-、HCrO4-等阴离子形式存在,具有很高的溶解度以及较强的迁移性,属于剧毒致癌物。Fu 等[75]采用POMs 催化酸洗零价铁处理含Cr(VI)废水,这一过程中POMs 可将电子从零价铁转移至溶解氧,加速H2O2的生成,从而促进Cr(VI)还原为Cr(III)并进一步去除,见图13 及式(7)~(9):
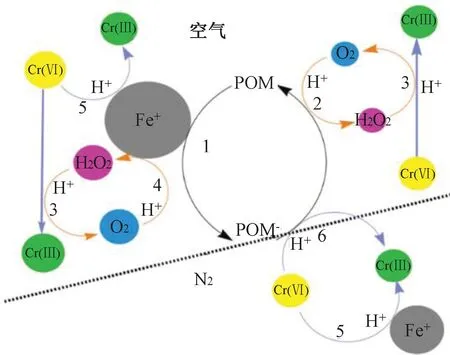
图13 多金属氧酸盐催化还原重金属示意图Fig.13 Schematic diagram of the catalytic reduction of heavy metals by polyoxometalates
Kim 等[76]研究了Keggin 型POMs 作为均相催化剂,处理Cr(VI)与阴离子染料共存的废水。POMs 被染料敏化而成为电子传递介体,催化电子由激发态染料向重金属离子转移,可同时实现Cr(VI)的转化和染料的降解。Troupis 等[77]以一系列POMs(PW12O403-,SiW12,P2Mo18O626-)为光催化剂,回收并提纯废水中的Cu。通过POMs吸收光能,催化作为牺牲性还原剂的有机底物,Cu(II)将被还原的POMs 再次氧化的这一过程,Cu(II)先被还原为Cu(I)随后又被还原为Cu,反应的最终产物为纯的零价态铜单质,不需要进一步催化分离。Song 等[78]研究了3 种POMs 的半导体光响应性质,并制得CdS-POMs(Ag3PMo3W9O40,Ag3PMo6W6O40,Ag3PMo9W3O40)复合纳米晶,测试其对As(III)的氧化能力。结果表明POMs 可延缓CdS 的电子空穴复合,促进镉的电荷分离及传导,提高CdS 对三价砷的氧化效率。
5 展望
POMs 是一种多核配位聚合物,由于结构中的{MO6}八面体和{XO4}四面体连接方式不同,可分为6 种基本类型。目前主要通过常温均相法、水热法、离子液体法等技术合成,并且可实现对POMs 分子结构以及理化性质的调控。POMs 具有Brønsted 酸性,氧化性强,热稳定性和溶解性优异,吸引了环境领域的关注。得益于其结构特点,POMs 可用于构建功能各异的复合材料,为解决生物质转化利用、污染物转化降解等问题提供了新思路。目前,POMs 在环境催化转化中的应用总体上还探索阶段,为了尽早实现工业化应用,可以在以下方面拓展研究。
1) 目前研究大多集中于Keggin 型以及Dawson 型2 种结构,相对而言其他类型POMs 的结构、特性和应用研究不足。结合多酸化学理论、离子液体等先进的合成方法和新型表征手段,对于POMs 开展结构调控以及复合材料设计的系统研究,不仅可以推动金属氧酸盐化学进一步发展,也有助于合理构建适于环境催化转化的POMs材料。
2) 在环境催化转化的特定系统中,对POMs的功能及应用特性的深入研究,延长催化剂寿命,提高对氧化剂的利用率和对目标物的转化效率,引导催化转化过程更加绿色环保。同时,系统分析POMs 催化与传统处理技术的协同作用,以此推动POMs 材料与已有工艺的联用,拓宽POMs 材料在环境领域的应用场景,促进其商品化和大规模工业应用。
总之,基于多酸化学的不断发展,借助各学科间理论与实践的充分融合,更多成功实用案例将证明POMs 材料在环境相关领域的良好应用前景。

