丹酚酸D稳定性研究
缪兴龙, 靳元鹏, 张兰兰, 周水平, 郭治昕*
(1.天津中医药大学,天津300193;2.天津天士力集团有限公司,天津300410)
丹参为唇形科鼠尾草属植物丹参Salvia miltiorrhiza Bunge的干燥根及根茎,具有祛瘀止痛、活血通经、清心除烦和滋补作用,在临床上用于心脑血管疾病、癌症、抗衰老等方面的治疗[1]。丹参中的化学成分主要为脂溶性和水溶性两类,脂溶性成分主要为丹参酮Ⅰ、丹参酮ⅡA、丹参酮ⅡB、隐丹参酮等;水溶性成分主要是酚酸类,包括丹参素、原儿茶醛、原儿茶酸、咖啡酸、丹酚酸 A、丹酚酸 B、丹酚酸D、迷迭香酸等[2]。丹酚酸类成分具有抗氧化、保护脑组织细胞损伤、保护心脑血管系统的作用[3]。但由于丹酚酸类成分不稳定,导致一些以丹酚酸水溶性成分为主的丹参制剂在生产过程中成分容易发生变化,给制剂生产过程中的质量控制带来影响。文献报道的此类物质的研究以丹酚酸B为主,丹酚酸B易受加热温度、加热时间和pH影响而发生水解反应[4];丹酚酸B在一定条件可转化为丹酚酸A,从而用于丹酚酸A的制备[5]。目前尚未见有关丹酚酸D(salvianolic acid D,SalD)的相关研究,因此本实验针对丹酚酸D的稳定性进行考察,采用高效液相色谱测定不同影响因素下的峰面积变化,为制剂生产过程中的稳定性控制提供实验依据;同时观察不同实验条件下其它一些丹酚酸类成分的生成情况,了解丹酚酸D与其它丹酚酸成分间的转化关系。
1 材料与方法
1.1 仪器 高效液相色谱仪(Agilent 1100,数据处理软件为ChemStation);电热恒温水浴锅(北京市长风仪器仪表公司);KQ-500DB型数控超声清洗器(昆山市超声仪器有限公司);HI 9025 microcomputer pH meter(Hanna Instruments Pte Ltd);TC-10K型电子天平(常熟双杰测试仪器厂);BUCHI Rotavapor R-200;BUCHI Heating Bath B-490;SHB-Ⅲ循环水式多用真空泵(郑州长城科工贸有限公司);调温电热套(北京中兴伟业仪器有限公司)。
1.2 材料、试剂 丹参药材购于陕西商洛GAP基地,经天津天士力制药股份有限公司鉴定为唇形科鼠尾草属植物丹参的干燥根及根茎;AB-8树脂(天津兴南允能高分子技术有限公司);聚酰胺(台州市路桥四甲生化塑料厂);MCI填料(日本三菱公司);色谱乙腈(Merck公司);浓盐酸、磷酸、氢氧化钠固体(分析纯);蒸馏水(Milli-Q制备);丹参浸膏(天津天士力制药股份有限公司生产车间提供)。
1.3 样品制备 丹参浸膏适量水溶解,上AB-8树脂柱,水洗脱得含丹参素、原儿茶醛、迷迭香酸、丹酚酸D的洗脱液;将上述洗脱液用浓盐酸调节至pH=3,再次上AB-8树脂柱,pH=3的酸水洗脱,除去丹参素及原儿茶醛,然后用95%乙醇溶液将迷迭香酸、丹酚酸D洗脱下来;将95%乙醇洗脱液减压浓缩后,上聚酰胺色谱柱,依次用30%、40%乙醇溶液洗脱,得到丹酚酸D溶液,减压浓缩得丹酚酸D粗品;再将丹酚酸D粗品溶解,过MCI色谱柱,依次用10%、20%乙醇溶液洗脱,得丹酚酸D溶液,减压浓缩得丹酚酸D样品。
1.4 pH值对丹酚酸D稳定性影响 丹酚酸D样品40 mg用300 mL蒸馏水溶解,量取丹酚酸D水溶液4份,每份50 mL,分别用浓盐酸溶液和氢氧化钠溶液调节pH为1、3、5、7。将4份不同pH的丹酚酸D水溶液进行加热回流10 h,定时取样检测,以峰面积比表征丹酚酸D变化情况。
1.5 不同体积分数乙醇溶液对丹酚酸D稳定性影响 丹酚酸D样品40 mg分别用300 mL的30%、60%、90%乙醇溶液溶解,各量取丹酚酸D溶液4份,每份50 mL,分别用浓盐酸溶液和氢氧化钠溶液调节pH为1、3、5、7。将4份不同 pH的丹酚酸 D不同浓度乙醇溶液进行加热回流10 h,定时取样检测,以峰面积比表征丹酚酸D变化情况。
1.6 温度对丹酚酸D稳定性影响 根据丹酚酸D在不同水-乙醇溶液中稳定性影响研究的基础上,进行丹酚酸D在不同温度下稳定性研究。丹酚酸D样品40 mg用300 mL适宜溶液溶解,量取丹酚酸D溶液4份,每份50 mL,分别用浓盐酸溶液和氢氧化钠溶液调节pH为1、3、5、7。将4份不同pH的丹酚酸D溶液置于不同温度下保存10 h,定时取样检测,以峰面积比表征丹酚酸D变化情况。
2 结果
2.1 色谱条件[6]色谱柱Agilent ZORBAX SB-C18(5 μm,4.6 mm × 250 mm);流动相 A:0.02% 磷酸水溶液,流动相B:乙腈-0.02%磷酸水溶液(80∶20),梯度洗脱(0 min,A:90%;0 ~8 min,A:90%→78%;8~15 min,A:78% →74%;15~55 min,A:74%→48%);体积流量1 mL/min;进样量10 μL;柱温30℃;检测波长280 nm。
此方法为复方丹参滴丸质量控制方法的色谱条件,可同时检测6种丹参水溶性成分:丹参素、原儿茶醛、丹酚酸D、迷迭香酸、丹酚酸B、丹酚酸A。见图1。
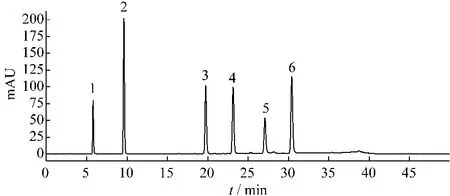
图1 6种丹酚酸成分色谱图Fig.1 The chromatogram of six salvianolic acid components
2.2 样品测定 1.3项制备的丹酚酸D样品进行HPLC检测,归一化法计算丹酚酸D峰面积大于90%,结果见图2。
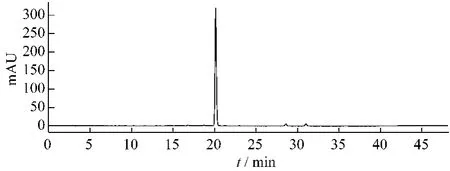
图2 丹酚酸D样品色谱图Fig.2 The chromatogram of salvianolic acid D sample
2.3 pH值对丹酚酸D稳定性影响 结果见表1和图3。
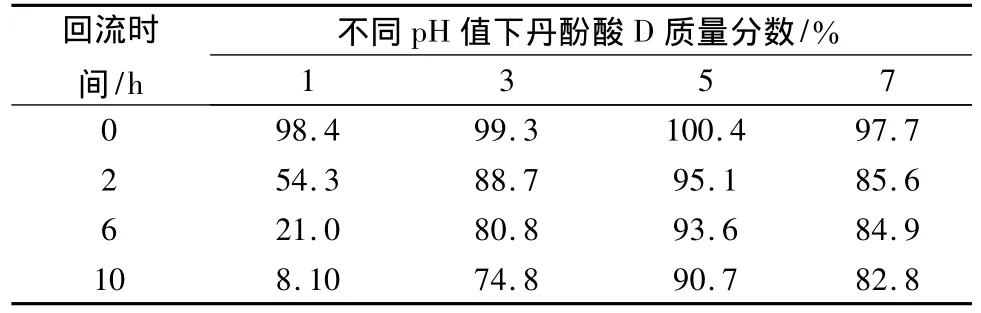
表1 调节pH及加热回流10 h后变化情况Tab.1 The content changes after pH adjustment and refluence 10 hours
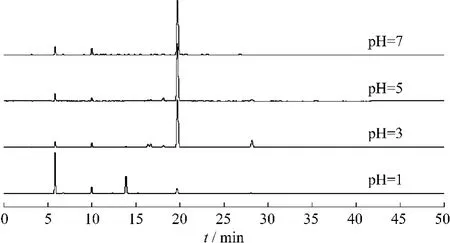
图3 加热回流10 h后成分变化情况Fig.3 The component changes after refluence 10 hours
调节丹酚酸D水溶液的 pH分别至1、3、5、7后,丹酚酸D峰面积基本保持不变。不同pH的丹酚酸D水溶液随着加热时间的增加,丹酚酸D的峰面积逐渐减少;不同pH的丹酚酸D水溶液加热回流10 h后丹酚酸D均发生转化,转化产物有丹参素和原儿茶醛(在所用检测条件下测得,以下相同),丹酚酸D减少量越多,丹参素和原儿茶醛的转化量越多。
由于丹酚酸类成分具有酚羟基,使丹酚酸类成分在碱性条件下极易成盐,导致丹酚酸类成分发生化学变化,因此本实验不对碱性条件下的丹酚酸D进行研究。通过实验研究发现不同pH的丹酚酸D水溶液加热后,丹酚酸D峰面积逐渐减少,溶液pH不同峰面积减少程度不同。pH为3~7的水溶液中丹酚酸D较pH=1的水溶液中稳定,但随着受热时间的增加,其峰面积不断减少;因丹酚酸D为弱酸性成分,故在弱酸性条件下相对稳定。丹酚酸D峰面积不断减少可能是由于高温及H+催化使丹酚酸D发生转化。丹酚酸类成分大部分为咖啡酸的聚合物[7],其中丹参素为咖啡酸的单体化合物,丹酚酸D为咖啡酸的二聚物,丹酚酸D结构中含有酚羟基、酯键及羧基,溶液在加热过程中丹酚酸D容易发生分解及被氧化,使丹酚酸D发生转化,转化为其它小分子的物质如丹参素和原儿茶醛等。随着加热时间的延长丹酚酸D量逐渐减少,丹参素和原儿茶醛的峰面积逐渐增加,与文献中报道的丹参素、原儿茶醛量随着丹参药材提取液的受热时间延长量持续增加具有一定的相似性[8-10]。化学结构见图4。
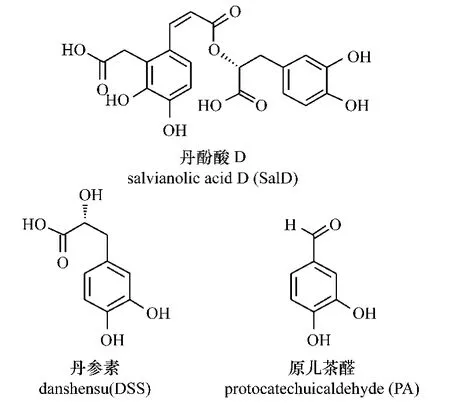
图4 丹酚酸D,丹参素,原儿茶醛化学结构Fig.4 The chemical structure of SalD,DSS,PA
2.4 不同体积分数乙醇溶液对丹酚酸D稳定性影响 结果见表2和图5、6、7。
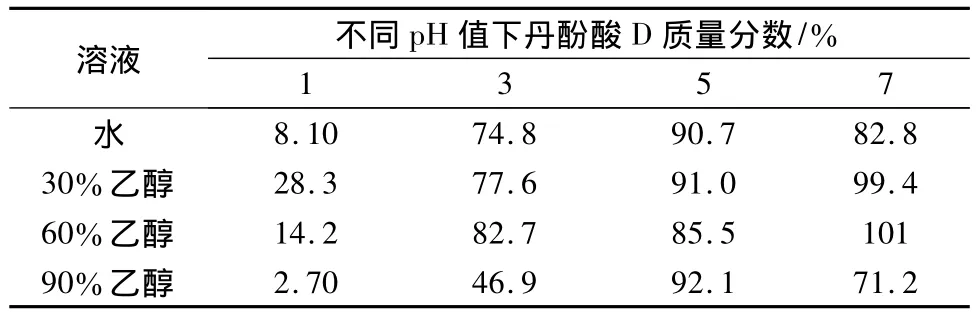
表2 不同溶液中加热回流10 h后变化情况Tab.2 The content changes in different solvents after refluence 10 hours
丹酚酸D在不同体积分数乙醇溶液中加热回流后峰面积均有不同程度减少:pH=1的4种溶液中丹酚酸D均不稳定,变化较大;pH=3,丹酚酸D在水溶液、30%乙醇溶液及60%乙醇溶液中较90%乙醇溶液中稳定,但仍有部分发生转化;pH=5的4种溶液中丹酚酸D稳定性差异不大,较为稳定;pH=7,丹酚酸D在30%、60%乙醇溶液中较其他2种溶液中稳定。

图5 30%乙醇溶液中加热回流10 h后成分变化情况Fig.5 The component changes in 30%EtOH solution after refluence 10 hours
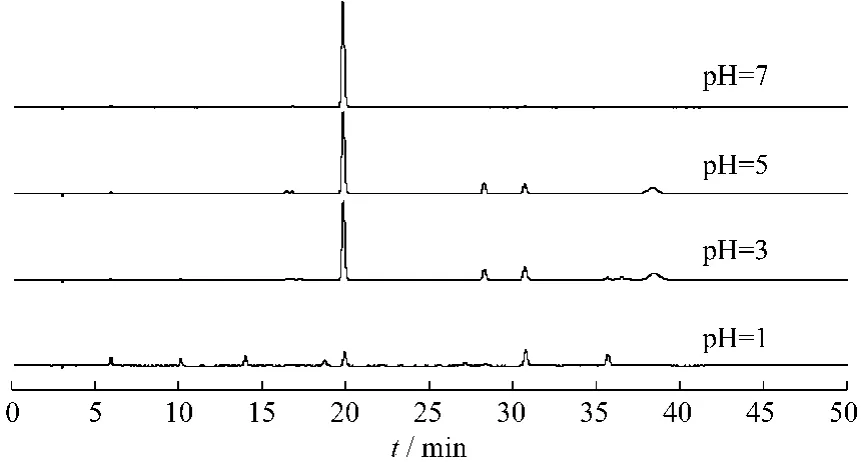
图6 60%乙醇溶液中加热回流10 h后成分变化情况Fig.6 The component changes in 60%EtOH solution after refluence 10 hours

图7 90%乙醇溶液中加热回流10 h后成分变化情况Fig.7 The component changes in 90%EtOH solution after refluence 10 hours
不同溶液中的转化关系:在水溶液中主要转化为丹参素、原儿茶醛;在乙醇溶液中可转化为丹酚酸A、丹酚酸B,且乙醇的体积分数越大转化的丹酚酸A和丹酚酸B越多。丹酚酸D在水溶液中可能是其自身发生降解转化生成丹参素和原儿茶醛;而丹酚酸D在乙醇溶液中可能发生降解和缩合反应,生成丹酚酸A和丹酚酸B。丹酚酸A为咖啡酸的三聚物,由一分子丹参素和两分子咖啡酸缩合而成,丹酚酸B为咖啡酸的四聚物,由三分子丹参素和一分子咖啡酸缩合而成。丹酚酸A、B可能的生成途径:①丹酚酸D与丹酚酸D转化得到的丹参素和原儿茶醛缩合而成;②丹酚酸D的转化产物丹参素和原儿茶醛等小分子成分缩合而成;③ 另外,丹酚酸B还可由两分子丹酚酸D缩合而成。化学结构见图8。

图8 丹酚酸A,丹酚酸B化学结构Fig.8 The chemical structures of SalA,SalB
2.5 温度对丹酚酸D稳定性影响 结果见表3。
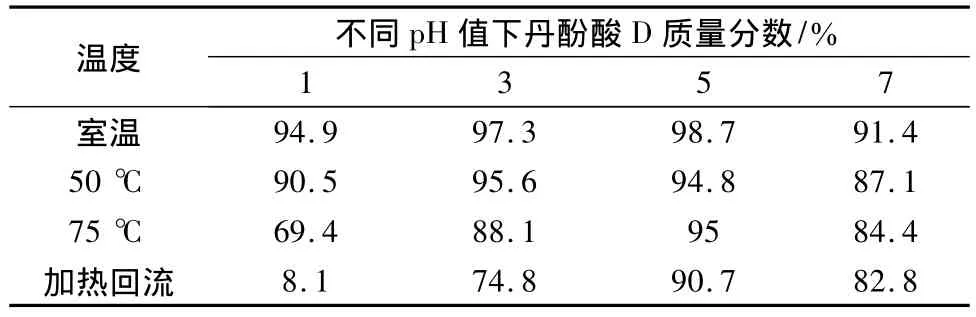
表3 不同温度10 h后变化情况Tab.3 The content changes in different temperatures after 10 hours
丹酚酸D在低温条件下稳定,峰面积变化较小,随着温度的升高丹酚酸D的峰面积逐渐减少;温度越高,丹酚酸D峰面积变化越大。
3 讨论
丹酚酸D在弱酸性条件下相对稳定;不同体积分数的乙醇溶液对丹酚酸D的稳定性影响较小;低温条件下丹酚酸D稳定,随着溶液加热温度的升高丹酚酸D峰面积逐渐减少,发生转化。丹酚酸D在水溶液中可转化为丹参素和原儿茶醛,在乙醇溶液中可转化为丹酚酸A、丹酚酸B。
丹酚酸D水溶液在高温强酸(pH=1)条件下有利于丹参素转化;丹酚酸D 90%乙醇溶液在高温弱酸(pH值为3~7)条件下有利于丹酚酸A、丹酚酸B的转化。丹酚酸D在水溶液和乙醇溶液中转化后产物不同,说明丹酚酸D在水和乙醇溶液中的转化途径存在一定的差异。
在制剂生产过程中丹酚酸D溶液应处在低温及弱酸的条件下,以防止丹酚酸D发生转化,导致成分量减少。
[1]赵 娜,郭治昕,赵 雪,等.丹参的化学成分与药理作用[J].国外医药:植物药分册,2007,22(4):155-160.
[2]Li Yongguo,Song Long,Liu Mei,et al.Advancement in analysis of Salviae miltiorrhizae Radix et Rhizoma(Danshen)[J].J Chromatogr A,2009,1216(11):1941-1953.
[3]陈 磊,陆 茵,郑仕中.丹参药理活性成分的整合效应[J].中草药,2009,40(3):476-479.
[4]朱 静,陈慧清,白 鹏,等.丹酚酸B水溶液分解反应的动力学研究[J].中成药,2009,31(4):541-544.
[5]李志刚,顾 群,渠守峰,等.一种丹参丹酚酸A的制备方法:中国,CN200710099618.8[P].2008-11-26.
[6]程翼宇,叶正良,吴永江,等.一种复方丹参滴丸质量控制方法:中国,CN200510055262.9[P].2008-04-16.
[7]Jiang Renwang,Lau Kitman,Hon Poming,et al.Chemistry and biological activities of caffeic acid derivatives from Salvia miltiorrhiza[J].Curr Med Chem,2005,12(2):237-246.
[8]徐德然,王康才,王峥涛,等.丹参中丹参素、原儿茶醛来源的初步研究[J].中国天然药物,2005,3(3):148-150.
[9]李 耿,于长安,李振坤,等.丹参煎煮化学成分溶出规律研究[J].中国实验方剂学杂志,2009,15(8):46-49.
[10]李建萍,贺英菊,闫根全,等.均匀设计法优选丹参提取液中丹参素的转化生成工艺[J].中成药,2008,30(12):1855-1857.