基于QbD理念的三七总皂苷定量分析方法持续改进研究
戴胜云++徐冰+史新元+徐翔+孙英强+乔延江


[摘要]该文提出基于质量源于设计(QbD)的中药分析方法持续改进策略。以三七总皂苷(PNS)5种皂苷类成分的超高效液相色谱(UPLC)定量分析方法开发为例,完成分析方法从HPLC到UPLC的转换。在UPLC开发中,采用PlackettBurman设计和BoxBehnken设计理解关键方法参数(CMP)与关键方法属性(CMA)之间的关系,建立贝叶斯概率设计空间;优选稳健色谱条件为初始乙腈20%,等度时间10 min,梯度变化速率6 %·min-1,分析时间17 min,采用Accuracy profile进行方法学验证。在相同的分析目标(ATP)下,从色谱条件、CMP辨识结果、CMPCMA关系模型、系统适用性等方面对PNS 的HPLC和UPLC定量分析性能的一致性进行比较,结果表明UPLC可缩短分析时间、提高关键峰对分离度、色谱系统适用性满足要求,UPLC可替代HPLC进行PNS定量分析。
[关键词]质量源于设计; UPLC; 持续改进; 贝叶斯设计空间; 三七总皂苷
[Abstract]This study is aimed to propose a continual improvement strategy based on quality by design (QbD) An ultra high performance liquid chromatography (UPLC) method was developed to accomplish the method transformation from HPLC to UPLC of Panax notogineng saponins (PNS) and achieve the continual improvement of PNS based on QbD, for example PlackettBurman screening design and BoxBehnken optimization design were employed to further understand the relationship between the critical method parameters (CMPs) and critical method attributes (CMAs) And then the Bayesian design space was built The separation degree of the critical peaks (ginsenoside Rg1 and ginsenoside Re) was over 20 and the analysis time was less than 17 min by a method chosen from the design space with 20% of the initial concentration of the acetonitrile, 10 min of the isocratic time and 6%·min-1 of the gradient slope At last, the optimum method was validated by accuracy profile Based on the same analytical target profile (ATP), the comparison of HPLC and UPLC including chromatograph method, CMA identification, CMPCMA model and system suitability test (SST) indicated that the UPLC method could shorten the analysis time, improve the critical separation and satisfy the requirement of the SST In all, HPLC method could be replaced by UPLC for the quantity analysis of PNS
[Key words]quality by design; UPLC; continual improvement; bayesian design space; Panax notogineng saponins
三七Panax notoginseng(Burk)FHChen為五加科植物,具有散瘀止血、消肿止痛之功效[1]。三七总皂苷(Panax notogineng saponins,PNS)为三七主根或根茎经加工制成的总皂苷提取物,已收录在《中国药典》2015 年版一部[2]。药典中PNS 5种皂苷类成分的含量测定采用HPLC,乙腈水梯度洗脱,流速15 mL·min-1。该法分析时间长,流速大、流动相消耗大,系统背压偏高,峰型也不尽理想。笔者曾尝试采用质量源于设计(quality by design,QbD)方法提高PNS分析方法性能。第1次方法改进时采用色谱柱(46 mm×150 mm,5 μm),将流速降低到1 mL·min-1,但分析时间没有变化[3]。第2次方法改进选择色谱柱(46 mm × 75 mm,25 μm),流速为08 mL·min-1,分析时间缩减到36 min,关键分离度为160,基本达到色谱分离的要求[4]。
超高效液相色谱(ultra high performance liquid chromatography,UPLC)具有高效、灵敏、快速的优点。本次研究中以三七总皂苷UPLC开发为例,完成分析方法从HPLC到UPLC的转换,期望缩短分析时间,减少有机溶剂消耗,并实现PNS分析方法的持续改进。在PNS的UPLC开发中,首先定义分析目标(analytical target profile,ATP),然后采用风险评估(risk evaluation)辨识关键方法属性(critical method attributes,CMAs)和键方法参数(critical method parameters,CMPs),采用回归模型建立CMAs和CMPs关系模型,基于模型开发分析方法设计空间(design space,DSp),最后基于DSp优化分析条件。方法开发完成后,以CMPsCMAs关系模型的准确性和系统适用性是否改变为判断标准,为评价分析方法改进的有效性,为新分析方法的应用提供参考。
1材料
11仪器与试剂
Acquity UPLC HClass 超高效液相色谱仪,包括四元泵处理器、样品处理器、柱温箱、TUV 检测器及Empower 色谱工作站(Waters 公司);AG135型电子分析天平(1/1万,Sartorius公司);BT25S型电子分析天平(1/10万,Sartorius公司);KQ100型超声波清洗器(昆山市超声仪器有限公司,100 W,40 KHz)。
三七总皂苷提取物(批号ZL20141208,质量分数>80%)购自南京泽朗生物科技有限公司;三七皂苷R1(批号10745201318,纯度≥98%);人参皂苷Rg1(批号110703201530,纯度≥98%);人参皂苷Re(批号110754201525,纯度≥98%);人参皂苷Rb1(批号110704201424,纯度≥942%)和人参皂苷Rd(批号111818201302,纯度≥98%)购自中国食品药品检定研究院;甲醇为色谱级,乙腈为质谱级(赛默飞世尔科技有限公司);水为屈臣氏蒸馏水。
12数据分析软件
DesignExpert V 80 (StatEase公司),Sigmplot 125(Aspire Software Intl,Ashburn,VA,USA),Matlab 2009a(Mathworks公司),数据处理程序自行编写,JMP(SAS公司)。
2方法与结果
21色谱条件
采用Acquity UPLC BEH色谱柱(21 mm×100 mm,17 μm);流动相为乙腈水先等度后梯度洗脱,检测波长203 nm,进样量2 μL,流速、柱温、梯度洗脱程序由试验设计确定。
22供試品溶液的制备
称取三七总皂苷提取物约25 mg,精密称定,置10 mL量瓶中,用70%甲醇定容至刻度线,摇匀,022 μm微孔滤膜过滤,续滤液备用。
23对照品溶液的制备
分别精密称取三七总皂苷中5种对照品适量,加70%甲醇溶解,分别从5种对照品中取一定量配制混合对照品,其中三七皂苷R1、人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1和人参皂苷Rd的质量浓度分别为0251 7,1266,0232 3,1260 1,0293 4 g·L-1。
24PlackettBurman设计
PlackettBurman设计是部分析因设计用于筛选的备选设计。主要针对因素数较多且未确定众因素相对于响应变量的显著性时采用的试验设计方法,能用最少实验次数筛选出因素的主效应,从众多考察因素中快速有效地筛选出最为重要的几个因素供进一步研究。
241参数设定选取柱温(A)、梯度变化速率(B)、流速(C)、等度时间(D)、初始乙腈浓度(E)为考察因素。根据预试验结果,为每个因素设定2个水平进行,见表1。梯度洗脱见表2。
242PlackettBurman设计结果与分析将设定的参数水平输入JMP软件的DOE筛选试验设计中,选择PlackettBurman设计,共12次,得到一个设计表。响应变量选取人参皂苷Rg1和人参皂苷Re的分离度和分析时间共2个指标进行考察。根据试验设计进行,并将结果输入响应中,见表3。
采用最小二乘法进行效应筛选模型拟合,分别得到2个关键方法属性与5个潜在关键方法参数Pareto分析图,见图1。图中黑色条框代表参数与响应成负相关关系,白色条框代表参数与响应成正相关关系,当P<005时说明参数对响应值影响明显,该参数为关键方法参数。对分析时间而言,初始乙腈浓度、梯度变化速率和等度时间模型P<005,故可作为关键方法参数;同样,梯度变化速率为关键分离度的关键方法参数。
此外,通过最小二乘法模型运算得到因素刻画图,见图2。该图为动态演示图,主要体现2个方面,一方面是因素之间是否存在相互作用,通过移动其中任何一个因素,若其他因素斜率发生改变则表明涉及因素间的交互作用,这一部分是Pareto图分析不能体现的内容;另一方面是参数对响应值影响的重要程度,主要通过观察预测迹的斜率。本实验中,未发现各因素间存在交互作用,而等度时间和梯度变化速率对2个响应值具有一定的斜率且均较明显,初始乙腈浓度对2个响应值具有一定的斜率但不及前2个因素明显,流速和温度对2个响应值影响不明显。因此,综合考虑5个因素对各响应值的影响,等度时间、初始乙腈浓度和梯度变化速率为关键方法参数进行进一步的考察,而影响较小的因素则选择一个常用值,如柱温选择室温25 ℃,流速04 mL·min-1进行后续实验。
25BoxBehnken试验设计
BoxBehnken设计与析因设计相比,可以明显减少实验次数,提高实验效率,降低实验的成本。
251参数设定根据PlackettBurman设计考察结果,选择梯度变化速率、等度时间、初始乙腈浓度为因素进行实验。因素水平、BoxBehnken因素设计见表4。
252BoxBehnken设计结果与分析将表4中的内容输入Design Expert806软件的BoxBehnken响应面试验设计中,共17次实验,见表5。以人参皂苷Rg1和人参皂苷Re间的分离度、分析时间为关键方法属性进行优化。
根据结果,分别以分析时间和分离度为响应值,建立响应值与3个关键影响参数梯度变化速率、初始乙腈浓度和等度时间之间的二项式模型,模型P<005,具有显著性,并且模型决定系数R2分别为0999 9,0878 1,表明模型拟合程度良好,可以解释关键影响因素与关键方法属性之间的相互关系。
26设计空间开发及其可靠性研究
BoxBehnken试验设计是响应面设计中的一种,而设计空间又是在BoxBehnken试验设计数据上建立的,故可认为设计空间的建立是基于预测响应面[5]。由于建立色谱方法时往往会牵涉到多个色谱参数和多个响应,因而设计空间应该是多个响应面的综合。然而Peterson[6]提出,这样由多个响应变量建立的设计空间有2个主要缺点,将直接导致设计空间的不可靠,其中一个缺点是模型参数
不确定性,另一个缺点是没有考虑多元回归模型误差向量的相关结构。因此,在建立设计空间时,有必要同时考虑这2个缺点来确保设计空间的可靠性,这样才能满足ICH Q8指南中对设计空间定义中的“保证质量”这一项要求,Bayesian理论恰好能同时考虑模型参数的不确定性和数据结构的相关性。根据Bayesian理论,Bayesian后验预测概率可以通过下式来计算[7]。
Pr(yA|x,data)(1)
其中,x是过程参数向量,y是响应值向量,A是具有规定阈值的可接受范围,data是实验数据,Pr代表响应值在可接受范围内的概率,故设计空间可以用下式表示。{x:Pr(yA|x,data)≥π}(2)其中,π表示能“確保质量”的设计空间预定义可靠性的概率。那些不确定因素对模型响应的影响应用Monte Carlo仿真模拟来估计。
在建立贝叶斯设计空间之前,首先要确定分析目标。本实验中,选择2个分析目标:①实现三七总皂苷中5种皂苷的基线分离,尤其是人参皂苷Rg1和人参皂苷Re;②缩短分析时间,提高分析效能,基于贝叶斯概率可建立一个多目标设计空间。
根据分析目标,选择关键分离度(Rcrit)和分析时间(t)作为三七总皂苷色谱分离的关键方法属性,该多变量设计空间可以用下式表示。
DS={x0X|Eθ[Pr(Rcnt>λ1,t>λ2)|θ]≥π(3)
其中,x0是整个实验区域X中的一个点,λ1和λ2是关键分离度与分析时间的可接受阈值,π为要求达到的质量水平的贝叶斯概率值,θ为模型评估参数的数据集,Pr和E代表概率的估计值和数学期望值。
一般而言,关键分离度Rcrit至少应该大于15,而对于分析时间t,考虑到中药的复杂性和UPLC特点,将其设置为17 min,设计空间就是理论上的稳健区域,区域中预测标准值高于可接受阈值并且尽可能至少达到此阈值[8]。此外,利用网格搜索法在整个实验范围内进行贝叶斯联合后验概率的计算,满足2个分析目标的贝叶斯后验预测概率通过对每个网格进行1万次的Monte Carlo仿真模拟计算得到[810]。
目前并没有一个针对色谱分析公认的概率阈值,故在本研究中选择88%作为π的基本标准建立设计空间,见图3,图中设计空间用黑线条描绘出来,设计空间内表示同时满足关键分离度和分析时间2个目标要求的概率至少大于88%,颜色越深,概率越大。
通过对三七总皂苷色谱分析过程的优化,采取Bayesian概率评价设计空间的可靠性,最后优化得到的分析方法的预测结果为10 min的等度时间,6 %·min-1的梯度变化速率和20%的初始乙腈浓度,此时可以实现三七总皂苷中5个成分的完全分离,见图4。
27方法验证
选择Accuracy profile[11]进行方法验证,分3 d进行,选择4个样品浓度,每个浓度进行3次重复,一共进行3×4×3次,即36次实验。三七总皂苷样品的4个质量浓度分别是125,25,30,50 g·L-1。每个浓度分别重复3次,实验分3 d考察方法的中间精密度。根据全析因设计和β期望容许区间计算Accuracy Profile中各个参数的值,验证试验采用matlab自行编写的程序进行计算。
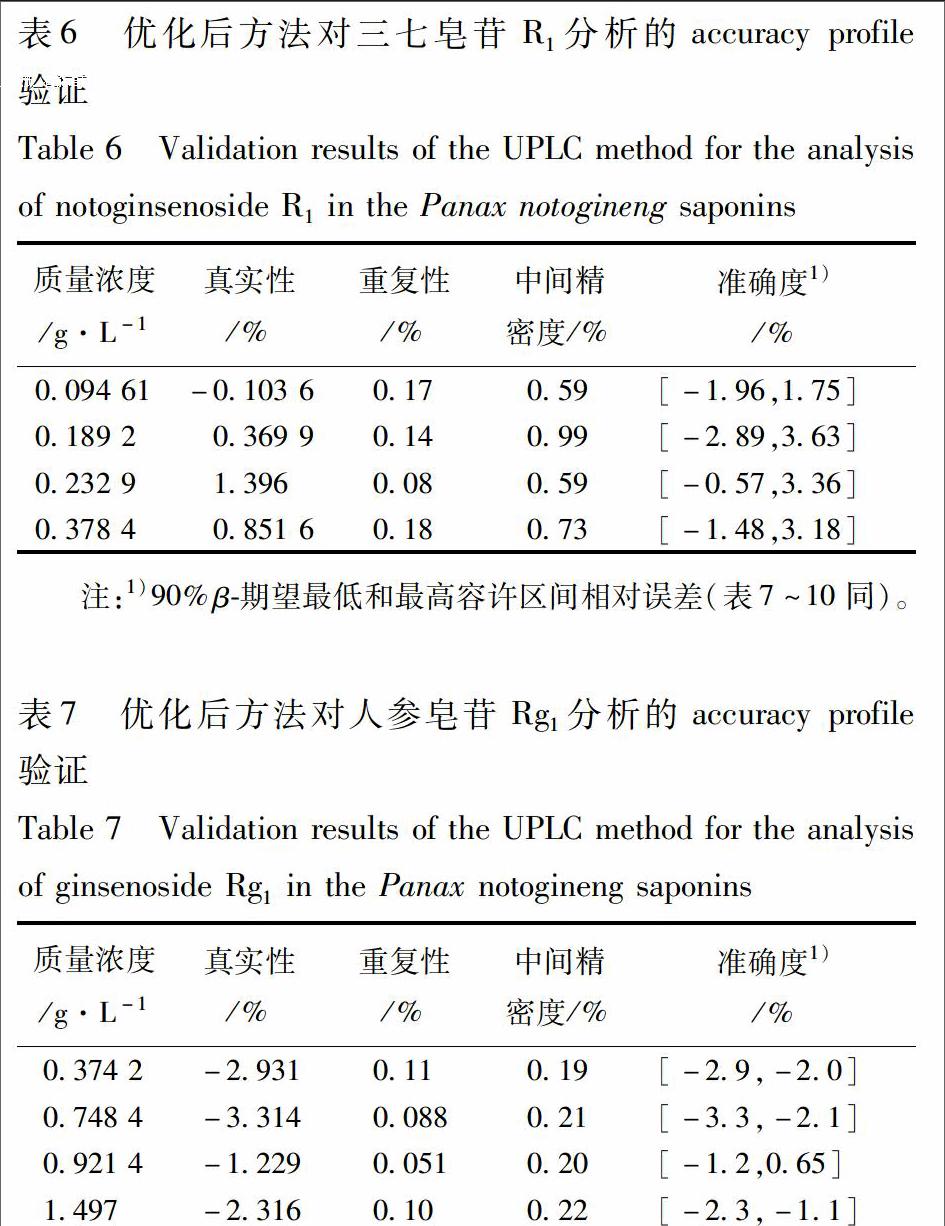
271真实性真实性代表总误差理论中的系统误差,分别用每个浓度3 d重复3次数据的相对偏差表示。5个成分相对偏差都小于5%,这说明优化后方法的真实性可接受,三七皂苷R1、人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1和人参皂苷Rd方法验证的结果见表6~10。三七皂苷R1、人参皂苷Rg1、人参皂苷Rb1和人参皂苷Rd 4个成分的相对偏差都小于3%,而人参皂苷Re前2个浓度水平的相对偏差分别为35%,32%,这可能因为人参皂苷Re含量较低,测量时存在偏差会比其他4个成分稍大。
272精密度精密度与总误差理论中的偶然误差有关,包括2个方面,分别是重复性和中间精密度,二者都用RSD表示。5个成分在4个浓度水平的重复性和中间精密度的RSD都小于2%,意味着优化后方法的偶然误差在可接受范围内,见表6~10。
273准确性准确性代表着误差理论中偶然误差与系统误差值之和,即总误差。三七皂苷R1、人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1和人参皂苷Rd 5个成分在90%β容许区间内并且可接受限
为5%的准确性,见表6~10,轮廓图见图5。除人参皂苷Rd以外,其他4个成分在设置的4个浓度水平都分布在可接受范围内,说明优化后的方法其准确性在设定的样品浓度范围内是可以接受的。但人参皂苷Rd则在第4个浓度水平处超过了5%可接受限,说明其浓度范围比其他4个成分浓度范围窄。此外,优化后方法在对三七总皂苷中5个成分进行分析时,不同成分的分析范围不一样,但方法准确性可接受。三七皂苷R1的分析范围为0094 61~0378 4 g·L-1,人参皂苷Rg1为0374 2~1497 g·L-1,人参皂苷Re为0039 16~0156 6 g·L-1,人参皂苷Rb1为0448 7~1795 g·L-1,人参皂苷Rd为0132 4~0493 2 g·L-1。
a 三七皂苷 R1;b人参皂苷 Rg1;c人参皂苷 Re;d人参皂苷 Rb1;e人参皂苷 Rd;绿色点为每个浓度每次试验的相对误差,红色实线为相对偏差,蓝色折线表示90%β期望容许区间,黑色点直线为±5%可接受限。
274最低定量限每个成分的最低定量限(limit of qualification,LOQ)也可从准确性轮廓图中看出,准确性轮廓限制线与90% β容许区间限制线的交叉点即为最低定量限。从试验设计的浓度来看,三七皂苷R1、人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1和人参皂苷Rd 5个成分的最低定量限分别为0094 61,0374 2,0039 16,0448 7,0132 4 g·L-1。
275线性为了考察方法的线性,对36次实验数据采取线性回归模型拟合方式得到5个成分的线性方程,三七皂苷R1、人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1和人参皂苷Rd的线性方程分别为Y=4928+1510×106X,Y=-1359+1706×106X,Y=-0479 5+1849×106X,Y=0917 9+1313×106X和Y=1907×104+1570×106X,此5个成分线性方程对应的相关系数均大于0999 5,表明方法的线性良好。
28方法持续改进前后定量分析性能比较
在相同的分析目标(ATP)下,从色谱条件、CMP辨识结果、CMPCMA关系模型、系统适用性等方面对笔者前期建立的三七总皂苷HPLC分析[34]和UPLC分析的性能进行比较,见表11。UPLC中选擇色谱柱(21 mm × 100 mm,17 μm)进行方法开发,人参皂苷Rg1和Re之间的分离度有较大改善,达到210以上,同时分析时间缩短到17 min,见图6。从CMPCMA关系模型角度来看,采用的试验设计方法一致,关键影响参数一致,模型R2符合要求,而设计空间的阈值更高,说明改进以后方法的稳健性更高,更能够满足预定义目标。本次改进方法同样经过accuracy profile方法学验证,真实性、中间精密度、重复性、分析总误差和线性均符合要求。因此,改进后的分析方法同样满足药典中PNS的定量分析要求,利于三七总皂苷质量控制,应用QbD工具提高了分析方法开发的效率和可靠性。
3总结
本研究建立了UPLC测定三七总皂苷中三七皂苷R1、人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1和人参皂苷Rd 5种皂苷的Bayes概率设计空间,该方
法一改常规单因素考察建立操作条件单一的色谱方法,而是基于科学和风险管理原则开发色谱方法的设计空间,增加了对三七总皂苷色谱分析过程的理解,设计空间内色谱条件的改变不会引起分析性能的改变,提高了色谱方法的稳健性。
QbD希望在药品监管和药品分析中取得一个平衡,实现监管者、分析者和使用者三者之间共赢[12]。本研究在前期研究基础上对分析方法进行持续改进,提出采用CMPsCMAs关系模型的拟合和预测指标,以及关键分离度、选择性、塔板数等系统适用性指标,评价持续改进效果和改进前后分析性能的一致性,更大程度提高方法的可靠性和可维护性,既满足监管要求,又有利于新技术的应用。
[参考文献]
[1]中国药典 一部[S] 2015: 11
[2]中国药典 一部[S] 2015: 393
[3]Dai S Y, Xu B, Luo G, et al Application of design of experiment and design space (DOEDS) methodology for the HPLC separation of Panax Notogineng Saponins[J] Open Chem Eng J, 2015, 9: 47
[4]Dai S Y, Zhang Y, Xu B, et al Robust design space development for HPLC analysis of five chemical components in Panax notoginseng saponins [J] J Liq Chromatogr Relat Techno, 2016, 39(10):504
[5]Peterson J J A Bayesian approach to the ICH Q8 definition of design space [J] J Biopharm Stat, 2008, 18(5): 959
[6]Peterson J J A posterior predictive approach to multiple response surface optimization [J] J Qual Technol, 2004, 36(2): 139
[7]Dai S Y, Xu B, Zhang Y, et al Establishment and reliability evaluation of the design space for HPLC analysis of six alkaloids in Coptis chinensis (Huanglian) using Bayesian approach [J] Chin J Nat Med, 2016, 14(9): 697
[8]Debrus B, Lebrun P, Ceccato A, et al Application of new methodologies based on design of experiments, independent component analysis and design space for robust optimization in liquid chromatography [J] Anal Chim Acta, 2011, 691(1): 33
[9]Lebrun P, Govaerts B, Debrus B, et al Development of a new predictive modelling technique to find with confidence equivalence zone and design space of chromatographic analytical methods [J] Chemom Intell Lab Sys, 2008, 91(1) 4
[10]Debrus B, Lebrun P, Ceccato A, et al A new statistical method for the automated detection of peaks in UVDAD chromatograms of a sample mixture [J] Talanta, 2009, 79(1): 77
[11]Feinberg M Validation of analytical methods based on accuracy profiles [J] J Chromatogr A, 2007, 1158: 174
[12]徐冰,史新元,吴志生, 等.论中药质量源于设计[J].中国中药杂志,2017,42(5):1015.[责任编辑孔晶晶]

