咖啡酸片治疗肿瘤化疗所致血小板减少症的临床观察
沈志祥 马军
咖啡酸片治疗肿瘤化疗所致血小板减少症的临床观察
沈志祥①马军②
目的:观察咖啡酸片治疗肿瘤化疗所致血小板减少症(chemotherapy induced thrombocytopenia,CIT)的临床疗效及安全性。方法:采用自身对照的方法,选取上海交通大学医学院附属瑞金医院等11家三级甲等医院2016年1月22日至2017年1月10日收治的60例肿瘤化疗所致CIT患者。给予咖啡酸片/模拟剂治疗,均为3片/次,3次/d。第1个化疗周期(阴性对照期)于化疗开始第1 d给予咖啡酸片模拟剂;第2、3个化疗周期(药物治疗期)需要接受与第1个化疗周期相同方案及剂量的化疗,分别于化疗开始第1 d给予咖啡酸片。结果:药物治疗期最低血小板(platelet,PLT)的升高值显著高于阴性对照期(P<0.001);药物治疗期化疗后,PLT恢复后最高值显著高于阴性对照期(P<0.001);药物治疗期PLT<50×109/L的持续天数与阴性对照期无显著性差异,但有缩短趋势(P>0.05);药物治疗期化疗后PLT恢复至≥75×109/L和≥100×109/L,所需的天数较阴性对照期均明显减少(P<0.001);试验期间无患者行PLT输注。结论:咖啡酸片用于肿瘤化疗所致CIT患者,疗效确切,不良反应较少,具有广泛的临床应用前景。
咖啡酸片 肿瘤化疗 血小板减少症
AbstractObjective:To evaluate the clinical efficacy and safety of caffeic acid for thrombocytopenia induced by cancer chemotherapy.Methods:A total of 60 patients received the same chemotherapy treatment on cycles 1,2,and 3.They were given mimetic agent as negative control on the first course.On the second and third cycles,caffeic acid tablets were given from the first day of chemotherapy.Results:The lowest and highest platelet levels of the treatment group during the drug treatment period were significantly higher than those of the negative control group(P<0.001).No significant difference in the period of days of PLT<50×109/L was observed between the groups,although a decreasing trend(P>0.05)was observed.After chemotherapy,the days required for platelet recovery to PLT≥75×109/L and PLT≥100×109/L in the treatment group was significantly fewer than in the negative control group(P<0.001).All the patients did not receive any platelet transfusion during the trial.Conclusion:Caffeic acid tablets were safe and effective for thrombocytopenia induced by tumor chemotherapy.
Keywords:caffeic acid tablets,tumor chemotherapy,thrombocytopenia
化疗作为肿瘤治疗的重要手段之一,对控制肿瘤的效果明显,可延长患者的生存时间。然而,许多化疗药物和联合化疗方案均可出现不同程度的血小板(platelet,PLT)减少[1,2-5]。肿瘤化疗所致血小板减少症(chemotherapy induced thrombocytopenia,CIT)是抗肿瘤化疗药物对骨髓产生的抑制作用,尤其是对巨核细胞产生抑制作用,导致外周血PLT计数<100×109/L[2,6]。目前,国内对 CIT 常用的处理方法主要为输注PLT和使用PLT生长因子等[1],虽有一定疗效,但由于血制品紧缺及不良反应、价格等因素,临床应用受到限制[5-6]。为明确咖啡酸片治疗肿瘤化疗所致CIT的疗效及安全性,本研究对该类型患者进行系统研究。
1 材料与方法
1.1 病例资料
选取上海交通大学医学院附属瑞金医院等11家三级甲等医院2016年1月22日至2017年1月10日收治的60例肿瘤化疗所致CIT患者。其中男性26例,女性34例,平均年龄为(38.90±8.43)岁。60例患者分别诊断为淋巴瘤、卵巢癌、肺癌、肝癌等多种肿瘤。采用的化疗方案分别为淋巴瘤CHOP方案、肺癌EP与NP方案、肝癌FOLFOX4方案和胃癌ECF方案及SP方案等多种肿瘤经典化疗方案。入组标准:第1个化疗周期50×109/L<PLT<100×109/L的患者皆入选本研究,且在本研究期间不改变化疗方案;体力状况评分(eastern cooperative oncology group,ECOG)0~2分,预估生存期≥6个月;骨髓造血功能基本正常,即化疗前PLT>100×109/L,中性粒细胞绝对值|ANC|≥1.5×109/L,血红蛋白≥9.5 g/dL;既往未接受脾切除术。本研究经被研究对象或其家属知情同意及符合人体试验委员会所制定的伦理学标准并得到伦理委员会批准。
作者单位:①上海交通大学医学院附属瑞金医院(上海市200025);②哈尔滨血液病肿瘤研究所
1.2 方法
1.2.1 给药方法 研究采用自身对照法,分为3个化疗周期,即第1个化疗周期于化疗开始第1 d给予咖啡酸片模拟剂,口服,3片/次,3次/d,用药21或28 d,化疗结束后监测外周PLT,作为第2、3个化疗周期的阴性对照值,且符合CIT的受试者(第1个化疗周期出现:50×109/L<PLT<100×109/L),并允许这部分受试者进入第2、3个化疗周期,反之则自动退出。第2、3个化疗周期为药物治疗期,要求接受与第1个化疗周期相同的化疗方案及剂量,并分别于化疗开始第1 d给予咖啡酸片(国药准字H37020537,规格:0.1 g/片,德州德药制药有限公司提供),用法及用量与第1个化疗周期相同,若出现连续2次PLT测定值恢复至≥175×109/L以上,则停药。如PLT<10×109/L或有出血倾向,临床给予PLT输注和重组人促血小板生成素(recombinant human thrombopoietin,rh TPO)进行紧急治疗;若10×109/L≤PLT<50×109/L,但未伴出血表现,必要时考虑采用rhTPO和(或)白介素11(interleukin 11,IL-11)进行预防治疗。
1.2.2 观察指标 药物治疗期与阴性对照期相比,观察指标为:1)化疗后最低PLT值和最高PLT值的差值;2)化疗后PLT恢复后最高值;3)PLT<50×109/L的时间(天数);4)化疗后PLT恢复至≥75×109/L以及≥100×109/L所需的天数;5)PLT输注情况。各化疗周期于化疗前,化疗后第(4±1)d、(7±1)d、(10±1)d、(14±1)d、(21±3)d、(28±3)d检查血常规。观察受试者用药后的不良反应发生情况。
1.3 统计学分析
采用SAS 9.4软件进行统计学分析。所有的统计检验均采用双侧检验。计量资料采用±s表示;计数资料采用频数(构成比)进行统计描述。治疗前后数据比较为配对资料。计量数据采用配对t检验或符号秩检验,计数资料采用McNemar检验。以P<0.05为差异具有统计学意义。
2 结果
2.1 各化疗周期化疗后PLT计数
患者在第2、3个化疗周期后服用咖啡酸片,其PLT计数较第1个化疗周期有显著升高,两者比较差异均具有统计学意义(均P<0.001,表1)。患者每个化疗周期结束后,PLT计数明显降低,但患者第2个化疗周期后服用咖啡酸片,PLT计数下降趋势减弱,并在第3个化疗周期后PLT计数呈上升趋势(图1)。

表1 第1、2、3个周期化疗后PLT计数的比较 (109/L)Table 1 Difference in the platelet counts among the first,second,and third cycle chemotherapy(109/L)

图1 试验过程中PLT变化趋势图 (109/L)Figure 1 Trends of variation in platelet level during the study(109/L)
2.2 服用咖啡酸片对化疗后最低PLT值的影响
对60例患者的化疗后最低PLT值进行分析。患者每个化疗周期结束后,其PLT计数明显降低。但是,患者第2、3个化疗周期后服用咖啡酸片,其最低PLT计数均较第1个化疗周期有显著升高,改善了患者因化疗所致PLT减少的影响,两者比较差异均具有统计学意义(均P<0.001,表2)。

表2 第1、2、3个周期化疗后最低PLT计数的比较 (109/L)Table 2 Difference in minimum platelet count among the first,second,and third cycle of chemotherapy(109/L)
2.3 服用咖啡酸片对化疗后PLT恢复至最高值的影响
第2、3个化疗周期与第1个化疗周期相比,化疗后PLT恢复至最高值前后差值分别为(14.10±28.11)×109/L、(50.98±31.39)×109/L,差异均具有统计学意义(均P<0.001)。从结果可见,患者服用咖啡酸片后,其化疗后PLT恢复至最高值较未服用咖啡酸片的患者存在显著性差异(表3)。

表3 第1、2、3个周期化疗后最高PLT计数的比较 (109/L)Table 3 Difference inmaximumplatelet count among the first,second,and third cycle of chemotherapy(109/L)
2.4 服用咖啡酸片对化疗后PLT<50×109/L的时间的影响
第2个化疗周期后59例患者和第3个化疗周期后54例患者PLT<50×109/L持续天数与第1个化疗周期相比较,差异均无统计学意义(P>0.05)。患者服用咖啡酸片后,可减轻PLT下降幅度及缩短PLT持续下降的时间(表4)。

表4 第1、2、3个周期化疗后PLT<50×109/L持续天数的比较Table 4 Difference in the platelet<50×109/L duration among the first,second,and third cycle of chemotherapy
2.5 服用咖啡酸片对化疗后PLT恢复至≥75×109/L及≥100×109/L所需天数的影响
第2个化疗周期后59例和第3个化疗周期后54例患者PLT恢复至≥75×109/L所需天数与第1个化疗周期进行比较,差异均具有统计学意义(均P<0.001);而化疗后PLT恢复至≥100×109/L所需天数,第2个化疗周期与第1个化疗周期进行比较,差异无统计学意义(P>0.05),第3个化疗周期与第1个化疗周期进行比较,差异具有统计学意义(P<0.001)。提示咖啡酸片可提高PLT计数,且可能在第2、3个周期达到治疗效果的高峰值(表5,6)。
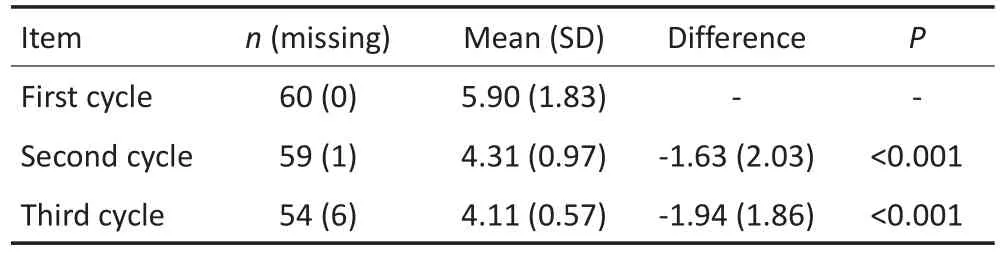
表5 第1、2、3个周期化疗后PLT恢复至≥75×109/L所需天数的比较Table 5 Difference in platelet≥75×109/L duration among the first,second,and third cycle of chemotherapy

表6 第1、2、3个周期化疗后PLT恢复至≥100×109/L所需天数的比较Table 6 Difference in platelet≥100×109/L duration among the first,second,and third cycle of chemotherapy
2.6 服用咖啡酸片对PLT输注次数的影响
1)试验期间所有患者均未行PLT输注(表7);2)应用咖啡酸片的不良反应:咖啡酸片组仅1例在用药第4个周期出现Ⅰ度肝转氨酶升高,另有1例服药1周后出现Ⅰ度恶心,经对症处理后,未停用咖啡酸片,均自行好转。

表7 第1、2、3个周期化疗后血小板输注情况Table 7 Condition of platelet transfusion after the second and third cycle of chemotherapy
3 讨论
肿瘤化疗所致的CIT为临床常见的化疗药物剂量限制性不良反应,有可能导致降低化疗药物剂量或延迟化疗时间,甚至终止化疗,影响临床疗效和患者生存,并增加医疗费用[7-9,14]。目前,化疗后CIT的治疗手段主要为输注PLT、rhTPO、IL-11等,但临床应用皆存在各自的限制[9-13]。为保证化疗的顺利进行,临床化疗过程中通常联合使用拮抗化疗不良反应的药物,以最大限度地减少不良反应的发生率和严重程度,提高化疗期间患者的生存质量和对化疗的依从性[1,9-10]。咖啡酸片的主要成分为咖啡酸,咖啡酸又名3-(3,4-二羟苯基)-2-丙烯酸,属于酚酸类化合物[11-12],广泛存在于植物中,是天然、安全的自由基淬灭剂[11-13]。经研究证实,咖啡酸片主要为通过刺激巨核细胞成熟,增加巨核细胞总数,可有效地预防及治疗药物对PLT减少的不良反应,具有抗氧化、抗细胞凋亡作用,从而升高PLT计数[11]。有研究显示,咖啡酸片可有效预防并减轻化疗过程中的骨髓抑制,有利于白细胞及PLT恢复正常[9,14]。本研究旨在观察咖啡酸片治疗肿瘤化疗所致CIT的临床疗效及安全性。对60例肿瘤化疗所致CIT患者服用咖啡酸片/模拟剂治疗的观察显示,服用咖啡酸片的药物治疗期与服用咖啡酸片模拟剂的阴性对照期相比,药物治疗期患者的PLT计数显著升高,PLT下降幅度及PLT持续下降的时间与阴性对照期虽无显著性差异,但仍能显现出降低的程度减轻和缩短的趋势,在持续用药疗程后,PLT恢复反应所需时间随之缩短,且试验期间所有患者均未行PLT输注,如期完成化疗并取得了较好的疗效。
综上所述,咖啡酸片用于肿瘤化疗所致CIT患者,疗效确切,不良反应较少,且口服方便,具有较好的临床应用前景。
[1]Li JC,Huang XY.Clinical study of Chinese and western medicine in the treatment of thrombocytopenia caused by chemotherapy[J].China Modern Medi,2015,22(17):15-17.[李金成,黄星尧.中西药物治疗化疗致血小板减少的临床研究[J].中国当代医药,2015,22(17):15-17.]
[2]Ma J,Qin SK,Wu YL.Consensus of Chinese experts on the diagnosis and treatment of chemotherapy induced thrombocytopenia 2014[J].Chin J Oncol,2014,36(11):876-879.[马军,秦叔逵,吴一龙 .肿瘤化疗所致血小板减少症诊疗中国专家共识(2014版)[J].中华肿瘤杂志,2014,36(11):876-879]
[3]Kaushansky K.The thrombocytopenia of cancer.Prospects for effective cytokine therapy[J].Hematol Oncol Clin North Am,1996,(10):431-455.
[4]Elting LS,Rubenstein EB,Martin CG,et al.Incidence,cost,and outcomes of bleeding and chemotherapy dose modification among solid tumor patients with chemotherapy-induced thrombocytopenia[J].J Clin Oncol,2001,19(4):1137-1146.
[5]Kuter DJ,Begley CG.Recombinant human thrombopoietin:basic biology and evaluation of clinical studies[J].Blood,2002,(100):3457-3469.
[6]Saroj Vadhan-Raj.Management of chemotherapy-induced thrombocytopenia current status of thrombopoic agents[J].Seminars in Hematology,2009,46(2):s26-32.
[7]Zhang MH,Zhang YY.The research progress of Chinese medicine in the prevention and treatment of thrombocytopenia caused by chemotherapy[J].Mod J Int Tradi Chin West Medi,2009,18(23):2868-2870.[张苗海,张英羽.中医药防治化疗后血小板减少症的研究进展[J].现代中西医结合杂志,2009,18(23):2868-2870.]
[8]Sun H,Li ZD,Xue D,et al.Clinical efficacy of Chinese medicine cervus blood granule for thrombocytopenia induced bychemotherapy[J].Evaluationand Analysis of Drug-Use in Hospitals of China,2011,12(9):832-833.[孙红,李占东,薛冬,等.中药鹿血晶治疗化疗后血小板减少症的临床观察[J].中国医院用药评价与分析,2011,12(9):832-833.]
[9]Sun T,Fang MZ,Clinical therapy progress in throm bocytopenia after chem otherapy[J].J Liao ning Uni TCM,2013,15(3):244-247.[孙婷,方明治.化疗致血小板减少症临床治疗进展[J].辽宁中医药大学学报,2013,15(3):244-247.]
[10]Xie CG,Wang JF,Xiang Y,et al.Marrow mesenchymal stem cells transduced with TPO/FL genes as support for ex vivo expansion of hematopoietic stem/progenitor cells[J].Cell Mol Life Sci,2005,62(21):2495-2507.
[11]Cai RG,Xu BH,Huang J.Recombinant human thrombopoietin in prevention of chemotherapy-induced thromcytopenia[J].Chin J Cancer Pre Tre,2009,16(9):707-709.[蔡锐刚,徐兵河,黄镜.重组人血小板生成素预防化疗引起血小板减少症的临床观察[J].中华肿瘤防治杂志,2009,16(9):707-709.]
[12]Tsimberidou AM,Giles FJ,Khouri I,et al.Low-dose interleukin-11 in patients with bone marrow failure:update of the M.D.Anderon Cancer Center experience[J].Ann Oncol,2005,16(1):139-145.
[13]Isaacs C,Robert NJ,Bailey FA,et al.Randomized placebocontrolled study of recombinant human interleukin-11 to prevent chemotherapy-induced thrombocytopenia in patients with breast cancer receiving dose-intensive cyclophosphamide and doxorubicin[J].J Clin Oncol,1997,15(11):3368-3377.
[14]Ma J.Expert consensaus on rational use of recombinant human IL-11 for thrombocytopenia in solid tumor patients[J].Chin J Oncol,2010,32(12):948-950.[马军.重组人白细胞介素11在血液病实体瘤血小板减少症合理应用的专家共识[J].中华肿瘤杂志,2010,32(12):948-950.]
(2017-07-13收稿)
(2017-09-08修回)
(编辑:孙喜佳 校对:郑莉)
Clinical observation of caffeic acid in the treatment of thrombocytopenia(CIT)caused by cancer chemotherapy
Zhixiang SHEN1,Jun MA2

10.3969/j.issn.1000-8179.2017.17.861
Correspondence to:Zhixiang SHEN;E-mail:drshenzx@126.com
1Ruijin Hospital,Shanghai Jiaotong University School of Medicine,Shanghai 200025,China;2Harbin Institute of Hematology&Oncology,Harbin 150010,China
沈志祥 drshenzx@126.com
沈志祥 专业方向为血液系统恶性肿瘤的诊断及治疗。
E-mail:drshenzx@126.com

