丁苯酞对血管性痴呆大鼠海马CA1区Bax和Bcl-2表达的影响
姚 刚 朱博驰 于挺敏 满玉红
(吉林大学第二医院神经内科,吉林 长春 130041)
丁苯酞(NBP)是人工合成的消旋正丁基苯酞,是治疗缺血性脑卒中的国家级一类新药,能够明显减轻急性缺血性脑卒中患者中枢神经功能缺损〔1〕。目前发现NBP对血管性痴呆(VD)也有较明显的改善作用〔2,3〕,但其作用机制还缺乏深入的研究。脑血管病后慢性脑缺血是VD最常见的病因,其病理机制与脑缺血引发的认知功能相关脑区神经细胞凋亡、氧化应激、能量代谢障碍、兴奋性氨基酸、炎性因子、胆碱能通道功能受损等多种因素有关,其中细胞凋亡学说是人们研究的热点〔4,5〕。B淋巴细胞淋巴瘤(Bcl)-2家族,通过线粒体相关信号通路调节细胞凋亡〔6〕,其中以Bax基因为代表的促凋亡基因与以Bcl-2基因为代表的抗凋亡基因相互拮抗,实现对细胞凋亡的调控。本研究通过观察NBP对VD大鼠海马CA1区Bax和Bcl-2表达的影响,探讨NBP对VD大鼠的保护作用及机制。
1 材料和方法
1.1实验动物、主要试剂和仪器 80只健康SPF级Wistar大鼠(雌雄各半),体重200~220 g,购于吉林大学基础医学院动物中心,动物合格证号:SCXK(吉)2003-001。丁苯酞氯化钠注射液(石药集团恩必普药业有限公司,批准文号:国药准字H20100041)。大鼠抗Bcl-2多克隆抗体、抗Bax多克隆抗体购自北京博奥森生物公司。
1.2分组 大鼠饲养于吉林大学第二医院动物实验室,室内温度22℃~26℃,相对湿度40%~60%,光暗周期12 h,自由摄取食物和水,动物模型制备前适应性喂养7 d。按随机分组法分为VD组、NBP治疗组、NBP对照组、Sham组,每组20只,每组又分为4个亚组:术后1、2、4、8 w,每个亚组5只。
1.3动物模型制备 采用永久性双侧颈总动脉结扎法制备VD大鼠模型。VD组和NBP治疗组大鼠术前禁食、禁水8 h,10%水合氯醛(0.3 ml/100 g)腹腔注射麻醉,仰卧位固定于操作台,常规消毒颈部手术区域,颈前正中作一长约1 cm的纵形切口,钝性逐层分离皮下软组织、颈前肌群,分离出气管侧后方的颈动脉鞘,进而分离颈总动脉与迷走神经,以1号丝线永久结扎颈总动脉,同法结扎另一侧颈总动脉。局部消毒后恢复组织层次并缝合皮肤。Sham组和NBP对照组大鼠除不结扎双侧颈总动脉外,其余操作与VD组和NBP治疗组大鼠一致。术后动物另放于干净鼠笼饲养,自由获取水源及饲料。
1.4药物干预 NBP对照组和NBP治疗组大鼠清醒后(术后1 d,可在笼中自由活动),给予丁苯酞氯化钠注射液腹腔注射,剂量为5 mg·kg-1·d-1(药物剂量根据成人常规每日剂量进行换算),Sham组和VD组大鼠给予生理盐水腹腔注射(0.2 ml/d)。各组大鼠连续腹腔注射给药7 d。
1.5标本采集及免疫组化 各组大鼠在术后各时间点(1、2、4、8 w),给予10%水合氯醛腹腔注射麻醉(麻醉剂量0.3 ml/100 g),生理盐水心脏灌注5 min,断头取脑,分离出海马,将组织块迅速置入10%中性甲醛固定48 h,PBS洗脱3次,80%~100%梯度酒精脱水,二甲苯透明后,石蜡包埋,制成厚度为4 μm的切片。免疫组化方法采用SP法。
1.6显微图像采集及分析 每张切片于400倍镜下随机选取5个视野,利用Leica Qwin图像分析系统检测阳性表达灰度值,同时计算每个视野下的阳性细胞总数占所有细胞总数的比率,细胞表达平均灰度计算采用视野灰度×阳性细胞比率,以5个视野的平均值表示。
1.7统计学分析 采用SPSS17.0软件包组间差别采用单因素方差分析和Tukey比较。
2 结 果
2.1Bax蛋白在各组大鼠海马CA1区的表达 Bax蛋白阳性表达显示为黄棕色颗粒,主要定位于细胞质。VD组大鼠海马CA1区神经元数目较少,排列紊乱,部分细胞出现空泡样变性,Bax表达呈强阳性,主要位于神经元。NBP治疗组大鼠海马CA1区神经元损伤明显减小,Bax表达显著减弱。见图1,图2。

图1 1 w、2 w Bax蛋白在各组大鼠海马CA1区的表达(DAB,×400)
VD组和NBP治疗组大鼠1 w、2 w、4 w和8 w时海马CA1区Bax蛋白表达灰度明显高于Sham组(P<0.05);NBP治疗组大鼠4 w和8 w时海马CA1区Bax蛋白表达均明显低于VD组大鼠相应时间点(P<0.05)。VD组大鼠不同时间点CA1 区Bax表达灰度比较,8 w组明显高于1 w和2 w组(P<0.05)。见表1。
2.2Bcl-2蛋白在各组大鼠海马CA1区的表达 Bcl-2蛋白阳性表达显示为黄棕色颗粒,主要定位于细胞质。VD组大鼠海马CA1区Bcl-2蛋白表达弱或无表达,NBP治疗组大鼠海马CA1区 Bcl-2表达显著增加,NBP对照组大鼠海马CA1区Bcl-2表达最强,NBP对照组和Sham组大鼠海马组织结构完好,神经细胞分布正常,Bcl-2表达中等程度或低表达。见图3,图4。

表1 各组大鼠海马CA1区Bax表达灰度比较
与Sham组比较:1)P<0.05;与VD组比较:2)P<0.05;与同组8 w比较;3)P<0.01;下表同
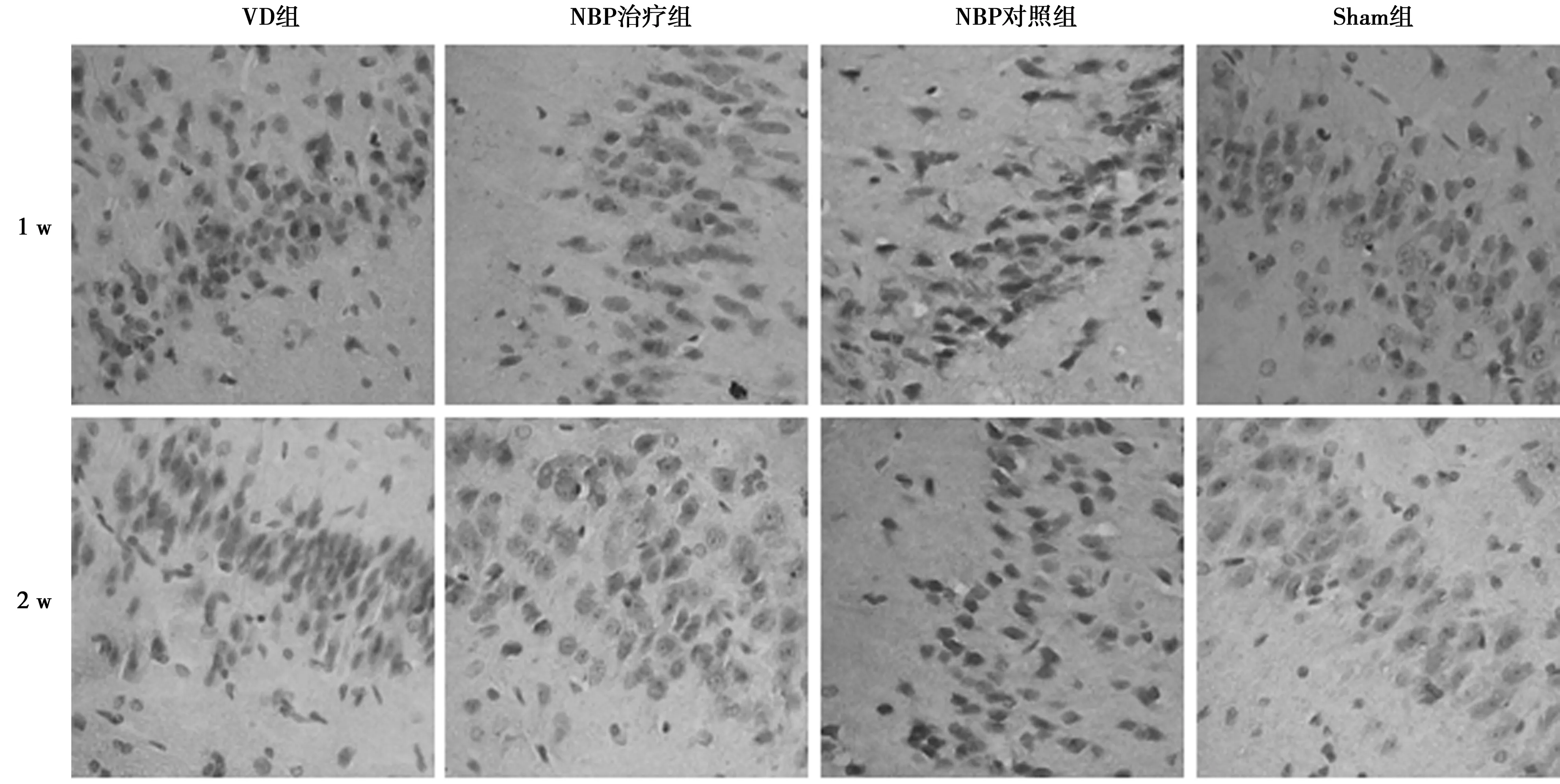
图3 1 w、2 w Bcl-2蛋白在各组大鼠海马CA1区的表达(DAB,×400)

图4 4 w、8 w Bcl-2蛋白在各组大鼠海马CA1区的表达(DAB,×400)
各时间点,NBP对照组大鼠海马CA1 区Bcl-2表达灰度均明显高于Sham组(P<0.05);2 w、4 w和8 w时NBP对照组大鼠海马CA1 区Bcl-2表达灰度均明显高于VD组(P<0.05);8 w时NBP治疗组大鼠海马CA1 区Bcl-2表达灰度明显高于VD组(P<0.05)。各组大鼠海马CA1 区Bcl-2表达灰度在不同时间点比较均无统计学差异(P>0.05)。见表2。

表2 各组大鼠海马CA1区Bcl-2表达灰度比较
3 讨 论
永久性双侧颈总动脉结扎法制备VD大鼠模型是目前公认的VD造模方法,大鼠脑血管系统与人类一样,具有发达的脑动脉环(Willis环),当双侧颈总动脉结扎后,并不会造成前脑组织的血供完全阻断,而是处于缺血状态〔7〕,接近VD慢性脑灌注不足的发病机制。海马、额叶等脑区的缺血性损伤是发生VD的基础。
研究发现,濒死状态的神经元中Bax呈高度表达〔8〕,Bax过度表达可以拮抗Bcl-2抑制凋亡作用,促进凋亡的发生。实验研究发现,前脑缺血可以导致海马CA1区诱导凋亡的Bax蛋白表达增加,Bax蛋白表达高峰先于DNA碎裂高峰,因而认为,Bax蛋白过度表达引起了海马CA1区神经元DNA断裂和凋亡〔9〕。本实验发现,NBP能够对前脑缺血导致的海马CA1区Bax蛋白过度表达起到抑制作用。
Bcl-2与Bax具有高度同源的氨基酸序列,其抗凋亡作用受到Bax的拮抗,Bcl-2/Bax的比值对神经细胞凋亡起着关键的作用〔10〕。Bcl-2在线粒体水平对抗各种凋亡刺激,对细胞起保护作用,其抗凋亡机制包括抑制Ca2+超载、抑制氧自由基、控制凋亡信号传导途径、抗谷氨酸毒性等多个方面〔11〕。Manji等〔12〕认为提高中枢神经系统Bcl-2的表达水平,能够提高神经元承受损伤的能力,还可以促进神经轴突的再生。本研究发现,NBP对照组大鼠海马CA1区Bcl-2表达最强,VD组大鼠海马CA1区Bcl-2蛋白表达有下降趋势,但未发现有统计学意义。8 w时,NBP治疗组大鼠海马CA1区Bcl-2表达显著增加,提示NBP可以提高大鼠海马CA1区Bcl-2蛋白的表达水平。本实验在制备VD大鼠的基础上,应用NBP给予干预治疗,观察不同时间点大鼠海马CA1区凋亡调控基因Bcl-2家族中促凋亡的Bax和抗凋亡的Bcl-2表达情况。结果发现:VD大鼠海马CA1区促凋亡蛋白Bax过度表达,抗凋亡蛋白Bcl-2的表达有减弱趋势;NBP对VD大鼠海马CA1区细胞凋亡具有明显的保护作用,可以抑制缺血损伤导致的海马CA1区Bax蛋白过度表达,同时能够提高大鼠海马CA1区Bcl-2蛋白的表达水平,抑制细胞凋亡,促进细胞存活,发挥神经保护作用。
1朱以诚,崔丽英,高 山,等.丁苯酞注射剂治疗急性脑梗死的多中心、随机、双盲双模拟、对照Ⅲ期临床试验〔J〕.中华神经科杂志,2014;(2):113-8.
2程文姚,杨 健,余新沛.丁苯酞软胶囊与尼莫地平对卒中后血管性痴呆患者的疗效〔J〕.解放军预防医学杂志,2016;34(4):516-8.
3赵万红,罗 超,龚应霞,等.消旋丁苯酞对慢性脑缺血大鼠认知功能的影响及其生化机制研究〔J〕.中华老年医学杂志,2014;33(4):412-5.
4Sun ZK,Ma XR,Jia YJ,etal.Effects of resveratrol on apoptosis in a rat model of vascular dementia〔J〕.Exp Ther Med,2014;7(4):843-8.
5Yang S,Zhou GG,Liu H,etal.Protective effects of p38 MAPK inhibitor SB202190 against hippocampal apoptosis and spatial learning and memory deficits in a rat model of vascular dementia〔J〕.Biomed Res Int,2013;2013:215798.
6Lock RB,Murphy KM.Immunodetecing members of the Bcl-2 family of proteins 〔J〕.Methods Mol Med,2005;111(1):83-96.
7Li Y,Zhang ZX.Gastrodin improves cognitive dysfunction and decreases oxidative stress in vascular dementia rats induced by chronic ischemia〔J〕.Int J Clin Exp Pathol,2015;8(11):14099-109.
8Prakasa Babu P,Yoshida Y,Su M,etal.Immunohistochemical expression of Bcl-2,Bax and cytochrome C following focal cerebral ischemia and effect of hypothermia in rat〔J〕.Neurosci Lett,2000;291(3):196-200.
9Kaneda K,Kashii S,Kurosawa T,etal.Apoptotic DNA fragmentation and upregulation of Bax induced by transient ischemia of the retina〔J〕.Brain Res,1999;815(1):11-20.
10Lindqvist LM,Vaux DL.BCL2 and related prosurvival proteins require BAK1 and BAX to affect autophagy〔J〕.Autophagy,2014;10(8):1474-5.
11Wang QQ,Zhang LL,Yuan XD,etal.The relationship between the Bcl-2/Bax proteins and the mitochondria-mediated apoptosis pathway in the differentiation of adipose-derived stromal cells into neurons〔J〕.PLoS One,2016;11(10):e0163327.
12Manji HK,Moore GJ,Chen G.Lithium upregulates the cytoprotective Bcl-2 in the CNS in vivo:a role for neurotrophic and neuroprotective effects in manic depressive illness〔J〕.J Clin Psychiatry,2000;61(9):82-96.

