回阳生肌膏对人来源微血管内皮细胞的干预作用
周敏 贾湘隆 徐旭英
糖尿病足溃疡(diabetic foot ulcer,DFU)是糖尿病微血管并发症中最常见最严重的一种,多发生在糖尿病血管损伤致组织缺血、坏死、感染之后,发病后未及时规范治疗往往会使病情进行性加重[1],致残致畸率极高,截肢(趾)术后5年病死率甚至高达50%~68%[2]。促进创面愈合是目前糖尿病足溃疡临床治疗与科学研究的重要着眼点,但现有的治疗方案往往起效慢且疗效不佳,急需安全有效的治疗手段促进创面愈合。创面修复的首要基础是血管新生带来的有效血氧供应,微血管内皮细胞通过多种方式参与血管新生及创面修复,改善糖尿病足溃疡微血管内皮细胞功能有助于治疗糖尿病足溃疡。回阳生肌膏是首都医科大学附属北京中医医院的一种外用制剂,在临床应用了数十年,已有研究对其促血管新生、促创面愈合的安全性及有效性进行了验证[3],本研究对2018年12月至2019年6月间北京中医医院疮疡血管外科住院部的大腿截肢患者进行了标本采集,按课题组前期研究报道的人来源原代微血管内皮细胞的分离培养[4],通过进行细胞学体外实验,探讨回阳生肌膏对人来源微血管内皮细胞的影响,以期进一步明确回阳生肌膏促进微血管新生、促创面愈合的机制。
1 材料与方法
1.1 标本来源
实验标本均来自北京中医医院疮疡血管外科住院部2018年12月至2019年6月行大腿截肢患者,取大腿截肢后创面周围皮肤和截除大腿近心端皮肤的真皮层。本实验符合中华人民共和国国务院颁发的《医疗机构管理条例》,经过医院伦理委员会论证并同意通过,标本采集前充分告知患者实验方案并签署知情同意书。
1.2 药物
回阳生肌膏由首都医科大学附属北京中医医院疮疡血管外科提供,由肉桂、炮姜、人参、黄芪、当归、白芥子、白蔹等药物与凡士林调匀制成。龙珠软膏由武汉马应龙药业集团股份有限公司提供,批号:110301。
1.3 人来源微血管内皮细胞分离与培养
采集标本后立即放入含双抗的DMEM培养基中,分离原代微血管内皮细胞:PBS冲洗组织3次,于DMEM培养基中将组织修剪成 1 mm3大小,转移至预湿培养皿,37℃、5% CO2细胞培养箱内静置2小时,加入含20%胎牛血清(fetal bovine serum,FBS)的DMEM培养基继续培养60小时,去除组织块并更换培养基,纯化细胞:滴3滴胰酶,10秒后吸弃旧培养基,加新培养基,每日1次换液,待细胞铺满单层后冻存或用于后续实验。原代微血管内皮细胞培养:细胞生长培养基由 90%1640培养基、5%内皮细胞生长添加物(endothelial cell growth supplement,ECGS)、5%FBS配制,于37℃、5%CO2恒温培养箱内培养。
1.4 实验试剂与仪器
1640培养基(GIBCO,11875-085),FBS(GIBCO,12664-025),ECGS(ScienCell,1052),RIPA总蛋白提取试剂盒(Sigma,R0278),PMSF(Sigma,PMSF-RO),蛋白酶抑制剂(Roche,11697498001),BCA蛋白定量试剂盒(Sigma, BCA1)等;IgG抗体(H+L)、HRP(Jackson,111035003),GAPDH抗体(天津锐尔康生物科技有限公司, REK0005),MTT Cell Viability Assay(Thermo, V13154),VEGFR2抗体(CST, 2479)。流式细胞仪(美国BD公司,Callibur II型),倒置荧光显微镜(Nikon,T1000),酶标仪(Therno scientific MultiSkan3),电泳仪(Therno scientific Mini,Ge Tank),转膜仪(Therno scientific,Mini Blot Module)。
1.5 实验分组及干预方法
实验细胞均为原代或1~3代,共分为4组:将截除肢体的近心端皮肤标本所得微血管内皮细胞分为空白组,创面周围皮肤标本所得微血管内皮细胞分别分为模型组、回阳生肌膏组、龙珠软膏组。空白组、模型组均不予干预,回阳生肌膏组与龙珠软膏组分别予最大无毒浓度Cmax1、Cmax2药物,作用时间均为48小时。
1.6 MTT法筛选药物最大无毒浓度
取空白组细胞,胰酶消化后制备为单细胞悬液,按细胞数1×104个、体积100 μL,接种于96孔板,共11个组,每组6个副孔,细胞贴壁后,吸弃旧培养基,随机10个组分别加入1640培养基配制的不同浓度(200 μg/mL、100 μg/mL、50 μg/mL、25 μg/mL、12.5 μg/mL)回阳生肌膏、龙珠软膏100 μL,对照组仅加100 μL 1640培养基,作用48小时后加MTT溶液,置于37℃培养箱4小时;吸弃溶液,10% SDS溶解细胞,570 nm下读吸光值,按公式:细胞抑制率=[对照组光密度(optical density,OD)值-实验组OD值]/对照组OD值×100%,计算细胞抑制率。运用GraphPad Prism 6.0计算出回阳生肌膏、龙珠软膏作用于人来源微血管内皮细胞48小时的最大无毒浓度,即Cmax1、Cmax2。
1.7 流式细胞术检测细胞凋亡
各组细胞按实验设计分组处理48小时后,以胰酶消化,各组分别制备100 μL密度为1×106个/mL的单细胞悬液,每组加10 μL Annexin V-FITC、5 μL PI,室温避光反应30分钟后加400 μL PBS重悬细胞,上流式细胞仪检测,收取细胞15000个/样,不足15000个收取全部细胞;应用CellQuest软件分析各组的细胞凋亡率。
1.8 ELISA检测相关因子
取对数生长期细胞,各组细胞根据实验分组分别处理48小时,按试剂盒操作说明书进行样本提取,细胞上清样品未做稀释,检测各组细胞基质金属蛋白酶1(matrix metallopeptidase 1,MMP1)、MMP9、基质金属蛋白酶抑制剂1(tissue inhibitors of matrix metalloproteinase 1,TIMP1)、基质金属蛋白酶抑制剂2(TIMP2)、血管内皮生长因子(vascular endothelial growth factor,VEGF)的表达量。
1.9 细胞迁移实验检测迁移能力
在24孔中放置Transwell小室,根据实验设计分组,上室加入对应分组的微血管内皮细胞,下室加入培养基及对应分组药物,培养48小时后,PBS洗2次,加细胞固定剂500 μL/孔,置于室温20分钟;PBS洗涤2次,加0.4%的结晶紫500 μL/孔,室温染色10分钟;PBS洗涤10次,显微镜拍照同时对各组细胞的迁移细胞计数。
1.10 Western blot 法检测相关蛋白表达
提取六孔板内细胞总蛋白,BCA法行蛋白定量,待检测蛋白样品上样量为13 μg/孔,加入浓缩胶配 SDS-PAGE 胶,电泳:选择MOPS缓冲体系,恒压90 V,约20分钟后恒压120 V;转膜,封闭,5%脱脂奶粉-TBS室温轻摇膜30分钟,分别加入VEGFR2抗体(1∶1000稀释)和GAPDH抗体(1∶10000稀释),室温孵育一抗10分钟,4℃过夜。洗膜,室温下孵育二抗40分钟,洗膜后ECL法显影曝光。应用Image J软件分析WB检测各条带的灰度值,并按公式计算各组细胞的血管内皮细胞生长因子受体2(vascular endothelial growth factor receptor 2,VEGFR2)蛋白相对表达量。
1.11 统计学处理

2 结果
2.1 药物无毒浓度筛选结果
回阳生肌膏浓度为12.5 μg/mL、25 μg/mL、50 μg/mL、龙珠软膏浓度为12.5 μg/mL均能在一定程度上促进人来源内皮细胞增殖。考虑到微血管内皮细胞均取自糖尿病足溃疡截肢患者,对应的高糖、缺血等病理状态使空白组细胞的功能已有一定下降,因此选择抑制率<10%情况下的最大浓度为后续试验浓度为回阳生肌膏50 μg/mL、龙珠软膏25 μg/mL,结果见表1。
2.2 回阳生肌膏对人糖尿病足创面内皮细胞抑制凋亡水平的影响
与空白组相比,模型组的总凋亡率显著增高(P<0.05);与模型组相比,回阳生肌膏组的总凋亡率降低(P<0.05),龙珠软膏组的总凋亡率也明显降低(P<0.05);回阳生肌膏组的凋亡率与龙珠软膏组相比没有统计学差异。结果见表2、图1。
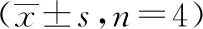
表1 药物无毒浓度筛选结果
注:与空白组比较,aP<0.05。
2.3 回阳生肌膏对人来源微血管内皮细胞中MMP1、MMP9、TIMPI、TIMP2及VEGF表达的影响
与空白组比较,模型组MMP1、TIMP1含量均明显增高(P<0.05),MMP9含量显著增高(P<0.05),TIMP2含量明显降低(P<0.05),VEGF含量显著降低(P<0.05)。与模型组相比,回阳生肌膏组与龙珠软膏组的MMP9含量均明显降低(P<0.05)、VEGF含量均明显升高(P<0.05),回阳生肌膏组的TIMP1水平出现降低(P<0.05),龙珠软膏组有降低趋势,回阳生肌膏组与龙珠软膏组的MMP1、TIMP2也有降低趋势。结果见表3。
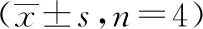
表2 各组人来源微血管内皮细胞凋亡水平比较
注: 与模型组比较,aP<0.05。
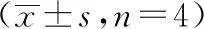
表3 各组人来源微血管内皮细胞基质金属蛋白酶类、抑制剂类及VEGF含量水平比较
注: 与模型组比较,aP<0.05。

注:A空白组;B模型组;C回阳生肌膏组;D龙珠软膏组。
图1 各组人来源微血管内皮细胞流式凋亡图
2.4 回阳生肌膏对人来源微血管内皮细胞迁移能力的影响
与空白组相比,模型组迁移细胞数显著降低(P<0.05);与模型组相比,回阳生肌膏处理后迁移细胞数增多(P<0.05);经龙珠软膏处理后迁移细胞数明显增多(P<0.05);回阳生肌膏组的细胞迁移数与龙珠软膏组相比没有统计学差异(P>0.05)。结果见表4、图2。

表4 各组人来源微血管内皮细胞迁移能力情况
注: 与模型组比较,aP<0.05。
2.5 回阳生肌膏对人糖尿病足创面内皮细胞中VEGFR2蛋白表达的影响
与空白组相比,模型组VEGFR2蛋白相对表达量呈现显著降低(P<0.05);与模型组相比,回阳生肌膏组、龙珠软膏组VEGFR2蛋白相对表达量均增高(P<0.05),而回阳生肌膏组的VEGFR2水平与龙珠软膏组相比没有统计学差异(P>0.05)。结果见表5、图3。
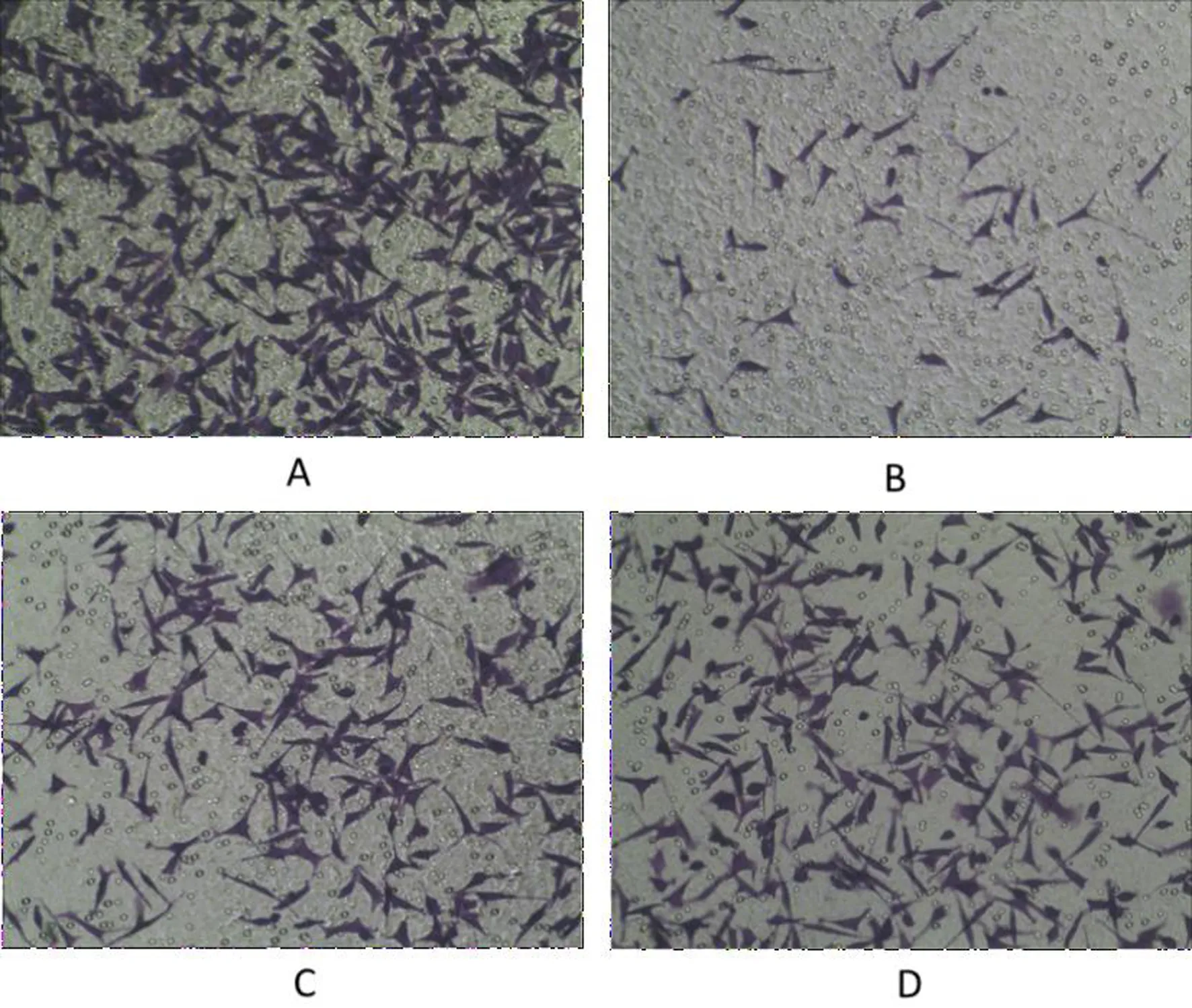
注:A空白组;B模型组;C回阳生肌膏组;D龙珠软膏组。
图2 各组人来源微血管内皮细胞迁移情况(×200)
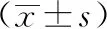
表5 各组人来源微血管内皮细胞VEGFR2 蛋白的相对表达量
注: 与模型组比较,aP<0.05。
注:A空白组;B模型组;C回阳生肌膏组;D龙珠软膏组。
图3 Western blot测定各组人来源微血管细胞VEGFR2蛋白的表达
3 讨论
截至2015年全球约4.15亿成人罹患糖尿病,带来的卫生支出总额约为6730亿美元[5],其中约有19%~34%的糖尿病患者在有生之年可能患糖尿病足溃疡[5-6],其中占大多数的慢性难愈性疮面也被称为慢性糖尿病足溃疡,与中医糖尿病足溃疡阴证创面十分相似:病变部位深(多在血脉、筋骨),创面脓质稀薄,肉芽苍白或紫黯,创周皮色苍白、紫黯[7],往往迁延难愈。根据2017年的《中国糖尿病足诊治指南》指出目前的治疗方向主要是在内科治疗基础上促进创面愈合,常用手段主要是外科手术清创,也有自溶、化学、机械及生物等清创方法,除此之外还有自体皮肤移植、敷料、血管重建、生长因子、干细胞、基因等[8]治疗方法。上述手段虽能在一定程度上延缓疾病进展,但往往速度缓慢、创面愈合效果不佳。在创面愈合中,血管新生带来的有效血氧供应、营养物质与细胞因子的输送是基础保障[9],微血管内皮细胞在目前已知血管新生的两种实现方式中均扮演了不可或缺的角色,主要通过增殖迁移成管及合成分泌MMPs参与血管新生。创面早期MMPs 能降解血管基底膜,增加血管通透性帮助微血管内皮细胞迁移增殖成管以及发芽形成新生血管网[10],但MMP1、MMP9的过度表达往往导致高蛋白水解并激发过度炎症反应,限制细胞迁移增殖、阻碍上皮化,导致创面难以愈合[11]。TIMP类是MMP类的天然内源抑制剂,可由内皮细胞合成,与MMP特异性结合能不可逆地抑制MMP活性改善过度水解,但有研究发现过高的TIMP1会诱导细胞凋亡,过高的TIMP2会抑制内皮细胞迁移[12],MMPs、TIMPs的过高表达均不利于血管新生和创面愈合。前面提到的MMPs在降解过程中还能通过刺激细胞因子的分泌参与血管新生,其中就主要包括生长因子VEGF[13],VEGFR2与VEGF的结合激活可刺激血管内皮细胞增殖、迁移,增强血管通透性,除此之外还可影响下游PIK3/Akt通路促进血管新生[14],这与课题组发现的回阳生肌膏能影响PIK3/Akt通路实现促血管新生的实验结果相吻合[15],VEGF/VEGFR2通路在诱导血管新生中也起着重要作用。
本研究发现回阳生肌膏与龙珠软膏均能抑制人来源微血管内皮细胞在糖尿病足溃疡状态下的MMP9过度表达,对MMP1、TIMP2的表达也有下调趋势,但回阳生肌膏对TIMP1含量的下调作用是龙珠软膏所没有的,除此之外,两种药物均能增加VEGF、VEGFR2的表达,龙珠软膏据报道在治疗糖尿病足溃疡中具有促创面愈合,减轻局部疼痛的效果[16],结合本科室临床治疗糖尿病足溃疡阴证创面的疗效,回阳生肌膏在促进糖尿病足溃疡阴证创面愈合方面的疗效可能高于龙珠软膏。首都医科大学附属北京中医医院疮疡血管外科的回阳生肌膏在业内享有盛誉,具有促新生血管生成、促创面愈合作用[17],由肉桂、炮姜、人参、鹿茸、白芥子、艾叶、黄芪、当归、赤芍等药物组成,其中黄芪性甘微温,善益气健脾,温分肉,肥腠理,为外科家之圣药,现代研究发现黄芪甲苷能提升血管内皮细胞活力[18],另一方面还能通过PI3K/AKT通路保护内皮细胞[19],人参所含人参皂苷能上调VEGFA、VEGFR2[20],人参、黄芪共奏益气之效;肉桂辛甘大热,补火助阳,活血通经,能够引导阳气宣通血脉,肉桂中的肉桂醛的抗氧化作用能保护血管内皮细胞[21],对体外成纤维细胞MMP1的过度表达也有下调作用,而鹿茸能上调VEGF表达[22],肉桂、鹿茸与炮姜、艾叶有温阳散寒之功,配伍当归、赤芍养血活血,赤芍中赤芍总苷能降低MMP9、TIMP1表达[23-24],以上诸药配伍能“温阳益气,活血生肌”,使回阳生肌膏能通过调控MMPs与TIMPs、VEGF与VEGFR2表达,改善糖尿病足溃疡阴证创面状态下的微血管内皮细胞增殖、迁移功能,促进血管新生,实现创面愈合。
糖尿病足溃疡阴证创面原本多“虚”多“瘀”,机体多脾肾阳虚、阴血不足,使机体气化无能,表现为创面板结晦涩、肉芽紫黯苍白、脓液稀薄,创面难以愈合,此类无血管新生、肉芽组织难以生长的创面应用回阳生肌膏后,脓液先由稀薄逐渐增多黄稠,而后再逐渐减少但仍淡黄,肉芽逐渐鲜明红活,创周、创底逐渐向愈敛和,这一现象与本实验发现的回阳生肌膏在体外对人来源微血管内皮细胞的影响有关,其机制可能是回阳生肌膏抑制了MMPs的过度表达改善了过度水解,对TIMP1的下调抑制了细胞凋亡,对TIMP2的下调增强了细胞迁移,从而促进血管新生实现了促创面愈合。另一方面,通过刺激VEGF/VEGFR2的表达,促进血管内皮细胞完成增殖迁移实现血管新生,并且影响PIK3/Akt通路改善氧化应激状态,也是回阳生肌膏促进创面愈合的机制之一。笔者猜想应用回阳生肌膏后,基质金属蛋白酶发挥的降解作用使坏死组织变得易于清除,创面脓液由原先的稀薄逐渐增多黄稠,实现“去腐”,为后续“生新”打下基础,为防止过度降解对TIMP1、TIMP2的表达进行了调控以抑制MMP1、MMP9的活性,或许这是脓液增多后再逐渐减少的原因;而当MMP/TIMP的比值到达相对平稳时,继续应用回阳生肌膏使MMP、TIMP的表达均有所下调,从而保证了血管内皮细胞的增殖与迁移;回阳生肌膏上调VEGF、VEGFR2的表达,脓液由原先的稀薄逐渐变为黄稠,血管内皮细胞迁移增殖促使血管新生网络形成,提供的血氧及营养物质使肉芽红活,创面愈合,这一“回阳以生肌,祛瘀以生新”过程正是回阳生肌膏理论依据“阳生阴长”的体现。
但在临床实际中创面愈合始终处于一个动态的过程,本实验中人来源微血管内皮细胞的标本采集与分离培养非常不易,数量有限,且试验均采用原代或1~3代细胞,仅对回阳生肌膏体外干预人来源微血管内皮细胞48小时进行了检测,若后期条件充分,考虑进行多时间点的检测对比,结合临床试验,以期更全面地探究回阳生肌膏是如何动态地影响微血管内皮细胞来促进血管新生、创面愈合。

