R+DA-EPOCH方案治疗弥漫大B细胞淋巴瘤的疗效
胡茂贵 丁凯阳 宋浩 吴国林 王馨辰
弥漫大B细胞淋巴瘤(diffuse large B cell lymphoma,DLBCL)是非霍奇金淋巴瘤(non-Hodgkin lymphoma,NHL)中发病率最高的1种亚型[1],R-CHOP方案一直被认为是所谓“标准”的治疗方案[2]。但近年来,随着研究的深入发现,约有50%甚至更多的DLBCL患者无法通过R-CHOP方案的治疗达到疾病的长期控制[3];而对于双重表达及双重打击亚型的DLBCL患者,其治疗效果更差,长期生存率低于20%~40%[4]。因此,如何提高高危组患者的治疗效果成为改善疾病整体预后的关键。目前,DA-EPOCH方案采用长时间、低浓度的方式作用于肿瘤细胞,杀伤作用更强,联合利妥昔单抗可诱导CD20阳性的肿瘤细胞加速凋亡,提高患者的反应率,已逐渐成为DLBCL的一线治疗方案[5]。本研究旨在评估R+DA-EPOCH方案治疗DLBCL患者的有效性与安全性,分析临床疗效的影响因素、无进展生存(progression free survival,PFS),为DLBCL个体化治疗提供思路,现报道如下。
1 资料与方法
1.1 一般资料 选择2015年5月至2018年1月安徽省肿瘤医院收治的30例初治DLBCL患者为研究对象,所有患者均通过组织病理学确诊。30例患者中,男性12例,女性18例;年龄18~76岁,平均(50.77±16.50)岁;双重表达淋巴瘤(double-expression lymphoma,DPL)患者13例,非DPL患者17例;Hans分型:GCB型患者8例,非GCB型患者22例;Ann Arbor分期:Ⅰ~Ⅱ期患者7例,Ⅲ~Ⅳ期患者23例;淋巴结内患者18例,淋巴结外患者12例。
1.2 纳入与排除标准 纳入标准:根据WHO的DLBCL分类标准,组织病理学确诊为CD20阳性的初治DLBCL;美国东部肿瘤协作组评分:0~3分。排除标准:存在第二肿瘤原发病史;原发肿瘤病灶无法评估测量;治疗期间出现与病情变化无关的死亡事件。
1.3 方法 所有患者均按体表面积(m2)计算药物用量接受R+DA-EPOCH方案化疗。具体如下:利妥昔单抗(瑞士罗氏,注册证号S20150002)375 mg/m2,第1天静脉滴注;依托泊苷(齐鲁制药,国药准字H20143143)50 mg/m2,避光24 h持续静脉滴注,第2~5天长春新碱(辅仁熙德隆,国药准字H20068151)0.4 mg/m2,避光24 h持续静脉滴注,第2~5天多柔比星(山西晋德,国药准字H14023143)10 mg/m2,避光24 h持续静脉滴注;环磷酰胺(江苏恒瑞,国药准字H32020857)750 mg/m2,静脉滴注,第6天;泼尼松(山东新华,H37020647)60 mg/m2,口服,第2~6天。每21 d为1个周期,化疗期间监测2次血常规。若中性粒细胞最低值≥0.5×109/L,依托泊苷、多柔比星和环磷酰胺在上一疗程基础上提高20%,若1~2次检测发现中性粒细胞最低值<0.5×109/L,维持上一疗程方案剂量,若≥3次检测中性粒细胞最低值<0.5×109/L,依托泊苷、多柔比星和环磷酰胺剂量在上一疗程基础上减20%,若血小板最低值<25×109/L,不管中性粒细胞最低值多少,依托泊苷、多柔比星和环磷酰胺剂量在上一疗程基础上减20%。
1.4 疗效评价 在治疗前、治疗的第4、8周期完成时进行影像学评估,随访期每3个月进行1次疗效评价。根据2017淋巴瘤国际工作组疗效评价标准[6]分为:完全缓解(complete remission,CR)、部分缓解(partial remission,PR)、无变化(no changed,NC)和疾病进展(progression of disease,PD),CR、PR为治疗有效,NC、PD为治疗无效。
1.5 随访 随访截止时间为2019年3月16日,采用入院复诊及电话随访结合的方式。随访内容包括肝胆胰脾、腹腔、浅表淋巴结B超,颈、胸、腹、盆腔增强CT或全身PET-CT等影像学指标,30例患者失访率为零。 PFS时间定义为从开始治疗至复发/进展、任何原因死亡或随访终点的时间。
1.6 不良反应评价 按美国国立癌症研究所不良事件常用术语标准(NCI CTCAE 5.0版)对不良反应进行分级,实验室安全性评估包括血液学和血生化等常规检查和免疫学指标的检查。
1.7 统计学方法 应用SPSS 17.0软件对数据进行统计分析,计数资料以率表示,率的比较采用Fisher确切概率法,生存分析采用Kaplain-Meier法绘制生存曲线。以P<0.05为差异具有统计学意义。
2 结果
2.1 疗效评价 30例患者均接受至少4个周期R+DA-EPOCH方案化疗,中位化疗6.5个周期。4个周期后评估结果:CR 12例(40.00%),PR 13例(43.33%),NC 5例(16.67%)。8个周期后再次疗效评估结果:CR 14例(46.67%),PR 7例(23.33%),NC 5例(16.67%),PD 4例(13.33%),治疗有效21例(70.00%),治疗无效9例(30.00%)。
2.2 临床疗效的单因素分析 8个周期后分析临床因素对疗效的影响, 30例患者中,DPL患者治疗有效率为92.31%,非DPL患者治疗有效率52.94%,差异具有统计学意义(P<0.05)。见表1。
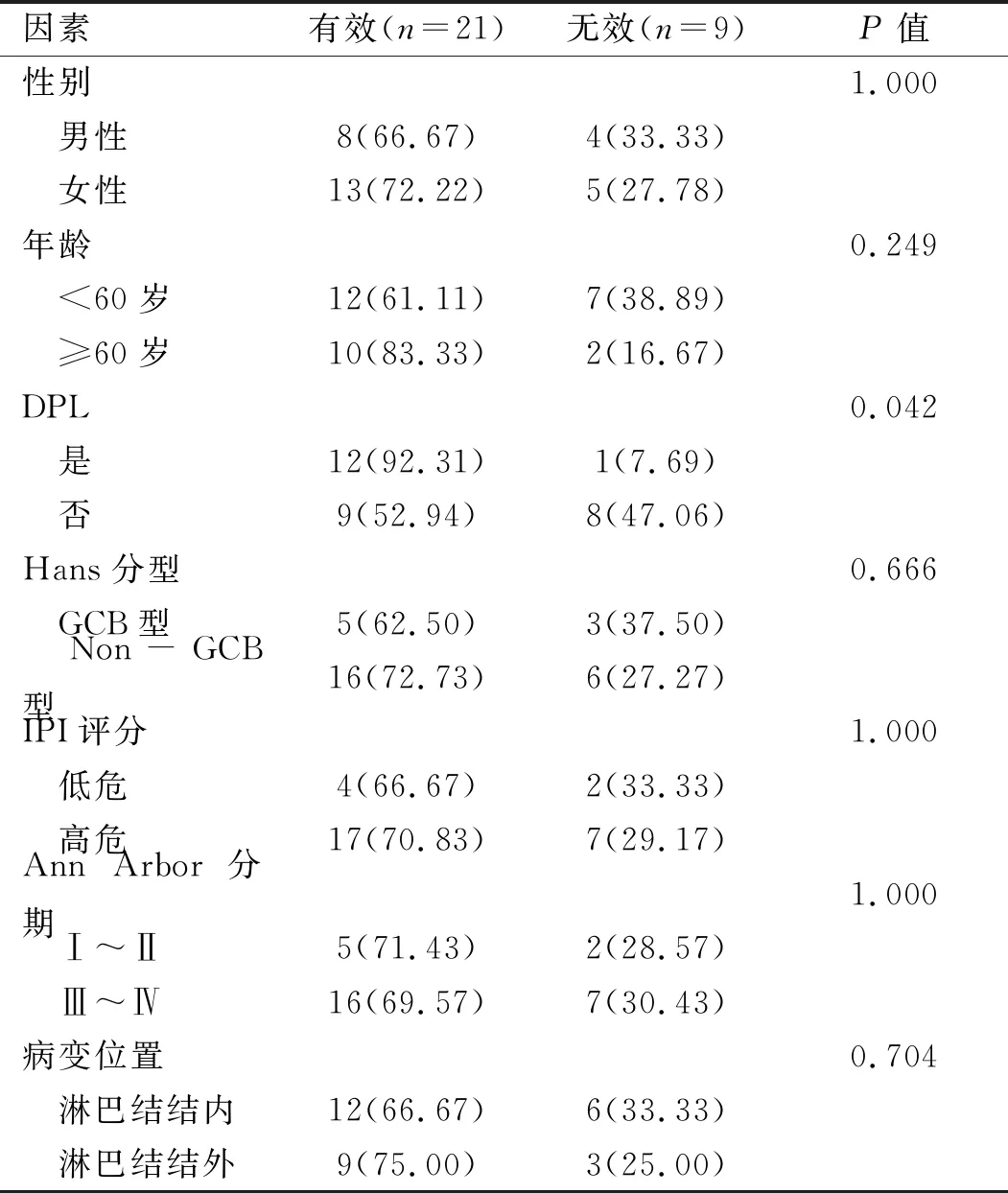
表1 DLBCL患者R+DA-EPOCH方案临床疗效的单因素分析[例(%)]
2.3 不良反应情况 30例患者中,2例出现Ⅳ度骨髓抑制,11例出现消化道症状,5例出现肝功能损害,无一例出现肾功能损害及严重心脏毒性反应,1例因患者高龄化疗后出现Ⅳ度骨髓抑制继发严重肺部感染而终止化疗。
2.4 生存时间分析 随访时间为13~45个月,中位随访28个月,截至随访终点,无死亡患者。30例患者的中位PFS时间未达到,24个月的PFS率为86.54%,至随访终点的PFS率为78.67%,见图1。
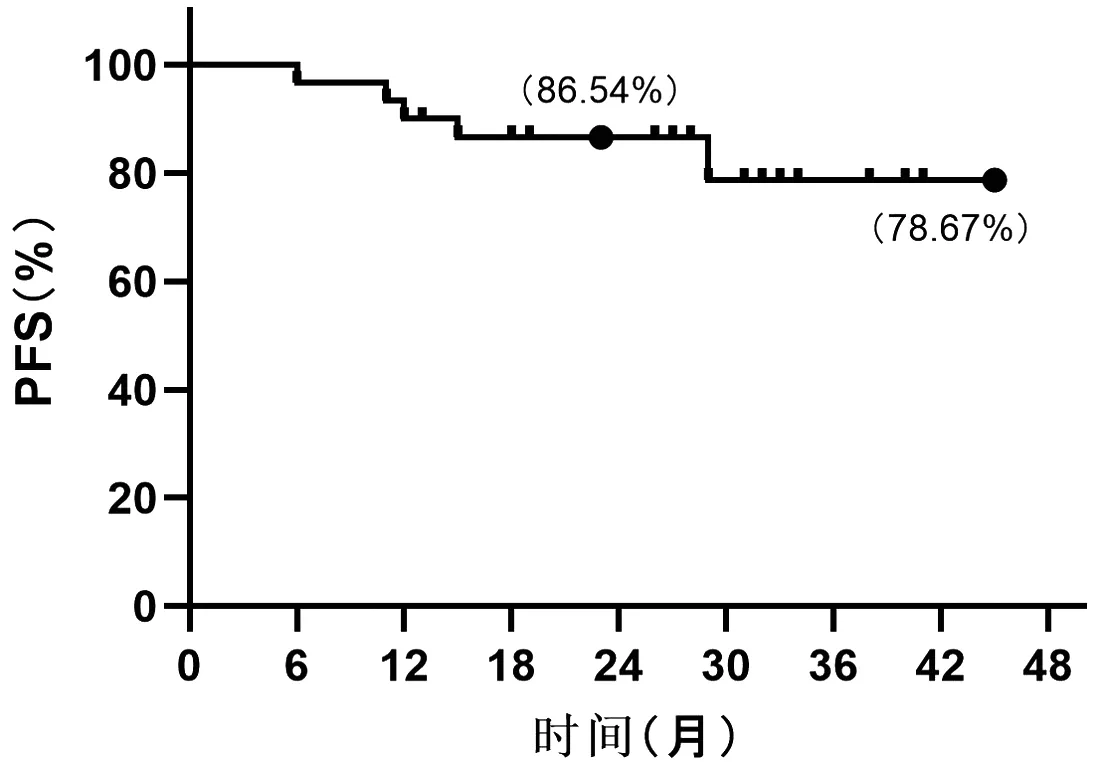
图1 R+DA-EPOCH治疗DLBCL患者的PFS
3 讨论
DLBCL是一种侵袭性极强的NHL,R-CHOP作为一线治疗方案显著改善了疾病治疗效果,但因该类疾病异质性极高,仍有50%左右患者面临复发/难治风险,预后差。如何选择个体化治疗方案进一步提高患者整体预后,成为目前疾病治疗的难点。
既往有研究[7-8]证实,DA-EPOCH方案可使70%的初治DLBCL患者无进展生存时间延长至62个月,总体生存率达到73%,明显优于传统的CHOP方案,联合利妥昔单抗后的R+DA-EPOCH方案效果更加明显,可使85%的患者获得12个月的无进展生存期。本研究结果显示,截至随访终点,30例患者24个月的PFS率为86.54%,至随访终点的PFS率为78.67%,良好改善了患者预后。
免疫组化双重表达(c-myc与Bcl-2/Bcl-6共表达)作为DLBCL独立高危因素,DPL患者预后明显差于普通DLBCL患者,更易进展为难治复发性淋巴瘤。刘薇等[9]在单中心临床研究中发现,DPL患者初治采用R+DA-EPOCH治疗,其CR率为74.1%、OS率为94.0%,有显著治疗效果。本研究结果显示,R+DA-EPOCH方案治疗的CR率为46.67%,总有效率为70.00%,单因素分析显示,治疗有效率与年龄、性别、病变位置、Hans分型、临床分期、IPI评分等参数无关,而DPL应用R+DA-EPOCH治疗有效率高于非DPL,差异有统计学意义(P<0.05),此结果与既往临床研究结果相似[10],表明R+DA-EPOCH在DPL的治疗中具有一定优势。
在不良反应方面,相对于R-CHOP方案,R+DA-EPOCH方案具有更强的毒性反应[11],但国外研究[12]发现大部分患者均可耐受R+DA-EPOCH方案的毒性反应。本研究结果显示,在R+DA-EPOCH方案治疗期间,Ⅳ度骨髓抑制发生率低,未出现严重心脏毒性事件,无继发第二肿瘤,肝肾功能受损轻微,患者耐受性良好。
综上所述,R+DA-EPOCH方案可改善DLBCL治疗效果,尤其对DPL患者的缓解率有明显提高,同时患者耐受性良好,安全性高,值得临床推广应用。但由于本研究样本量较少,临床研究深度不足,有关R+DA-EPOCH方案的远期疗效和安全性,还需大样本及分子遗传学研究的进一步探索。

