耳内镜下与显微镜下鼓膜修补术的临床应用对比*
林碧玉 李瑞玉 王一红
慢性化脓性中耳炎引起的鼓膜穿孔是传导性耳聋的重要原因[1]。鼓膜修补术是鼓膜穿孔的重要治疗方法,通过组织移植修复鼓膜穿孔部位,恢复鼓膜的完整性,提高听力[2]。采用显微镜下鼓膜修补术治疗鼓膜穿孔存在一定的不足,如手术视野窄、创伤性大、术后恢复慢[3]。耳内镜下鼓膜修补术由于手术视野清晰、探查部位广等优点得到临床医师的青睐[4]。本研究对70 例慢性化脓性中耳炎后遗症鼓膜穿孔患者进行研究,对比耳内镜下与显微镜下鼓膜修补术的临床应用效果及对纯音听阈、鼓膜愈合率的影响。现报道如下。
1 资料与方法
1.1 一般资料 选取2016 年1 月-2019 年8 月本院收治的70 例慢性化脓性中耳炎鼓膜穿孔患者进行研究。纳入标准:(1)鼓膜大小不等的边缘性或中央性穿孔;(2)上鼓室和听骨链无病变;(3)咽鼓管良好;(4)传导性耳聋。排除标准:(1)胆脂瘤型中耳炎;(2)全聋,无残余听力;(3)3 个月内有头颅外伤史;(4)伴有糖尿病和高血压。按随机数字表法将患者分为对照组和观察组,各35 例。患者均签署知情同意书,本研究经伦理委员会批准。
1.2 方法 观察组采用耳内镜下鼓膜修补术,全麻后对耳屏和外耳道皮肤浸润麻醉,在手术侧耳屏游离侧切开软骨,修整软骨膜,保持软骨膜宽度大于软骨1~2 mm,在软骨取一切口嵌顿于锤骨柄上缝合伤口。耳内镜观察鼓膜,在离鼓环5 cm 处作弧形切口,切开皮肤达骨质表面,剥离鼓膜创面暴露鼓环,采用内贴法植入软骨-软骨膜,碘仿纱布填充术腔,缝合切口后包扎伤口。对照组采用显微镜下鼓膜修补术,在耳道四壁和耳后浸润麻醉,耳廓上方作2 cm 切口,选取颞肌筋膜备用。分离外耳道骨片至颞线,前方显示外耳道上方,磨除外耳道前上棘,采用内贴法植入颞肌筋膜,鼓室周围填充明胶海绵,碘仿纱布填充术腔,缝合切口后包扎伤口。
1.3 观察指标及判定标准 比较两组的手术时间和住院时间、出血量、疼痛程度、切口美观度、纯音听阈和鼓膜愈合率。手术苏醒后按照NRS 评分对患者的疼痛情况进行评价:0 分无痛;1~3 分轻度疼痛;4~6 分中度疼痛;7~10 分为重度疼痛。了解患者对手术切口的美观满意程度。采用自行设计问卷调查患者对切口美观的满意度,满意:对美观效果满意,符合心愿;一般:不在意美观效果;不满意:对美观效果不满意。比较两组术后1、3 个月纯音听阈(气导听阈、气骨导差)的情况。术后1 周根据切口愈合情况拆线,术后3 周取出外耳道填塞物,术后1 个月、6 个月、1 年进行耳内镜检查,观察鼓膜愈合和再穿孔情况。
1.4 统计学处理 采用SPSS 20.0 软件对所得数据进行统计分析,计量资料用()表示,组间比较采用t 检验,组内比较采用配对t 检验;计数资料以率(%)表示,比较采用χ2检验;等级资料采用秩和检验。以P<0.05 为差异有统计学意义。
2 结果
2.1 两组一般资料比较 观察组35 例,男19 例,女16 例;年龄15~49 岁,平均(29.57±2.43)岁;鼓膜穿孔大小为(3.25±0.93)mm。对照组35 例,男20 例,女15 例;年龄19~46 岁,平均(29.49±2.31)岁;鼓膜穿孔大小为(3.19±0.96)mm。两组上述资料比较,差异均无统计学意义(P>0.05),具有可比性。
2.2 两组手术时间和住院时间、出血量比较 观察组手术时间和住院时间均短于对照组,出血量少于对照组,差异均有统计学意义(P<0.05),见表1。
表1 两组手术时间和住院时间、出血量比较()
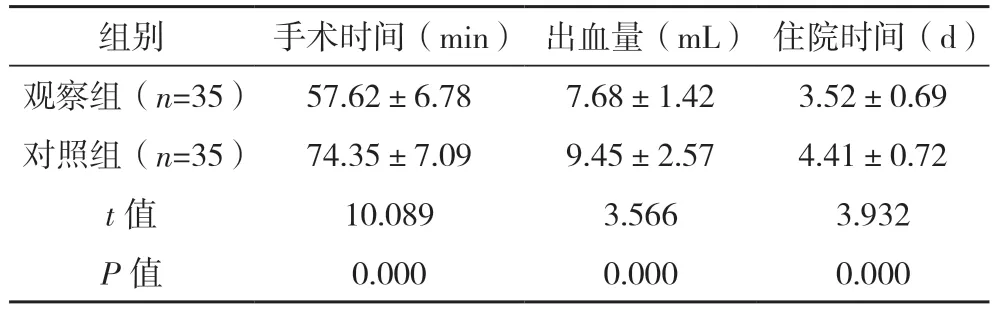
表1 两组手术时间和住院时间、出血量比较()
2.3 两组疼痛程度比较 观察组疼痛程度优于对照组,差异有统计学意义(Z=3.932,P=0.000),见表2。

表2 两组疼痛程度比较 例
2.4 两组切口美观满意度比较 观察组对切口美观满意度高于对照组(Z=2.782,P=0.006),见表3。

表3 两组切口美观满意度比较 例(%)
2.5 两组纯音听阈比较 术前,两组纯音听阈比较,差异无统计学意义(P>0.05);术后1、3 个月,两组气导听阈、气骨导差均下降,且观察组均低于对照组,差异均有统计学意义(P<0.05)。见表4。
2.6 两组鼓膜愈合率、再穿孔率比较 两组术后1 个月、6 个月、1 年鼓膜愈合率和再穿孔率比较,差异均无统计学意义(P>0.05),见表5。
表4 两组纯音听阈比较()
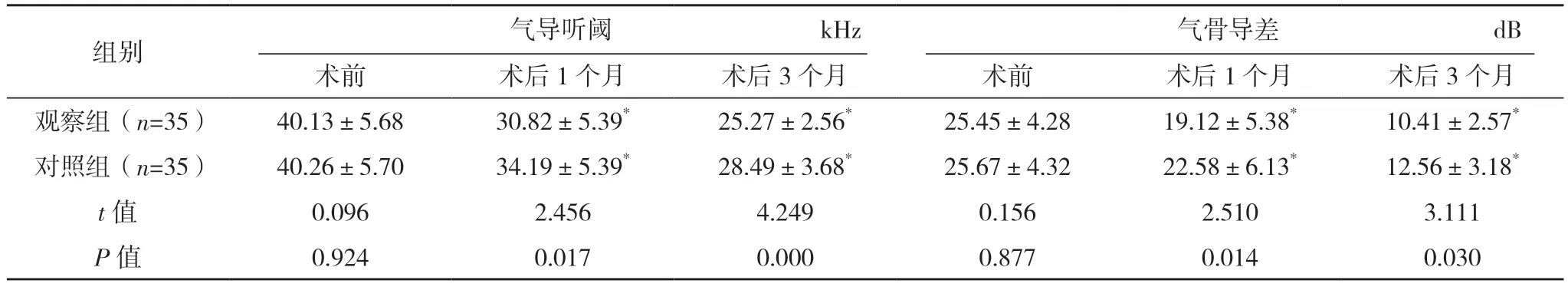
表4 两组纯音听阈比较()
*与术前比较,P<0.05。

表5 两组鼓膜愈合率、再穿孔率比较 例(%)
3 讨论
慢性化脓性中耳炎导致鼓膜穿孔最为常见,影响患者的生活质量,治疗目标为提高听力,预防再次感染。鼓膜穿孔表现为耳部疼痛、流液和听力下降。鼓膜穿孔愈合是穿孔边缘上皮层细胞和成纤维细胞增殖的结果[5]。移植物起到支撑作用,细胞分化和增殖上皮细胞沿着移植物周围向中心迁移,毛细血管长入移植物中完成愈合[6]。
本研究说明耳内镜下鼓膜修补术对鼓膜穿孔的综合效果优于显微镜下鼓膜修补术。显微镜下鼓膜修补术是成熟的手术[7]。显微镜光源不能覆盖所有穿孔的边缘,术中需要不断调节镜头方向窥见穿孔边缘,临床上外耳狭窄或鼓膜前下方穿孔的患者,显微镜下鼓膜修补较为困难,需要行耳内或耳后切开术扩大外耳道,增加了手术时间和出血量,增加患者的疼痛程度[8-9]。此外,单纯筋膜移植术后易萎缩,影响负压,粘连和塌陷的风险较高[10]。耳内镜下鼓膜修补术采用筒形骨瓣法置入软骨-软骨膜,与显微镜相比,优势在于耳内镜下光源明亮、术野清晰、视杆细长、多角度探查,越过狭窄和深入深腔,增加病变侧方和深面的视野,降低失误率,减小切口,减少对外观的影响,降低暴露术腔外侧的要求,避免术腔外侧组织去除,缩短手术时间,减少损伤组织,降低并发症的发生,缩短康复时间[11-13]。软骨-软骨膜是中胚层组织,软骨膜血管丰富,有助于新生血管生成,促进上皮细胞移行,软骨表面无血管,避免与鼓室粘连,胆脂瘤发生率低,弹性好,取材方便,切口小,易于放置,质柔韧,耐感染强,改善鼓室前径,降低移位风险[14-16]。不用留置明胶海绵,不易产生裂隙,抗感染能力强,有助于建立血运,存活率高[17-18]。耳内镜下鼓膜修补术存在一定的局限性,镜面易污染,术中应该用温水擦拭镜面,保持清洁;术野易扭曲,术者需要建立视觉反射后才能顺利操作;缺乏立体感,对术者要求高,术者需要掌握耳内镜技术和解剖结构,避免外耳道出血影响操作;单手操作影响手术进程,需要进行解剖训练,与助手磨合后弥补不足;耳内镜需要去除骨质器械、去除肉芽组织、处理深部病变。
综上,耳内镜下鼓膜修补术与显微镜下鼓膜修补术效果相当,但是耳内镜下鼓膜修补术手术时间和住院时间短、出血量少、疼痛程度轻、更加美观,可明显地提高纯音听阈,值得临床上广泛使用。

