胸腺肽a1联合恩替卡韦治疗抗乙型肝炎病毒患者对H3K9乙酰化修饰蛋白与Toll样受体9结合变化的研究
朱海鹏,杜 巍,曹焕焕,钟庆杨,殷思纯
(东莞市第九人民医院感染科,广东东莞 523000)
我国是肝病大国,据统计,全国慢性乙型肝炎病毒(HBV)感染者将近一亿,而其中尤以广东省的 HBV 感染率居高,且约20%患者可发展成重型肝脏疾病[1-2]。因此,探讨各种新型HBV 治疗方法及治疗分子机制一直是临床重要的研究方向。由于慢性乙型肝炎发病机制复杂,现阶段治疗方法也呈现出复杂与多样性,包括抗病毒治疗、调节免疫、抗炎和抗氧化、抗纤维化等[3]。近期多项胸腺肽a1(Ta1)联合恩替卡韦抗HBV临床研究显示,该治疗方案可以提高血清谷丙转氨酶(ALT)复常率、HBV病毒载量(HBV DNA)转阴率等重要指标,临床常见不良反应少而轻[4-6]。为此,Ta1联合恩替卡韦抗HBV治疗成为一个重要的临床治疗补充手段,针对其联合治疗的分子机制也成为一个重要课题。前期工作在研究Toll样受体10(TLR10)在HBV感染中的作用仅发现TLR9和TLR10的表达与HBV载量具有相关性[7]。有文献报道,组蛋白乙酰化修饰状态与多种病毒感染密切相关[8-9]。本课题组在比较慢性乙型肝炎不同疾病状态中外周血CD4+T 淋巴细胞中组蛋白H3K9 在全基因组启动子区域乙酰化修饰状态中发现,TLR9基因的2个序列区存在H3K9乙酰化修饰调控,提示TLR9的H3K9乙酰化修饰在慢性乙型肝炎发生发展中也发挥了重要的作用,现报道如下。
1 资料与方法
1.1 一般资料 选取2017年12月至2019年2月东莞市第九人民医院收治的3例慢性乙型肝炎患者为研究对象进行回顾性分析,患者中男性1例,女性2例;年龄18~65岁,平均年龄(36.50±4.50)岁。本研究经东莞市第九人民医院医学伦理委员会批准。纳入标准:①符合《慢性乙型肝炎防治指南(2015年更新版)》[10]中慢性乙型肝炎的诊断标准;②初次检测感染患者;③年龄18~65岁。排除标准:①HBV外其他病毒感染;②存在原发性肝细胞癌(HCC)或甲胎蛋白(AFP)≥400 ng/mL持续超过1个月;③因其他疾病需要免疫抑制治疗或放疗、化疗;④妊娠或哺乳期患者。
1.2 研究方法 染色质免疫共沉淀及TLR9基因H3K9乙酰化检测。先抽血收集临床样本,然后给予联合治疗,具体过程如下。抽取患者肘静脉血5 mL,置于500 μL肝素抗凝管中,于抽血后2 h内分离外周血单核细胞(PBMCs),采用抗凝管收集受试者血液样本。给予患者恩替卡韦(中美上海施贵宝制药有限公司,国药准字H20052237,规格:0.5 mg/片)口服治疗,0.5 mg/次,1次/d,治疗4周;注射用胸腺素a1(成都地奥制药集团,国药准字H20020545,规格:1.6 mg/瓶)行皮下注射,1.6 mg/次,2次/周,治疗4周。全部新鲜样本分离血液PBMCs,加入细胞裂解液,以3 000 r/min转速离心5 min涡旋离心取上清。试剂盒内MNase Digestions Buffer重 悬 沉 淀,Micrococcal Nuclease混匀水浴,MNase Stop Solution终止反应。蛋白质裂解液(Lysis Buffer)重悬沉淀,冰浴、涡旋、离心、收集上清。加入750 μL的DNA 结合缓冲液(Binding Buffer),加入到DNA Clean-Up柱,以3 000 r/min 转速离心5 min离心弃上清。将剩余的样品加入同一个DNA Clean-Up柱,加入750 μL DNA 柱清洗缓冲液(Column Wash Buffer),同法离心弃上清,再次离心。加入50 μL DNA 稀释溶液(Elution Solution),同法离心收集纯化DNA,进行实时荧光定量核酸扩增检测(qPCR)检测,引物信息见下文。qPCR的总反应体系为20 μL,反应体系,见表1;qPCR采用两步法扩增体系,反应条件如表1所示,循环数为50个循环,反应过程为95 ℃预变性10 min,95 ℃变性15 s,60 ℃延伸 1 min。

表1 qPCR反应的反应体系
血清白细胞液相色谱-质谱联用技术(LCMS/MS)检测组蛋白乙酰化。液相色谱-质谱联用技术:使用Thermo Fisher公司的血清高丰度蛋清去除试剂盒Pierce™ Top 12 Abundant Protein Depletion Spin Columns去除12种常见的高丰度蛋白。使用Thermo Fisher公司检测蛋白质浓度试剂盒Pierce™ BCA Protein Assay Kit给蛋白质定量。使用AB Sciex公司的iTRAQ 试剂-多标缓冲液试剂盒还原及封闭蛋白质。使用Sangon公司的Trypsin TPCK Treated酶解蛋白质。使用AB Sciex公司的iTRAQ多重试剂盒标记iTRAQ实验的蛋白质。iTRAQ实验的蛋白质经过标记后需要进行第一维高Ph-rp液相分离。iTRAQ实验和非标记蛋白组学技术(Label free)实验都进行RPLC-MS。肽段用样品溶解液(0.1%甲酸、5 %乙腈)溶解,充分振荡涡旋,13 500 r/min,4 ℃离心20 min,上清转移到上样管中,进行质谱鉴定;流动相A为0.1%甲酸+2%乙腈水溶液;流动相B为0.1%甲酸+98%乙腈水溶液;流速为600 m/s,每个组分分析时间90 min。采用Proteome Discoverer 2.2进行数据库检索,见表2。
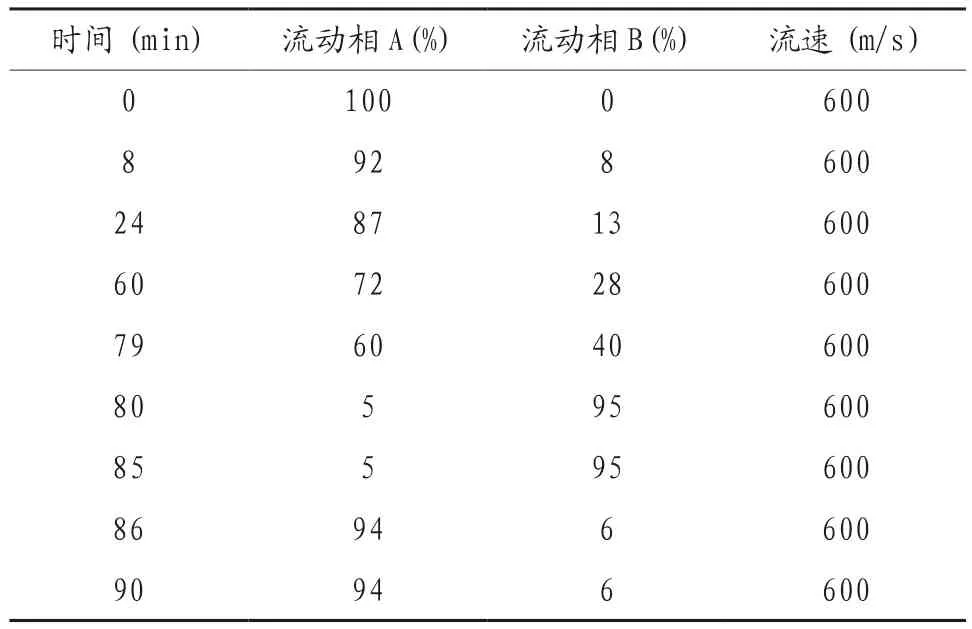
表2 LCMS/MS检测第二维液相梯度条件
采用Proteome Discoverer 2.2进行数据库检索。软件参数设定消化酶为Trypsin,数据库为uniprot-human-filtered-organism Homo sapiens (Human) 。iTRAQ实验数据需要设定静态修饰为8标iTRAQ试剂标记。鉴定的原始结果设置MS准确度10 mg/kg,MS / MS准确度0.02 Da,胰蛋白酶消化,允许两次错过切割,固定的半胱氨酸的氨基甲酰基甲基修饰和氧化甲硫氨酸的可变修饰。
HBV感染患者在入院第一天、恩替卡韦和胸腺肽a1联合用药治疗1个周期、恩替卡韦和胸腺肽a1联合用药治疗结束3个阶段中患者血清PBMCc中TLR9基因与蛋白H3K9Ac存在结合情况、组蛋白修饰水平。
1.3 观察指标 ①统计3例受试者的临床血清学指标信息。②分析Ta1联合恩替卡韦抗HBV治疗过程中TLR9基因的H3K9乙酰化修饰。
1.4 统计学分析 采用SPSS 20.0统计学软件分析数据。符合正态分布的计量资料以()表示,两组间比较采用t检验,多组比较采用单因素方差分析。以P<0.05为差异有统计学意义。
2 结果
2.1 3例受试者的临床血清学指标信息 本研究开始纳入了20例患者,因各种患者和疫情影响因素,最终全部治疗进程完成的患者只有3例。对纳入研究的3例受试者治疗不同时间段谷丙转氨酶(ALT)、总胆红素(TBIL)、凝血酶原活动度(PTA)、HBV病毒载量等实验室血清学信息进行了统计,见表3。
表3 3例受试者的临床血清学指标信息()
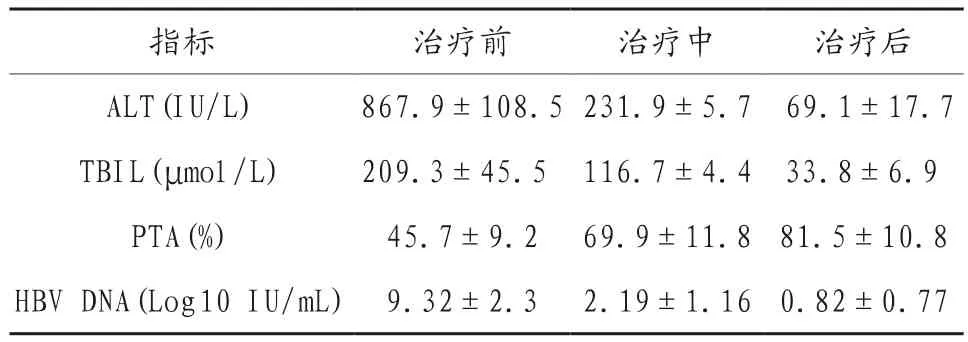
表3 3例受试者的临床血清学指标信息()
注:ALT:谷丙转氨酶;TBIL:总胆红素;PTA:凝血酶原活动度;HBV DNA:乙型肝炎病毒载量。
指标 治疗前 治疗中 治疗后ALT(IU/L) 867.9±108.5231.9±5.7 69.1±17.7 TBIL(μmol/L) 209.3±45.5 116.7±4.4 33.8±6.9 PTA(%) 45.7±9.2 69.9±11.881.5±10.8 HBV DNA(Log10 IU/mL) 9.32±2.3 2.19±1.160.82±0.77
2.2 Ta1联合恩替卡韦抗HBV治疗过程中TLR9基因的H3K9乙酰化修饰 通过ChIP实验探究了恩替卡韦和胸腺肽a1联合用药过程中患者血清PBMCs细胞中,蛋白H3K9Ac与TLR9 基因启动序列(promoter )区的结合情况。通过序列比对分析,TLR9基因与蛋白H3K9Ac预测的3个潜在结合位点,分别设计了对应的验证引物信息,见图1。

图1 免疫共沉淀ChiP技术实验检测不同人群血清PBMCc中TLR9基因与蛋白H3K9Ac结合情况
进一步研究测试了3例HBV感染患者在刚入院、恩替卡韦和胸腺肽a1联合用药治疗一个周期、恩替卡韦和胸腺肽a1联合用药治疗结束3个阶段中患者血清PBMCc中TLR9基因与蛋白H3K9Ac存在结合情况。结果很明显,3个结合位点在治疗过程中均有显著的改变,尤其是位点2,这说明恩替卡韦和胸腺肽a1联合用药临床增强免疫、抑制HBV病毒复制的过程中确实与TLR9基因与蛋白H3K9Ac有显著的关系。
通过DNA序列分析也发现H3K9Ac在其他细胞模型中具备同一区域修饰模型的变化,ChiP检测的PCR产物经过测序我们也找到了TLR9的部门基因序列,在治疗好转的过程中起序列匹配度更好。这一点与固定的DNA位点组蛋白修饰的改变进而诱导基因调控的模型是吻合的,见图2。
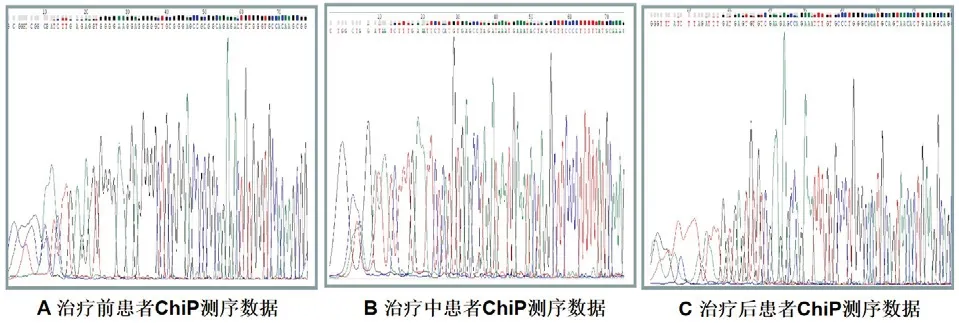
图2 治疗前中后患者免疫共沉淀PCR产物测序数据(同一组样本混合)
此外,本研究通过LCMS/MS技术也初步探讨了HBV感染患者在恩替卡韦和胸腺肽a1联合用药治疗过程中血清PBMc细胞组蛋白修饰的程度的变化。如图3所示,随着治疗进程的增加,可 在uniprot-human-filtered-organism Homo sapiens (Human)可检索到乙酰化修饰片段增多。这说明恩替卡韦和胸腺肽a1联合用药增加了组蛋白修饰水平,这可能会促使患者PBMc核内的TLR9相关的转录因子释放,增加其表达水平,改变患者免疫水平。
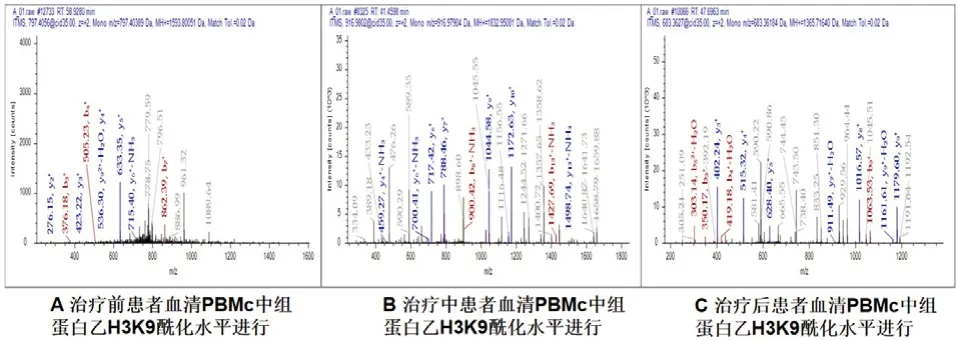
图3 治疗前中后期液质LCMS/MS技术检测患者血清PBMc中组蛋白乙H3K9酰化水平
3 讨论
本研究前期工作中,针对Tolls在HBV感染患者PBMCs上差异表达,发现慢性乙型肝炎患者血清中PBMCs TLR9 mRNA表达与血清HBV DNA载量具有显著相关性。考虑到慢性乙型肝炎患者外周血细胞中TLR9基因的2个序列区存在H3K9乙酰化修饰调控。随后进一步探究了3例慢性乙型肝炎患者恩替卡韦和胸腺肽a1联合用药治不同治疗进程过程中H3K9乙酰化蛋白与TLR9的结合情况。本研究结果显示,对纳入研究的3例受试者进行恩替卡韦和胸腺肽a1联合用药,具有显著的临床抗病毒效果,并且整个过程中肝功能具有明显提高。
本研究系统地考察了HBV感染患者在恩替卡韦和胸腺肽a1联合用药治疗过程中患者血清PBMc细胞中组蛋白修饰的变化、蛋白H3K9Ac与TLR9结合情况 ,结果显示,TLR9的H3K9乙酰化修饰在慢性乙型肝炎患者中存在并发挥了重要作用。在恩替卡韦和胸腺肽a1联合用药治疗的过程中,TLR9的组蛋白乙酰化修饰显著提高、H3K9乙酰化蛋白与TLR9结合位点变化显著,这可能会增加了TLR9在mRNA和蛋白水平的表达,进一步调节各种炎症因子、细胞因子的表达,进一步抑制病毒增殖、发挥抗病毒效果。研究结果证实了TLR9、H3K9乙酰化修饰等参与Ta1联合恩替卡韦抗HBV过程的免疫反应,为慢性乙型肝炎抗病毒的免疫控制理论提供了新依据,具有重要的临床应用意义。
综上,在恩替卡韦和Ta1联合用药治疗的过程中两者的结合可能会增加TLR9在mRNA和蛋白水平的表达,发挥其抗病毒作用。

