基于HPLC指纹图谱评价不同产地山楂叶质量
高静云,段丽颖,赵胜男,杜义龙,潘海峰
承德医学院河北省中药研究与开发重点实验室(河北 承德 067000)
山楂叶为蔷薇科山楂属植物山里红CrataeguspinnatifidaBge.Var.majorN.E.Br.或山楂CrataeguspinnatifidaBge.的干燥叶,具有理气通脉,活血化瘀,化浊降脂的功效[1-2]。其中黄酮类成分为主要活性成分[3-7]。此外,以山楂叶提取物为原料的益心酮胶囊、心安胶囊等制剂在临床上应用较广[8],可发挥降血脂、降血压、降糖,抗血栓、心肌缺血、心律不齐,以及抗炎等疗效[9-10]。现如今山楂叶在我国辽宁、山西、河北、山东等多地被种植,由于其嫁接技术不同、品种多样、气候不一,使得不同产区、不同品种的山楂叶质量参差不齐。2020年版《中国药典》一部中仅以山楂叶单一成分(金丝桃苷)和总黄酮含量为含量测定标准,以芦丁、金丝桃苷为鉴别标准,测定指标单一,无法控制山楂叶整体质量[1],不能满足对不同产地山楂叶质量进行客观评价的要求。近年来,指纹图谱结合化学模式识别的分析方法,从定性与定量方面在中药鉴别和质量控制方面得到广泛应用[11-16]。本文对4个不同产地的山楂叶进行指纹图谱研究以及多组分含量测定,并运用主成分分析、聚类分析等方法,对不同产地的山楂叶质量进行客观的评价,为其更好的开发利用提供科学依据。
1 仪器与试药
1.1仪器Agilent 1200高效液相色谱仪,美国安捷伦公司;JA5003上皿天平(千分之一),天津天马衡基仪器有限公司;AG225电子分析天平,瑞士梅特勒-托利多公司;KQ-700超声波清洗器,昆山市超声仪器有限公司;HC-2062高速离心机,科大创新股份有限公司中佳分公司;FW100高速万能粉碎机,天津市泰斯特仪器有限公司。
1.2试药对照品绿原酸(批号18071907)、牡荆素葡萄糖苷(批号20042305)、牡荆素鼠李糖苷(批号20042304)、牡荆素(批号18052906)、芦丁(批号181227)、金丝桃苷(批号19103001)、异槲皮素(批号18062702)均购自成都普菲得生物技术有限公司。乙腈、四氢呋喃均为色谱纯,购自美国Fisher Scientific公司,甲醇、甲酸为分析纯,纯净水(批号GB19298,广州屈臣氏食品饮料有限公司)。
2021年10、11月收集的22批山楂叶样品经全国老中医药专家(传统鉴定)学术经验继承人孙宝惠主任药师鉴定为山里红CrataeguspinnatifidaBge.var.MajorN.E.Br.的干燥叶。经检测22批山楂叶均符合2020年版《中国药典》一部山楂叶质量控制各项下要求,见表1。
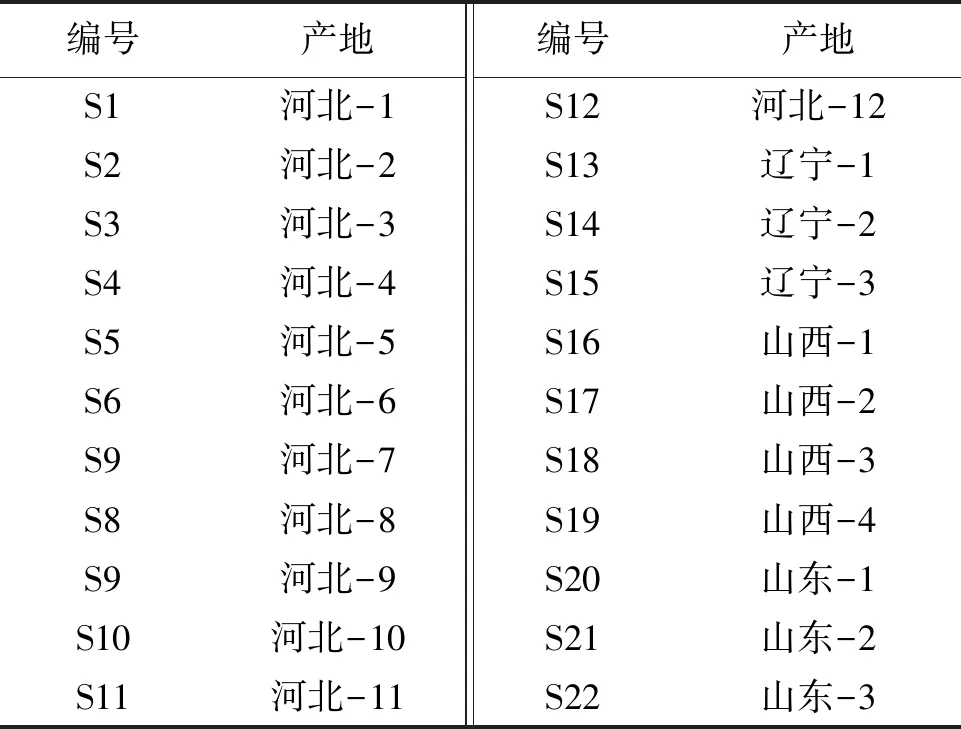
表1 22批山楂叶样品信息
2 方法与结果
2.1溶液制备
2.1.1 混合对照品溶液 分别精密称取对照品绿原酸、牡荆素葡萄糖苷、金丝桃苷、异槲皮素、牡荆素鼠李糖苷适量,置于容量瓶中,配制为母液。精密吸取适量上述对照品母液,置于容量瓶中,配制质量浓度分别为61.98、131.82、204.00、300.00、192.00μg/mL的混合对照品溶液,摇匀,备用。
2.1.2 供试品溶液 22批不同产地山楂叶经粉碎后过80目筛。精密称取1.0g,置于具塞三角瓶中,加60%甲醇溶液50mL,称重,密封超声30min,静置,待其恢复室温重新称定并补足失重。12000r/min,10min,离心,取上层清液,0.45μm微孔滤膜滤过,得续滤液即为供试品溶液。
2.2指纹图谱及含量测定色谱条件安捷伦ZORBAX SB-C18色谱柱(4.6mm×250mm,5μm);流动相0.3%甲酸水(A)-乙腈:四氢呋喃(B,12∶1),梯度洗脱(0~15min,8%~12%B;15~25min,12%~16%B;25~38min,16%~15%B;38~45min,15%~20%B;45~50min,20%~34%B;50~55min,34%~100%B)。1mL/min的流速及30℃的柱温;进样体积10μL;检测波长363nm。
2.3方法学考察
2.3.1 线性关系及定量限、检测限 精密吸取5mL“2.1.1”项下的混合对照品溶液,置10mL的容量瓶中,加60%甲醇摇匀,定容。倍比稀释依次加60%甲醇制成系列浓度溶液,获得7个水平的混合对照品溶液,通过“2.2”项下的色谱条件进行测定。以质量浓度为横坐标(X),峰面积为纵坐标(Y)进行线性回归分析,得回归方程、相关系数及线性范围。精密吸取“2.1.1”项下混合对照品溶液适量,倍比稀释,通过“2.2”项下的色谱条件测定,以S/N=10作为定量限(LOQ),信噪比(S/N)=3作为检测限(LOD),见表2。
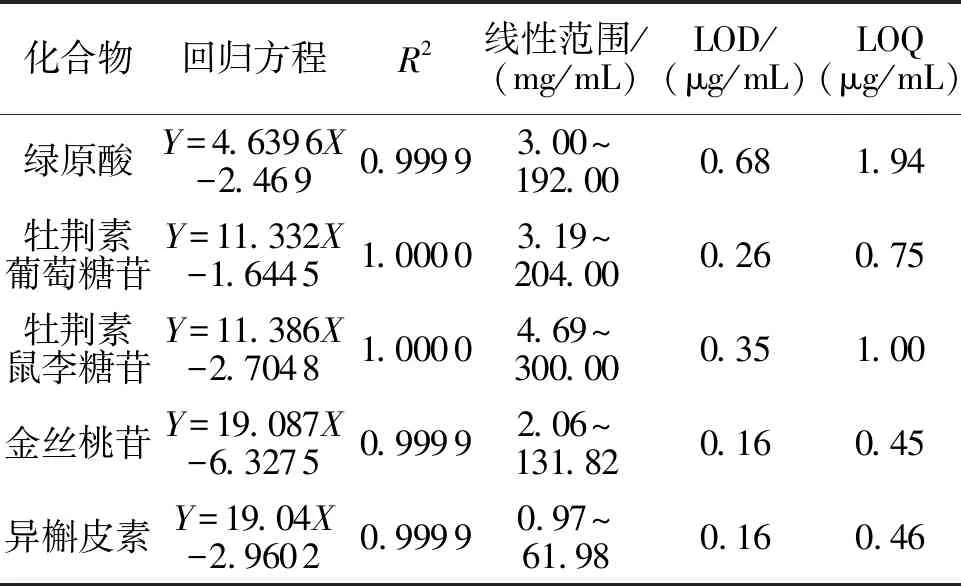
表2 5种指标成分的回归方程,相关系数,线性范围及定量限,检测限
2.3.2 专属性考察 取适量“2.1”项下的混合对照品溶液和供试品溶液,依照“2.2”的色谱条件,进样分析,记录色谱图(图1)。结果表明,供试品溶液中绿原酸、牡荆素葡萄糖苷、金丝桃苷、牡荆素鼠李糖苷和异槲皮素的色谱峰保留时间与混合对照品溶液一致,且均与相邻色谱峰的分离度良好。空白溶液对测定无干扰。


A:混合对照品溶液;B:供试品溶液;C:空白溶液;1.绿原酸;3.牡荆素葡萄糖苷;4.牡荆素鼠李糖苷;8.金丝桃苷;9.异槲皮素。
2.3.3 精密度试验 取“2.1.2”项下山楂叶供试品溶液(S9,连续进样6次,按“2.2”项下色谱条件进行检测,记录指纹图谱。以牡荆素鼠李糖苷为参比峰,计算各共有峰的相对峰面积0.1%~2.05%,相对保留时间RSD均<0.5%(n=6)。绿原酸、牡荆素葡萄糖苷、牡荆素鼠李糖苷、金丝桃苷、异槲皮素峰面积的RSD分别为0.29%、0.21%、0.33%、0.82%、0.25%。表明仪器精密度良好。
2.3.4 重复性试验 取“2.1.2”项下山楂叶药材(S9),按“2.1.1”项下制备方法,平行制备6份,并按“2.2”项下色谱条件进行检测,以牡荆素鼠李糖苷为参比峰,计算各共有峰的相对峰面积为0.23%~2.91%,相对保留时间RSD均<0.18%(n=6)。计算绿原酸、牡荆素葡萄糖苷、牡荆素鼠李糖苷、金丝桃苷、异槲皮素峰面积的RSD分别为0.91%、0.93%、0.90%、1.18%、1.01%,证明了该方法重复性良好。
2.3.5 稳定性试验 取“2.1.2”项下山楂叶供试品溶液(S9)分别于室温下放置0、2、4、8、12、22h进样,按“2.2”项下的色谱条件进行检测,以牡荆素鼠李糖苷为参比峰,计算各共有峰的相对峰面积为0.11%~2.66%(n=6)、相对保留时间RSD<0.22%(n=6)。计算绿原酸、牡荆素葡萄糖苷、牡荆素鼠李糖苷、金丝桃苷、异槲皮素峰面积的RSD分别为0.61%、0.44%、0.82%、0.73%、0.89%,说明了供试品溶液置于室温22h内稳定性良好。
2.3.6 加样回收率 精密称取6份S9样品,每份0.50g,分别按已知指标成分含量的100%加入绿原酸、牡荆素葡萄糖苷、牡荆素鼠李糖苷、金丝桃苷、异槲皮素对照品溶液。按“2.1.2”及“2.2”项下方法制备供试品溶液并测定,记录峰面积,计算加样回收率。结果如表3显示,各成分的平均加样回收率92.92%~107.19%,RSD为0.30%~2.78%,表明方法准确度良好。
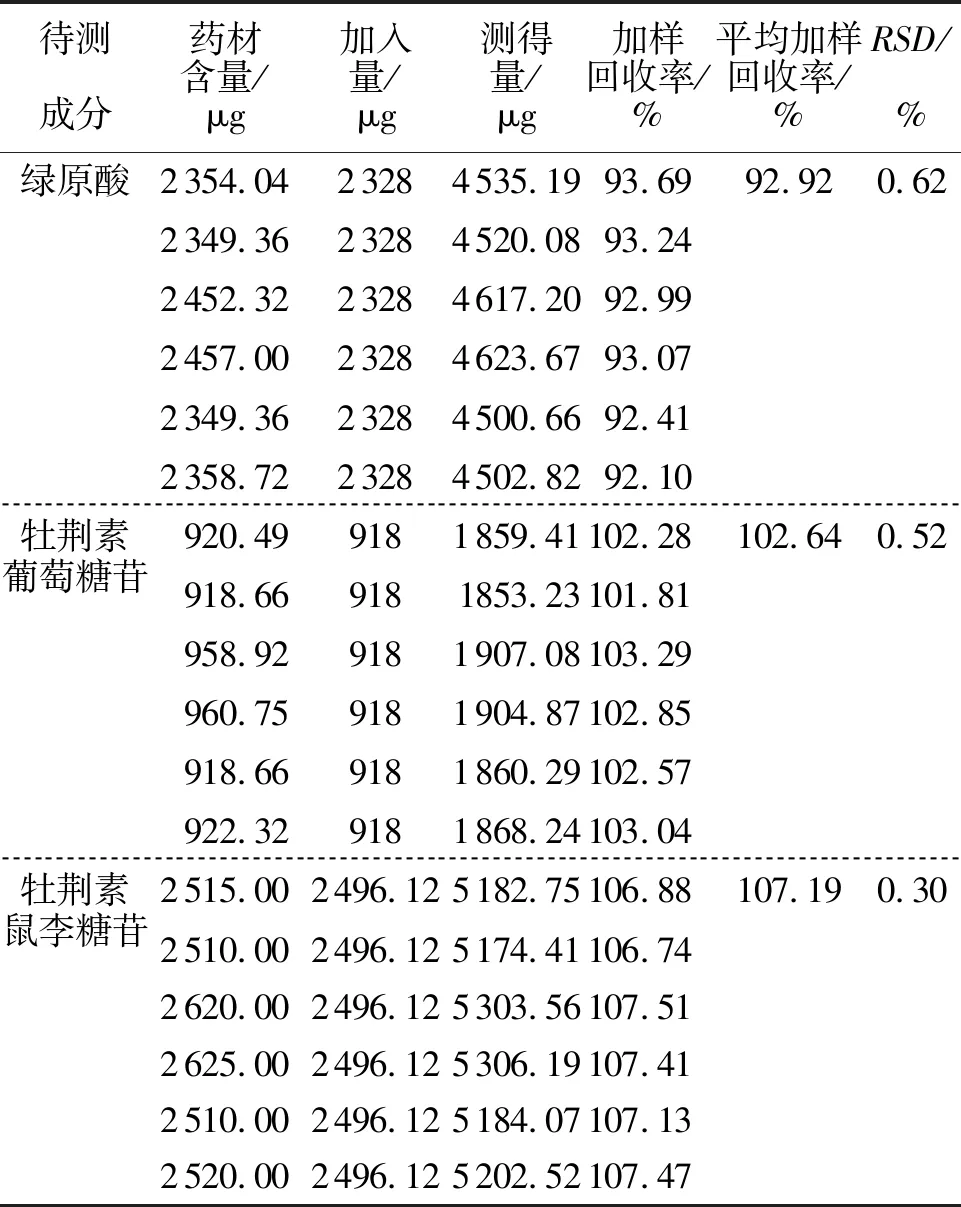
表3 绿原酸等5个成分的加样回收率试验结果(n=6)
2.4HPLC指纹图谱的建立与共有峰指认
2.4.1 建立山楂叶指纹图谱以及指认共有峰 分别称取22批山楂叶药材粉末1.0g,依照“2.1.2”与“2.2”项下方法与条件制备供试品溶液并测定记录色谱图。将山楂叶的色谱图导入《中药色谱指纹图谱相似度评价系统(2012年版)》中进行分析,参照S9样品色谱图,经中位系数法对各色谱峰进行多点校正、自动匹配并生成对照图谱(R)以及22批山楂叶样本的叠加色谱图。结果显示(图2、3)22批山楂叶样品的指纹图谱中标定了10个共有峰。结合混合对照品色谱图1(A)可见,指认峰1为绿原酸、峰3为牡荆素葡萄糖苷、峰4为牡荆素鼠李糖苷、峰8为金丝桃苷、峰9为异槲皮素。
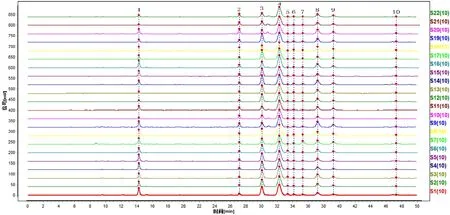
图2 22批山楂叶的叠加色谱图
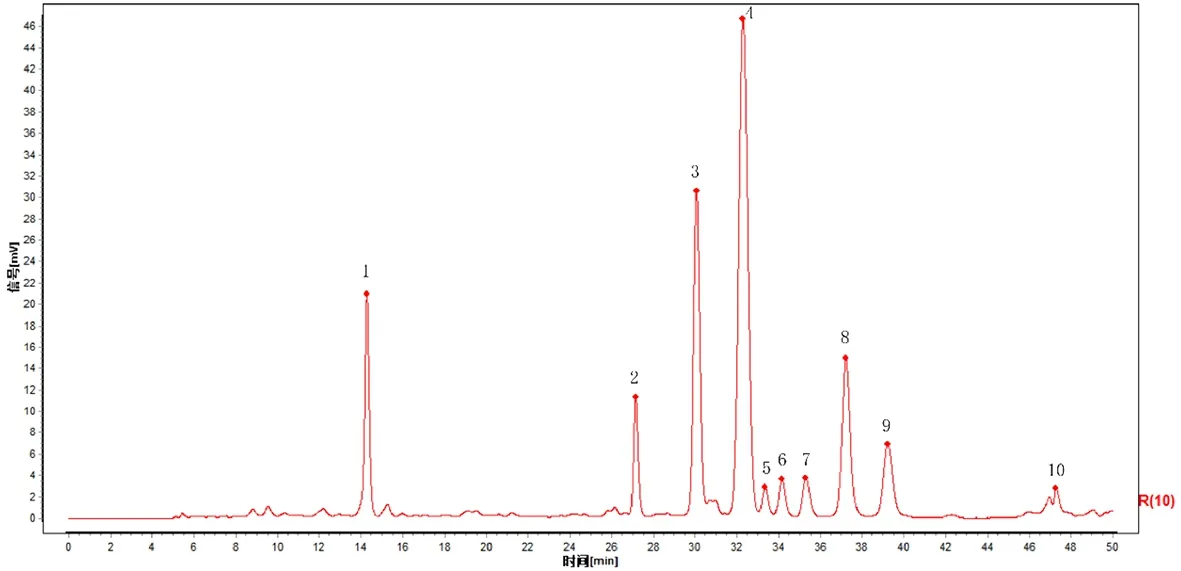
图3 山楂叶的对照指纹图谱
2.4.2 相似度评价 通过《中药色谱指纹图谱相似度评价系统(2012年版)》软件,对22批山楂叶样品指纹图谱与对照指纹图谱的相似度进行分析。由表4所示,发现22批山楂叶指纹图谱与对照图谱相似,S1~S22相似度均高于0.900。这表明不同产地山楂叶的色谱特征相似,化学成分大体相同。
2.5化学模式识别分析
2.5.1 系统聚类分析 采用SPSS 21.0软件,使用Ward法,以平方欧氏距离为测度,以22批山楂叶指纹图谱的10个共有峰峰面积为变量,进行聚类分析[17]。22批山楂叶的聚类分析树状图(图4),结果显示,当平方欧氏距离为10时,22批样品可聚为两类,S1~S15辽宁、河北产地药材聚为一类,S16~S22山西、山东产地药材聚为一类。这可能与产地的温度气候、空气土壤和地理位置等因素相关。
2.5.2 峰面积的主成分分析 采用SPSS 21.0对22批山楂叶样品进行主成分分析。由表5所示,前3个因子的特征值>1,对总方差的累计贡献率达到80.825%,提示这3个主成分涵盖了山楂叶样品指纹图谱中10个分析变量的大部分信息。由表5、表6看出,主成分1的信息量最大,方差贡献率为44.059%。峰1、3、5、6、7在第1主成分上有较高载荷,说明单主成分1就反映了这5个成分的信息;第2主成分方差贡献率为23.795%,主要反映了峰2、8、9、10的指标信息;主成分3的方差贡献率为12.971%,主要反映了峰4的指标信息。由此因子荷载矩阵表推测,影响山楂叶质量差异的并不是单一成分,而是多成分的协同作用的结果。同时以此三类主成分构建22批山楂叶三维(3D)图,结果见图5,其分类结果与“2.5.1”项下聚类分析结果一致,即S1~S15河北、辽宁产地聚为一类,S16~S22山东、山西产地为一类。
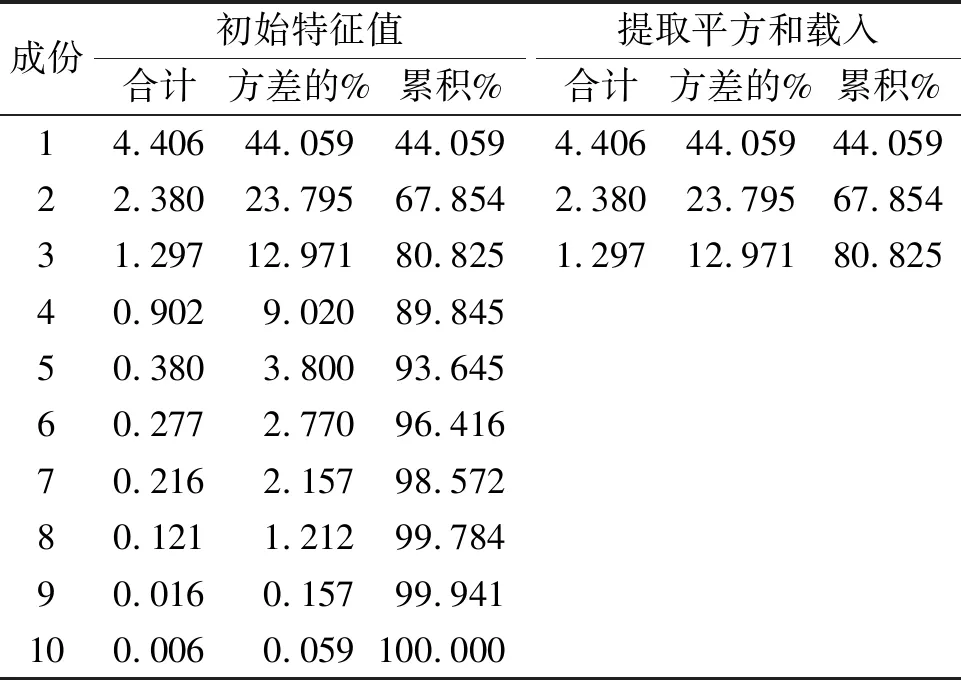
表5 山楂叶主成分分析的特征值与累计方差贡献率
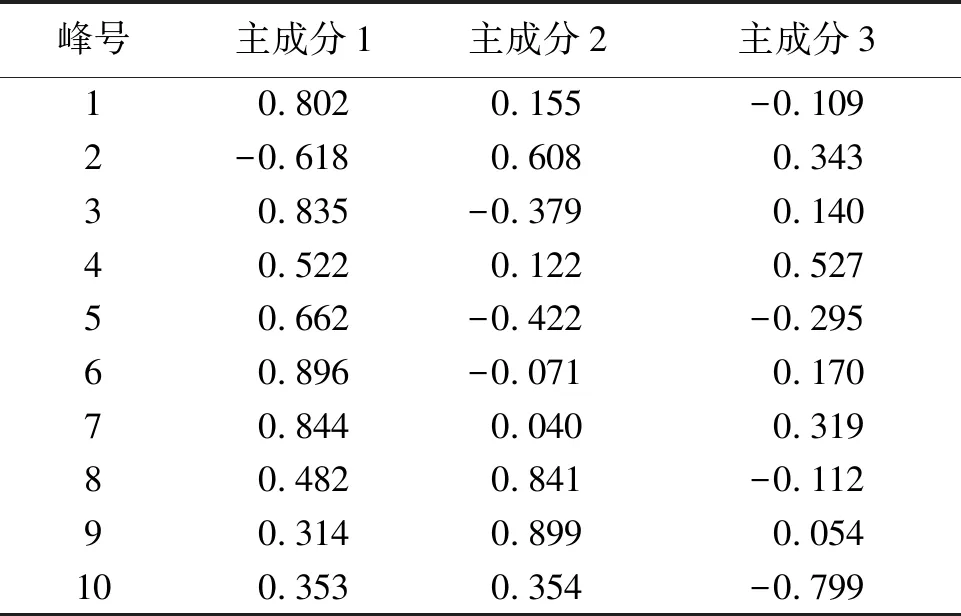
表6 山楂叶主成分分析的初始因子载荷矩阵
2.6主要成分含量测定
2.6.1 溶液的制备 混合对照品溶液和供试品溶液的制备分别同“2.1.1,2.1.2”项。空白溶液为60%甲醇。
2.6.2 色谱条件 同“2.2”项。
2.6.3 样品含量测定 精密称取22批山楂叶样品粉末各1.0g,按“2.1.2”项下方法制备供试品溶液,再按“2.2”项下色谱条件进样测定,记录峰面积,按外标法计算样品含量。各样品平行测定3次,见表7。

表7 22批山楂叶药材的含量测定结果(n=3,mg/g)
3 讨论
本课题组在前期实验中以色谱峰的分离度、峰形、峰面积等为指标考察了不同流动相系统、不同柱温(20、25、30℃)、检测波长(363、350、340、320、296nm)以及流速(1.0、1.2、0.8mL/min)等,结果显示,以0.3%甲酸水(A)-乙腈:四氢呋喃(B,12∶1)为流动相,柱温为30℃,波长为363nm,流速为1mL/min时,色谱图中基线相对平稳,色谱峰峰形较好,分离度较高。
本研究建立了山楂叶的HPLC指纹图谱及5个成分的含量测定方法。并对22批山楂叶样本进行了主成分分析和聚类分析,两种分析结果完全一致,显示可聚为两类,河北与辽宁产地的药材S1~S15聚为一类,因其峰1(绿原酸)、峰3(牡荆素葡萄糖苷)、峰4(牡荆素鼠李糖苷)均较高,这与河北、辽宁同纬度,地处亚欧大陆东岸,同属大陆性季风气候相关。山西与山东产地的药材S16~S22聚为一类,5种成分含量均差别不大,这与山东、山西地处同纬度,地理条件相似有关。对5种成分含量进一步研究发现,河北、辽宁产地的绿原酸、牡荆素葡萄糖苷含量均高于山东、山西,牡荆素鼠李糖苷、金丝桃苷含量四地差别不大,这也是河北、辽宁产地药材聚为一类,山东、山西产地药材聚为一类的原因。由4个产地的牡荆素鼠李糖苷、金丝桃苷含量相似可以看出,《中国药典》将这两种成分作为山楂叶药材与山楂叶提取物主要含量测定指标进行质控是经过多方考量的。
综上,本研究所建立的HPLC指纹图谱和含量测定方法分离度高、平稳、简单、准确。指纹图谱结合多组分含量测定、主成分分析以及聚类分析,相对于单一成分的测定方法可从整体上体现山楂叶质量。不同的环境气候、空气土壤使得药材质量参差不齐,药材质量不同对临床疗效也是不尽相同的,中药化学成分复杂,不同药材的内在质量必然影响疗效。因此本研究建立的方法能够对不同产地山楂叶药材的质量进行客观地评价,为其在临床上更好的应用提供更加客观的理论基础。同时为更准确评价山楂叶质量,还需开展更多药效与药材内在质量联系研究,以完善山楂叶质量标准。

