ZHL-02 置换镀和电镀银层的耐蚀性能研究
郑乐怡,王 荣,姚佳雯,卢玄冰,俞巧珍,于晓辉,张 楠,史天静,赵健伟
(1.嘉兴学院a.材料与纺织工程学院,b.设计学院,浙江 嘉兴 314001;2.江苏东华分析仪器有限公司,江苏 靖江 214500)
0 前 言
我国海域存在湿度大、海水含盐量高的特点,沿海及海上的电力系统和仪器仪表受海水、海风、盐雾等环境因素的影响极易受到氯盐侵蚀,使其安全服役性能下降,结构提早失效[1]。目前,针对海洋环境中混凝土和钢结构腐蚀的防护技术已有诸多研究[1,2]。但对海洋建筑及基础设施中的电子元件和仪器、仪表的耐腐蚀性能的研究则少有报道。银因具有良好的反光度和导电、导热、焊接性能而被广泛应用于电力系统中的高压隔离开关、电子工业以及仪器仪表制造等高端产业。银镀层的质量,尤其是耐腐蚀性能的好坏直接影响镀件性能的稳定性和使用寿命[1]。传统的氰化镀银因具有镀液稳定、成本低以及镀层性能优良等特点,曾被广泛应用于工业生产,但因氰化物为剧毒,对环境以及操作者的身体有巨大危害,已于2006 年底前被淘汰[3,4]。目前,国内外无氰镀银体系主要有硫代硫酸盐、亚氨基二磺酸盐、甲基磺酸和乙内酰脲[5-11]等,但这些体系下得到的银镀层的耐腐蚀性能的研究几乎没有报道。本课题组基于互补型双组分配位的原理,开发了以5,5-二甲基酰胺为主配位剂的系列无氰镀银工艺[12],具有较宽的工作温度范围和较大的电流密度[13,14],可广泛应用于挂镀[15],滚镀和刷镀[16],获得的银颗粒尺度可以低至十余nm[17],表现出极高的拉曼光谱增强活性[18,19]。但该工艺还存在一些问题,主要在于制备的镀层的性能稳定性还不够理想,如新鲜的镀银层呈蓝色,但在含卤化物、硫化物的空气中易变色,并且此前试验研究发现[20]制备的镀层长期保存在潮湿的自然环境中时易发生腐蚀变色,因此有必要对该工艺制备的镀层的耐蚀性能进行研究。
1 试验部分
1.1 试剂与仪器
本工作使用的主要试剂如下:NaCl(质量分数为99.5%)为分析纯,ZHL-02 无氰镀银基础镀液(AgNO3含量为22.5 g/L),镀件为市售紫铜片(40.0 mm×50.0 mm×0.8 mm)。
本工作采用的主要仪器如下:SU8010 扫描电子显微镜;DH7003 双通道电化学工作站;UTP1306S 直流稳压电源;D8-A25 X 射线衍射仪(XRD);EDX600 X 射线荧光镀层测厚仪。
1.2 样品制备
将紫铜镀件分别在丙酮和去离子水中各超声处理5 min,再用体积分数为10%的盐酸浸蚀3~5 min,体积分数为5%的硫酸活化3~5 min,水洗后进行置换镀银或直流电镀银,电镀后的试样水洗、干燥后测试用。其中将ZHL-02 镀液温度设定在(40±1) ℃。电镀采用恒电流方法,电流密度为1.0 A/dm2,持续时间分别为1、2、5 min。
对比试样为相同条件下制得的样品,但未用电线连接。
1.3 腐蚀测试
试样表面腐蚀测试、电化学测试采用三电极体系,其中镀银铜片为工作电极、饱和甘汞电极为参比电极、螺旋状铂丝电极为辅助电极,在3.5%(质量分数,下同)NaCl 溶液中测量交流阻抗(EIS)谱和Tafel 极化曲线。
EIS 测量采用控制电位的方式,先将镀银铜片置于3.5%NaCl 溶液中腐蚀4 h,待稳定后再进行控制电位EIS 测试。测试频率设置为1.0×(10-2~105)Hz,振幅为10 mV。进行Tafel 极化测试时,为考察试样的阳极极化特征,电位扫描由相对开路电位-300 ~-500 mV扫描至300~500 mV,阶跃高度为0.1 mV,阶跃时间为0.1 s,即扫描速率为1.0 mV/s。
电偶腐蚀测试按照GB/T 15748 将镀银铜片作为一极,纯银片作为一极,把这两极配成偶对,每一偶对都需并排垂直放置。将配好的偶对置于含3.5%NaCl溶液的烧杯中,试验溶液与试样面积比不小于20 mL/cm2,2 个试样之间的距离为30 mm,保持每组平行试样之间的距离一致,且2 个试样水平中心线在同一高度。利用电偶腐蚀方法每天分别测量试样在试验溶液中的电偶电位和电偶电流。电偶腐蚀测试时长为15 d。
1.4 数据分析
腐蚀速率计算公式见式(1):
式中,F为法利第常数96 485 C/mol,v深为腐蚀速率,mm/a;Δm为阳极试样溶解金属的质量,g;S为试样的表面积,m2;t为腐蚀时间,h;Jcorr为腐蚀电流密度,μA/cm2;M为试样的相对原子质量;ρCu为紫铜的密度,g/cm3;nCu为铜的价数。
平均电偶腐蚀速率见式(2):
式中,Kc为平均电偶腐蚀速率,mm/a;Wc0和Wc1分别为阳极试样在试验前和试验后的质量,g;W0和W1为对比试样在试验前和试验后的质量,g;S为阳极试样的表面积,m2;t为试验时间,h。
2 结果与讨论
2.1 ZHL-02 置换镀银层的耐蚀行为
银离子的标准电极电位是0.799 V,即使在配位剂过量的条件下,依然有一定浓度的游离银离子,可以与铜(标准电极电位为0.340 V)或其他活泼金属基底发生置换反应,形成一层较薄的置换银层。这也形成了一种特殊的施镀方法,即无电沉积(Electroless Deposition)。该方法比传统电镀法有更好的分散能力和深镀能力,使有复杂三维结构的零件也能均匀地镀上一层薄银,其不足之处是难以得到较厚的镀层,且耗时长,成本高。因镀层较薄,其耐腐蚀性能更需要深入考察。
图1 为置换镀银层的SEM 形貌和XRD 谱。由图1a 可知,在未加电极电位时,由于铜在零件表面与银离子通过置换发生反应,反应条件温和,速率慢,因此银层在大范围内较为均匀,且晶态发育良好。其晶面平整,棱角分明,顶点尖锐与在微米尺度铜材置换镀银的结晶特点一致。同时颗粒尺度大至数百纳米,形状不规则。图1b 展示了置换镀银层的XRD 谱。置换镀银层的厚度较薄,利用X 射线荧光镀层测厚仪可知在试验开始3~4 min 后镀银层厚度稳定在0.6 ~0.7 μm,不足以完全遮蔽铜基底,因此从图1b 中仍可以看到在43.079 0°、50.170 7°和73.915 2°处出现Cu 的特征衍射峰,峰型尖锐,分别对应Cu 的(111)、(200)和(220)晶面。位于37.843 0°和44.088 0°的2 个特征衍射峰对应Ag 的(111)和(200)晶面。其中,通过衍射峰的峰宽可以得到不同晶面的晶粒尺寸,结合Scherrer 公式计算得到,置换镀银层表面Ag 的(111)和(200)晶面的表观晶粒尺寸分别为68 nm 和58 nm。
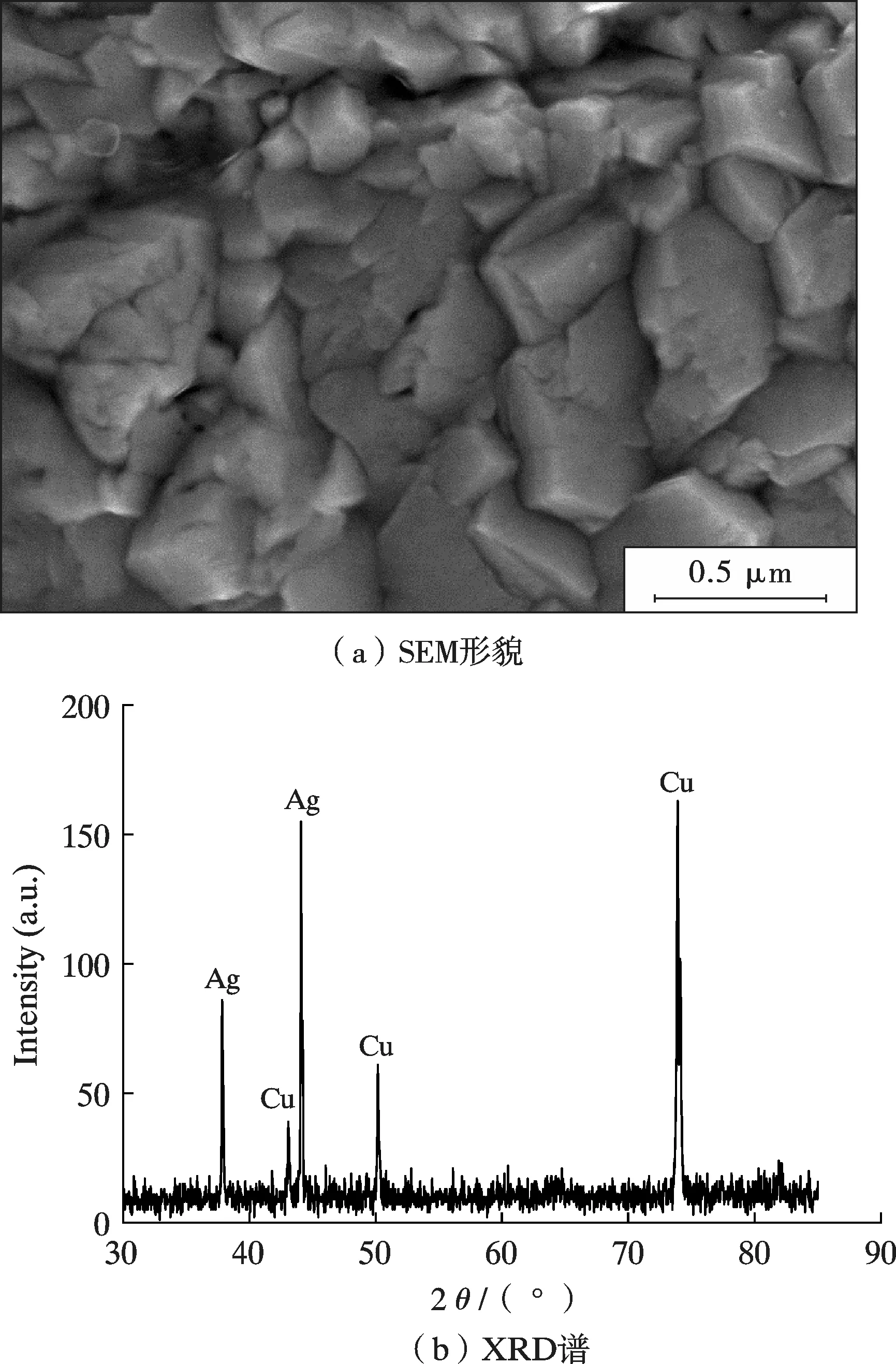
图1 置换镀20 min 后银层的SEM 形貌和XRD 谱Fig.1 SEM morphology and XRD spectrum of silver layer after 20 min of replacement plating
图2 比较了铜基底和置换镀银分别为3、6、30 min的4 个试样的Tafel 曲线。由图2 可知,在阴极极化区试样受到了保护,电流密度在较大的电位变化区间(-0.7~-0.3 V)内缓慢降低,在-0.15~-0.30 V 区间内4 个试样的极化电流密度均急剧减小,最小电流密度对应的电位为自腐蚀电位。铜基体的自腐蚀电位为-0.280 V,置换镀3 min 后试样的自腐蚀电位正移至-0.210 V,而置换镀6 min 和30 min 后试样的自腐蚀电位分别为-0.180 V 和-0.170 V,二者相差不大。自腐蚀电位更正,说明试样有更好的耐蚀性能,此外,在阳极极化区,相比铜基材,镀银试样的自腐蚀电流密度也有明显降低。通过Tafel 直线外推法可以得出铜基体和置换镀银3、6、30 min 试样的自腐蚀电流密度,代入式(1)可计算出对应的自腐蚀速率,分别为5.40×10-2、9.15×10-3、7.35×10-3、1.15×10-2mm/a。
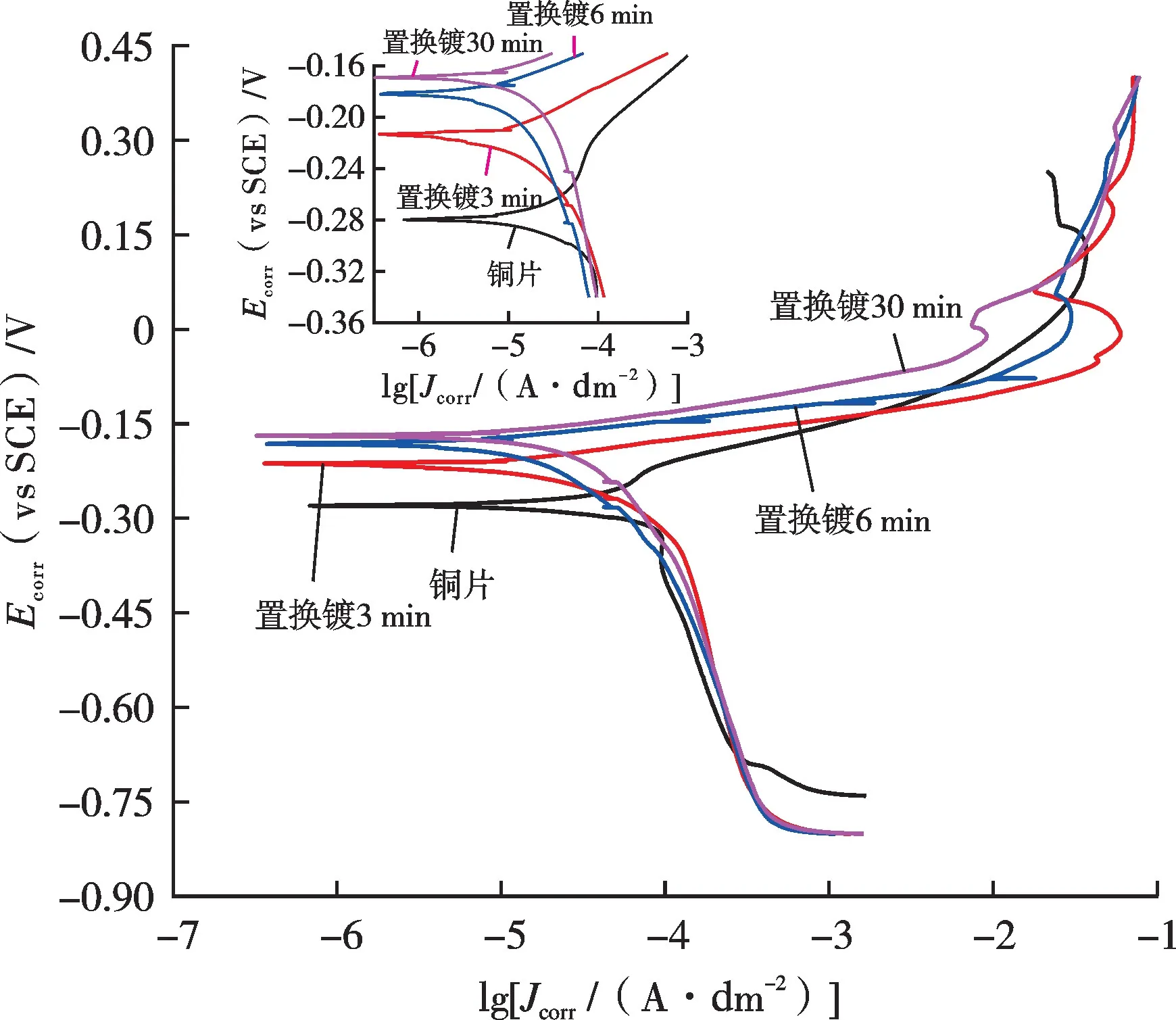
图2 基底和置换镀银层的Tafel 曲线Fig.2 Tafel curves of substrate and replacement silver plating layers
镀银件在潮湿、近海等恶劣环境中发生腐蚀的现象普遍存在。可利用电偶腐蚀方法每天分别测量试样在试验溶液中的电偶电位和电偶电流密度,如图3 所示。由图3a 可知电偶电流密度在前2 d 有超过0.2 mA/dm2的降幅后,在随后的10 余天内变化不再显著,说明腐蚀形成的惰性层能阻碍腐蚀的进一步发展。而电偶电位在前10 d 持续下降,降幅超过40 mV 后保持稳定。随时间的延长,置换镀银层的厚度变化很小甚至不变,因此选取了20 min 时的情况作为重点研究,当置换镀银20 min 时,对比试样腐蚀前后质量差为0.062 7 g;进行电偶腐蚀时,质量差为0.072 0 g,这时的电偶腐蚀失重为0.009 3 g,电偶平均腐蚀速率为1.84×10-3mm/a。
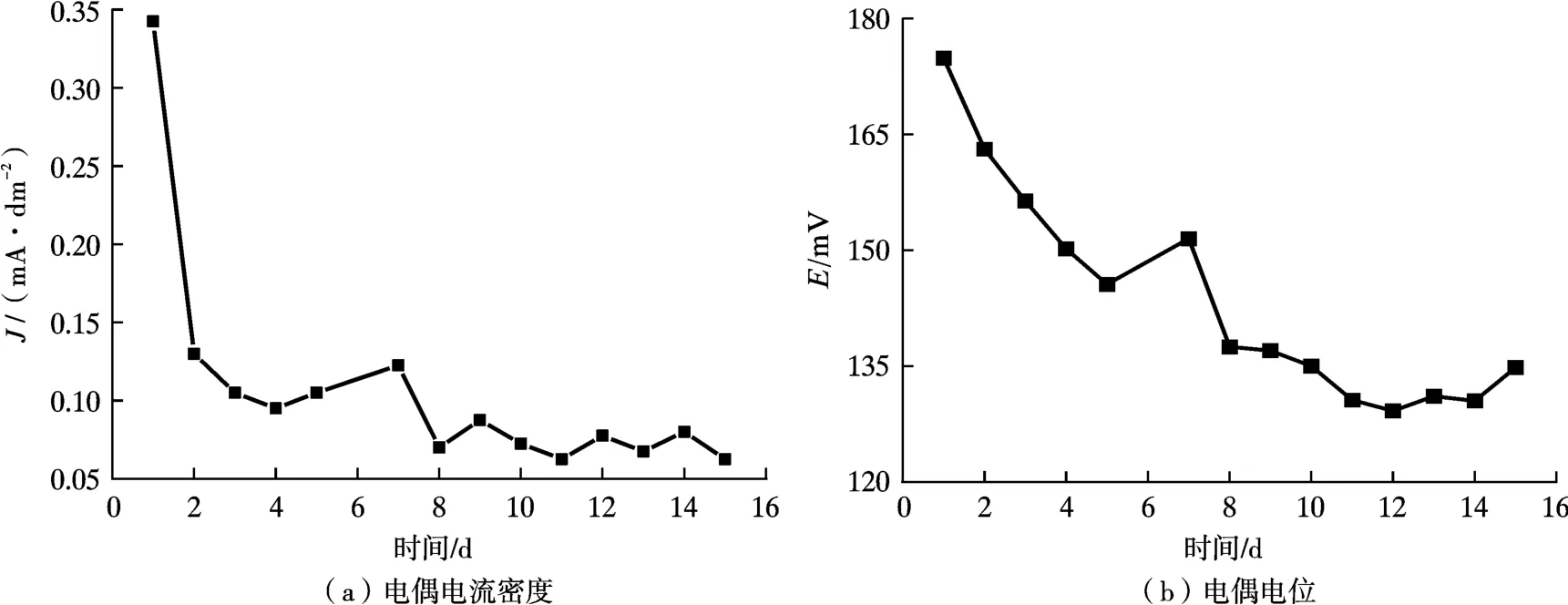
图3 置换镀银20 min 后银层的电偶腐蚀参数与时间的关系Fig.3 Relationship between galvanic corrosion parameters and time of the silver layer after 20 min of replacement silver plating
图4 为置换镀银层浸泡在3.5%NaCl 溶液中腐蚀的EIS 谱。在Nyquist 谱中,中低频区对应镀层的腐蚀反应,所包含的腐蚀变化较为复杂,而高频区可能与镀层的物理电阻有关。由图4 可知,置换镀银层在腐蚀测试期间,出现1 个半圆形,且半径比较大,此时镀层表面较为紧密,腐蚀介质较难到达基体表面。
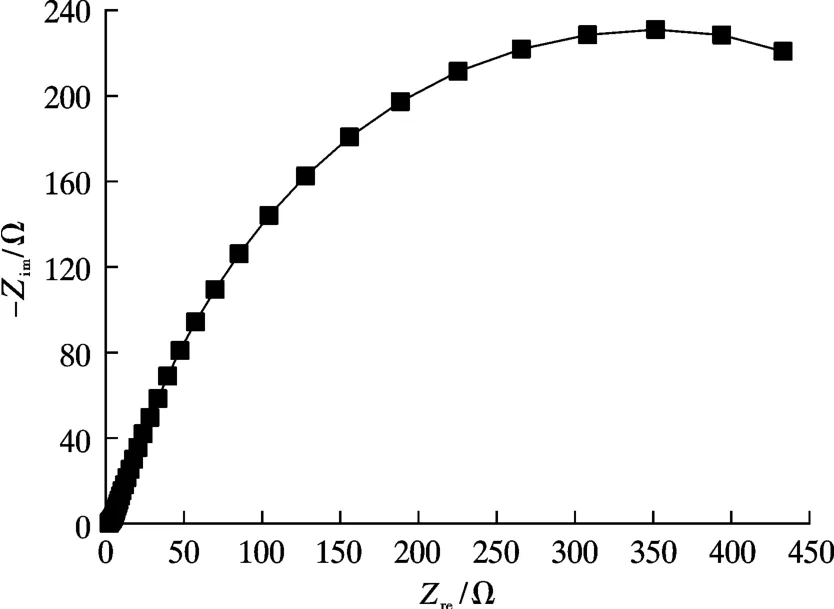
图4 置换镀银20 min 后银层浸泡在3.5%NaCl溶液中腐蚀的EIS 谱Fig.4 EIS spectrum of corrosion of the silver layer immersed in 3.5%NaCl solution after 20 min of replacement silver plating
图5 为置换镀银层在腐蚀前后的显微形貌。腐蚀前,置换镀银层表面平整,镀层相对均匀。对比试样腐蚀15 d 后,可以看到镀层表面出现了较多细小的腐蚀点,多数沿着基底原有划痕分布。经过15 d 电偶腐蚀后,置换镀银试样表面出现了较多大面积的腐蚀点,部分已经连成片。从上述结果也可以看出,置换镀银层的耐蚀性较差。

图5 置换镀银层在腐蚀前后的显微形貌Fig.5 Micro-morphology of replacement silver plating layers before and after corrosion
2.2 ZHL-02 电镀银层的耐蚀行为
对于尺寸较大的镀件,可以利用电镀工艺获得更厚的银镀层,从而提高镀件的耐蚀性能。图6 为电流密度为1.0 A/dm2时不同电镀时间镀银层的SEM 形貌和XRD 谱。由图6 可知,在电镀1 min 时,铜基底上己经覆盖一层银颗粒,颗粒排列紧密且分布均匀。电镀5 min 时,银层中大颗粒明显增多,镀层变厚,颗粒尺寸约为12~14 μm。利用X 射线荧光镀层测厚仪可知在电镀1、2、5 min 时的基底上,镀层的厚度分别约为0.45~0.50 μm、0.95 ~1.05 μm、2.40 ~2.70 μm。从图6所示XRD 谱中也可以看到:与置换镀银相比,电镀银层形成得更为快速,沉积效率更高。在电镀1 min 后,电镀银层的厚度就达到了与置换镀银7 ~90 min 后类似的结果。随着电镀时间的延长,银的特征衍射峰强度随之增加,铜的特征衍射峰逐渐被银层覆盖。在电镀1 min 时仍能观察到铜的衍射峰,电镀2 min 后铜的衍射峰明显减弱,基本上观察不到铜的衍射峰,在5 min 时电镀银层覆盖得更为明显,说明电镀银层的形成比置换镀银层的形成更为迅速,且镀层更厚,电镀银层的银的晶粒尺寸为16~18 nm,远小于置换镀银形成的银的晶粒尺寸。这与观察电镀银层和置换镀银层的SEM 形貌所得的结果一致。
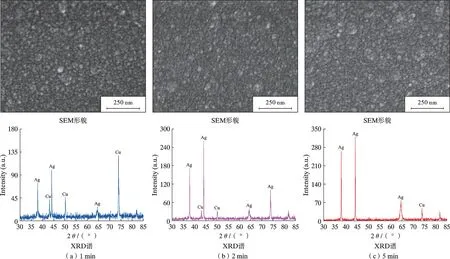
图6 不同电镀时间镀银层的SEM 形貌和XRD 谱Fig.6 SEM morphology and XRD spectra of silver plating layers at different plating times
图7 为电镀时长分别为1、2、5 min 的电镀银层的Tafel 曲线。
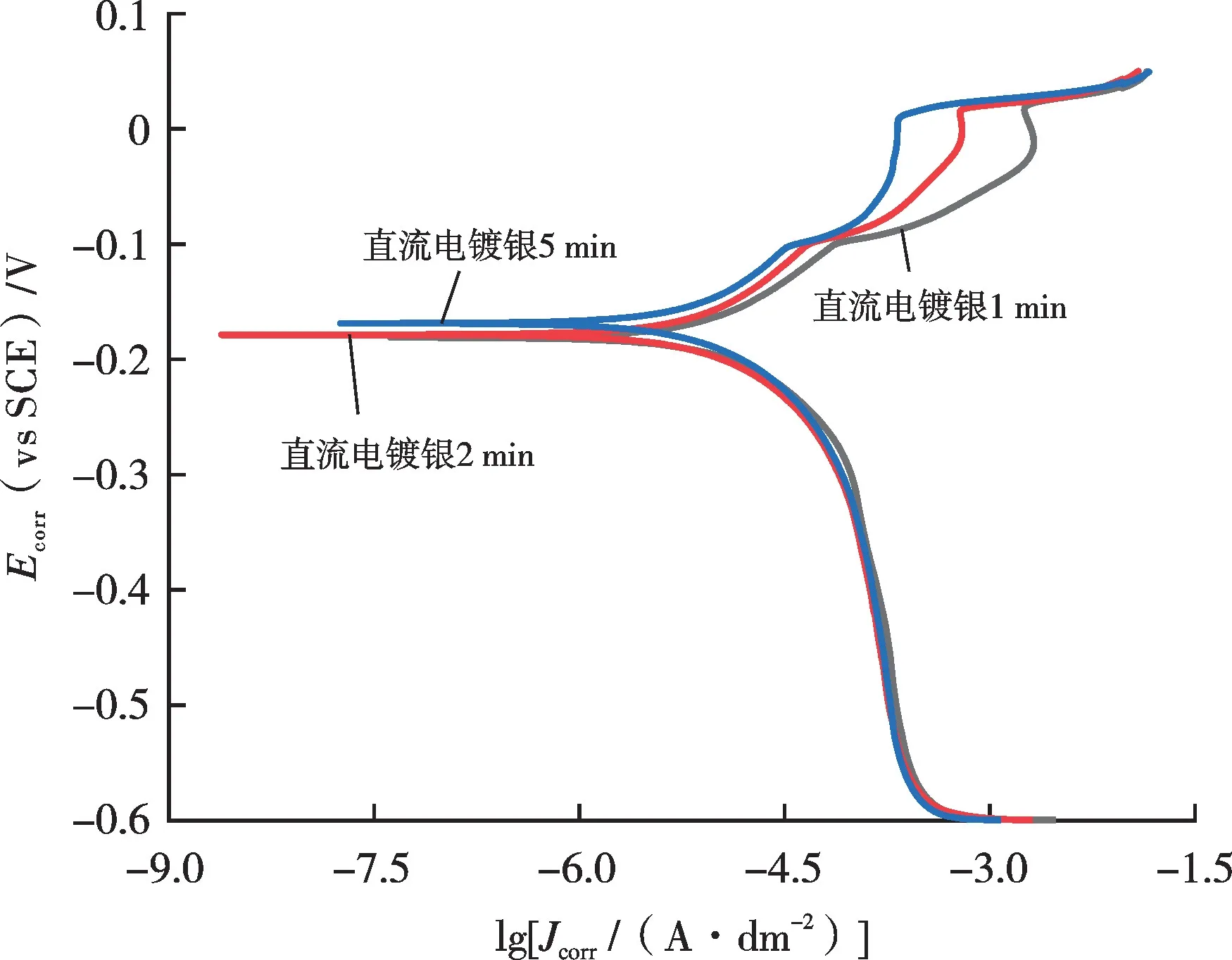
图7 电镀银层的Tafel 曲线Fig.7 Tafel curves of silver plating layers
电镀时长分别为1、2、5 min 的电镀银层的自腐蚀电位分别为-0.181、-0.178、-0.168 V,随着电镀时间的延长,腐蚀电位有微小的正移,说明镀层的耐蚀性能逐渐提高。此外,还发现电镀1 ~2 min 的银镀层与置换镀银6 ~30 min 的银镀层的自腐蚀电位相当。通过Tafel直线外推法可以得出电镀银时间为1、2、5 min 的银镀层的自腐蚀电流密度,代入式(1)可计算出对应的自腐蚀速率,分别为7.15×10-3、5.30×10-3、4.27×10-3mm/a。与置换镀银层的自腐蚀速率相比,电镀银镀层的自腐蚀速率较小,由此可见电镀银镀层的耐腐蚀性能较好。
图8 为电镀银层的电偶腐蚀参数与时间的关系。由图8 可知,电镀时间为1 min 时,试样的电偶电位及电偶电流密度偏大,说明电偶腐蚀较严重,当电镀时间为2~5 min 时,试样的电偶电位及电偶电流密度的差异不显著,且耐蚀性能与电镀1 min 的试样相比有明显改善。电镀1 min 的镀层的平均腐蚀速率为3.06×10-3mm/a,大于饱和置换镀银(即置换镀银20 min 且镀液中银离子过量)镀层的平均腐蚀速率。当电镀2 min,镀层的厚度接近1 μm,平均电偶腐蚀速率为1.98×10-3mm/a,略大于饱和置换镀银的平均电偶腐蚀速率。当镀上更厚的银层时,电镀5 min 时的镀层的平均腐蚀速率为4.90×10-3mm/a,耐蚀性能反而下降。这是由于随着电镀时间的延长,银层中会出现较大的颗粒,形成细小气孔等缺陷结构。结果表明,电镀时间为1、2、5 min 的镀层的耐蚀性均不如置换镀的镀层。
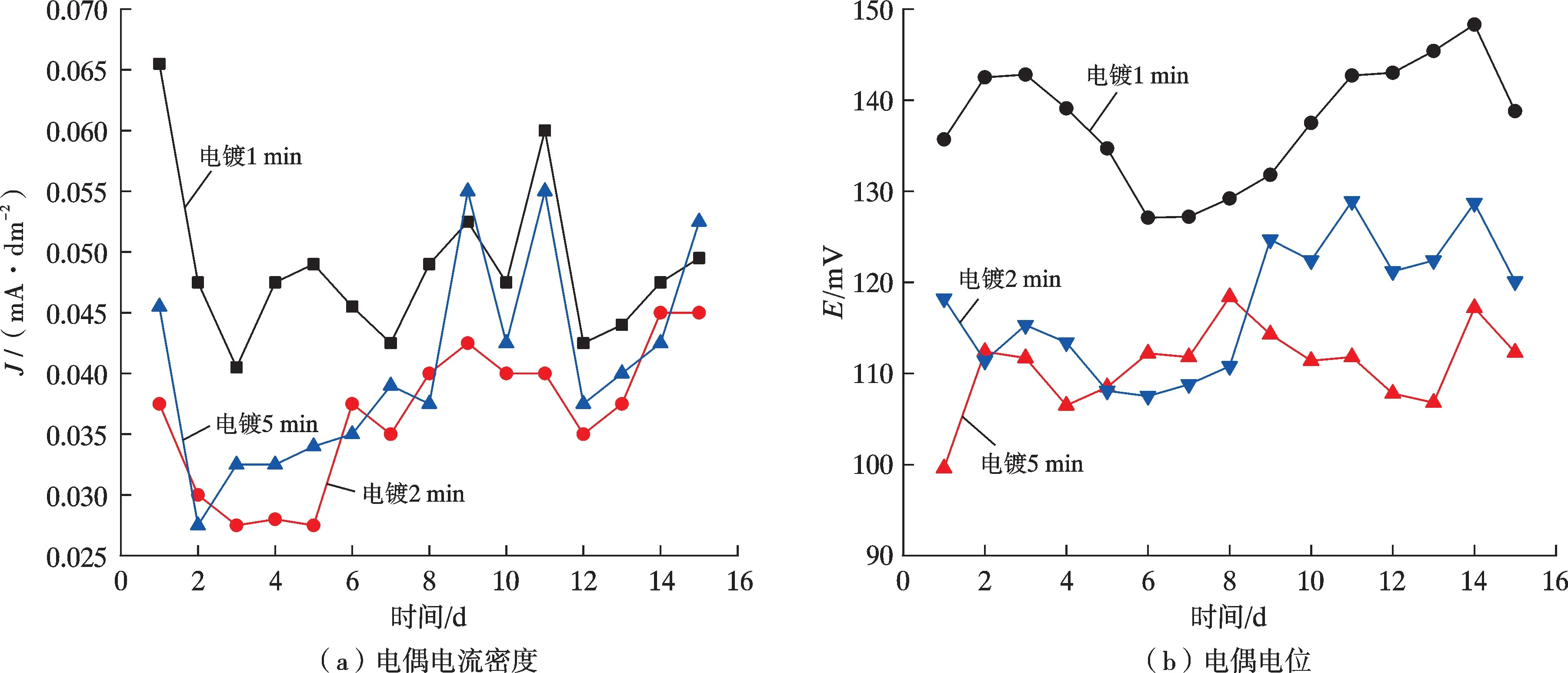
图8 电镀银层的电偶腐蚀参数与时间的关系Fig.8 Relationship between galvanic corrosion parameters of silver plating layers and time
图9 为电镀银层浸泡在3.5%NaCl 溶液中腐蚀的EIS 谱。由图9 可知,不同电镀时间镀银铜片的电化学阻抗在腐蚀期间内差异较大,在低频区更为明显,这是因为低频半圆给出了镀银铜片的相关腐蚀反应的信息。阻抗谱仅具有1 个时间常数,基体表面的镀层等同于屏蔽层,将腐蚀介质和基体完全隔离开。从图9可以看出,随着电镀时间的延长,曲线半径增大,说明镀层的致密度增加,腐蚀介质难以进入基体表面。即适当延长电镀时间能提高镀层的耐蚀性能。
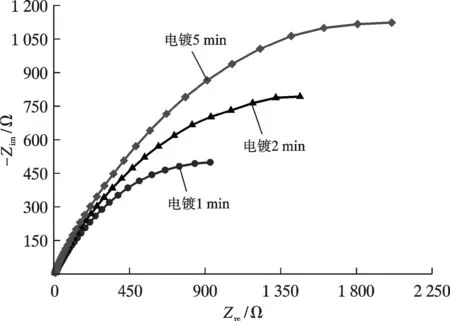
图9 电镀银层浸泡在3.5%NaCl 溶液中腐蚀的EIS 谱Fig.9 EIS spectra of corrosion of silver plating layers immersed in 3.5%NaCl solution
3 结 论
置换镀层结晶好,覆盖更完整,在同等厚度条件下,耐电偶腐蚀性能略优于电镀层。随着置换镀银时间的延长,镀层的自腐蚀速率逐渐下降。但置换镀银耗时长,且难以获得厚度大于1 μm 的镀层,一定程度上限制了其应用。相较于置换镀银,电镀银的反应速率快得多,电镀5 min 就可获得厚度>2.4 μm 的银镀层。随着电镀时间的延长,银层中会出现较大的颗粒,形成细小气孔等缺陷结构,电镀银时间为1、2、5 min时,对应的自腐蚀速率分别为7.15×10-3、5.30×10-3、4.27×10-3mm/a,随着电镀时间的延长,镀层的平均电偶腐蚀速率先下降后增大。在相同的镀银时间下,电镀镀层的耐蚀性能优于置换镀层,但耐电偶腐蚀性能却比置换镀层略差。

