含铜低碳钢在不同pH 值的Cl-环境中的腐蚀性能研究
王建斌,许秀婷,薛云升,刘宏宇,海国泉,郭 菁,滕莹雪
(辽宁科技大学材料与冶金学院,辽宁 鞍山 114051)
0 前 言
腐蚀会显著降低钢材的力学性能,缩短设备的使用寿命[1]。钢材在不同的pH 值环境中具有不同的腐蚀特性。当钢材处于碱性和中性的腐蚀介质中时,其质量损失主要是磨损所致。因为在碱性和中性腐蚀介质中腐蚀产物不易溶解,从而附着于钢材表面,减小了腐蚀反应的有效面积,进而降低了腐蚀速率,产生的蚀坑较小;在酸性腐蚀介质中钢材的质量损失主要是由腐蚀引起的,由于在酸性的环境中,钢的腐蚀产物会溶解于介质中,新鲜表面不断与腐蚀介质接触,同时钢中的渗碳体与铁素体形成微原电池,使得腐蚀速率增大[2-5]。
一般来说,向钢中添加铜、镍、铬等成分有利于提高钢材的耐蚀性,铜、镍、铬的含量达到特定值时,钢的耐蚀性会大幅度提高[6-9]。铜元素作为钢中重要的合金元素,可以提高钢的强度、耐腐蚀性能、冷加工性能[10-14]。目前,可采用含铜钢制备在高温条件下服役的具有良好耐蚀、耐磨性能的设备[15-17]。对含铜钢进行固溶处理可以得到均匀的组织和可控的晶粒尺寸,而时效处理可使过饱和固溶体析出富铜相[18],从而提升材料性能。Tomio 等[19]在H2S-Cl-环境中对含铜奥氏体不锈钢进行腐蚀试验,发现Cu 会促进不锈钢表面氧化铬膜的形成,从而提高其耐点蚀性。刘欣等[1]通过电化学试验,研究了碳钢在不同pH 值红壤模拟溶液中的电化学腐蚀行为,发现碳钢的腐蚀速率随pH 值的升高而降低。Liu 等[20]通过海水挂片试验研究发现含铜钢中的Cu 可以促进α-FeOOH 的成核和结晶,使锈层更致密;富集的Cu 还可与析出的Cr 形成Cu2Cr2O4等氧化物,吸附在锈层周围,降低锈层导电性,保护基体,使含铜钢具有良好的耐蚀性。为研究含铜低碳钢在不同pH 值环境中的腐蚀规律,从而找到其最佳服役环境,本工作通过比较含铜低碳钢与普通耐候钢在不同pH 值的Cl-环境中的腐蚀特性,评价含铜低碳钢在不同pH 值条件下的耐蚀性,为含铜低碳钢在海洋环境中的应用提供参考。
1 试 验
1.1 试样制备
以普通Q345 低碳钢、船体含铜低碳钢(0CuAl)、含铜低碳钢(0Cu3Cr)为试样,3 种材料的化学成分见表1。将试样机加工为150 mm×75 mm×6 mm 的尺寸,并对试样150 mm×75 mm 的工作面钻取3.2 mm 的孔。用水砂纸逐级打磨后抛光,丙酮除油,无水乙醇清洗。用鼓风机干燥,并在使用前保存在干燥器中。
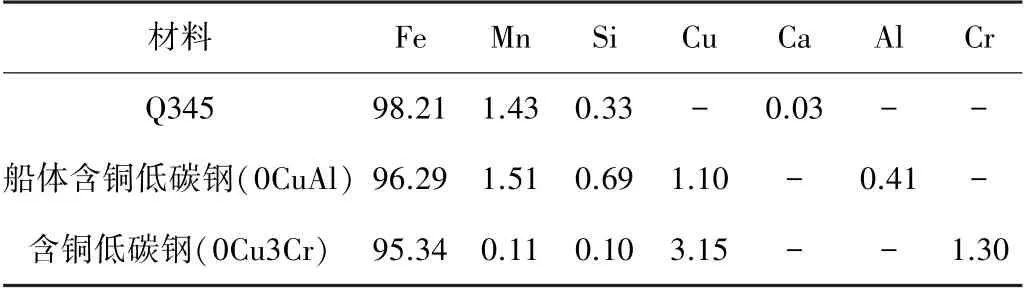
表1 3 种材料的化学成分(质量分数) %Table 1 Chemical compositions of three materials (mass fraction) %
1.2 电化学试验
1.2.1 电解质溶液的配制
为探究3 种材料在不同pH 值条件下的腐蚀规律,用为10%(质量分数,下同)HCl 溶液和6%的NaOH 溶液将3.5%NaCl 溶液的pH 值分别调整至3、6、8、12。
1.2.2 测试方法
电化学测试采用三电极体系(如图1 所示),参比电极使用232 型饱和甘汞电极(SCE),铂电极(铂片尺寸为10 mm ×20 mm)为辅助对电极,Q345 低碳钢、0CuAl 及0Cu3Cr 分别作为工作电极,工作电极和参比电极之间采用盐桥连接,采用GAMRY1000E 电化学工作站测试钢材的开路电位(OCP)、交流阻抗(EIS)及动电位极化曲线,交流阻抗测试在自腐蚀电位下进行,动电位极化曲线测试扫描速度为2 mV/s,扫描范围为-2~2 V;交流阻抗测试频率范围为1.0×(10-2~105)Hz,交流激励信号幅值为10 mV;循环阳极极化试验扫描速度为2 mV/s,起始电位为-0.5 V,回扫电位为0 V。对浸泡在pH 值分别为3、6、8、12 的3.5%NaCl 溶液中的Q345、0Cu3Cr、0CuAl 依次进行粗磨、细磨、抛光,再用2%~4%(体积分数)硝酸酒精溶液对试样进行腐蚀,最后采用MEF-4M 型金相显微镜观察试样的蚀坑大小、数量、形貌。
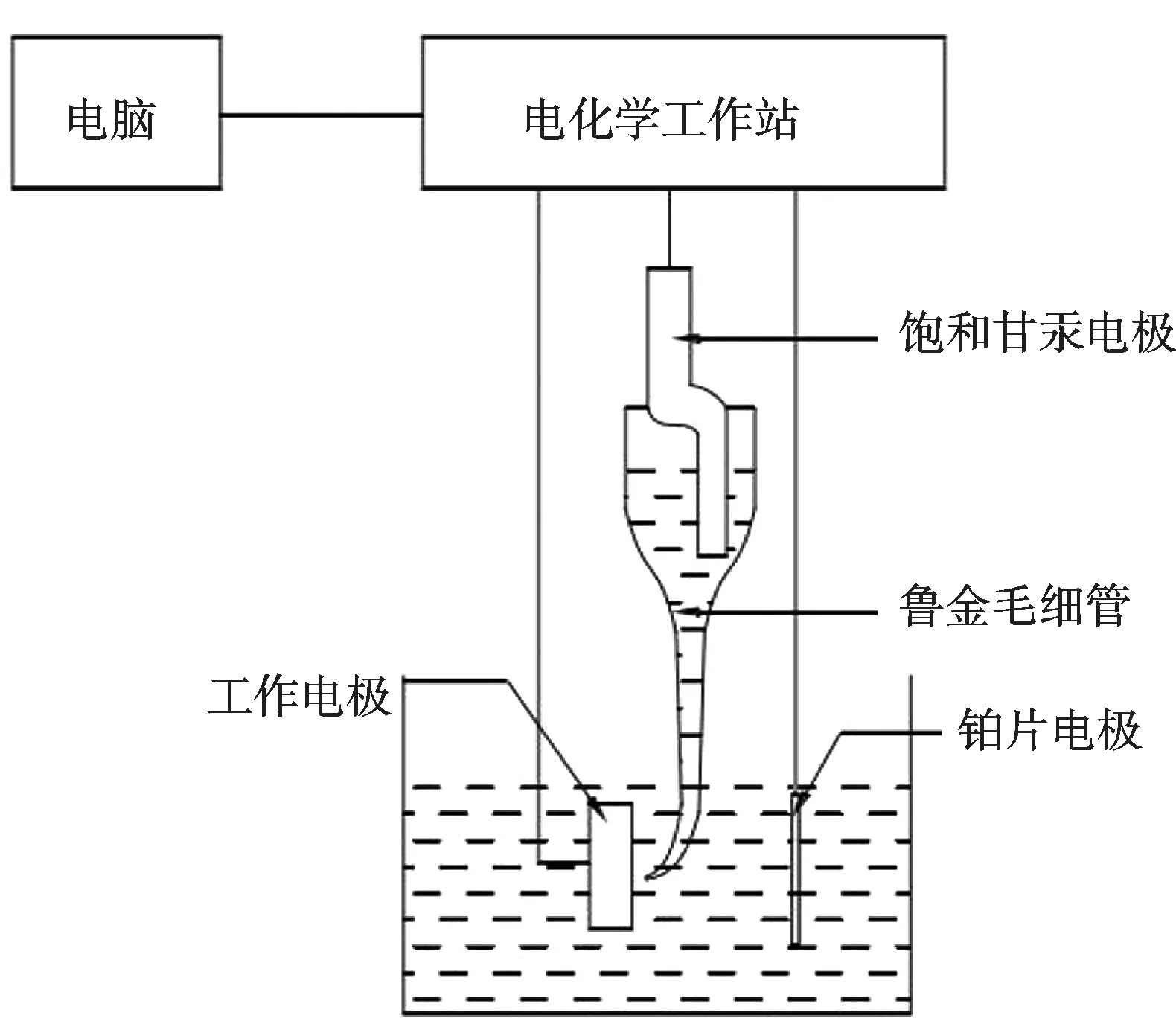
图1 电化学测试系统和试样封装示意图Fig.1 Schematic diagram of electrochemical test system and sample packaging
2 结果与分析
2.1 极化曲线分析
图2 为试样在pH 值为3、6、8、12 的NaCl 溶液中经电化学动电位测试后获得的Tafel 拟合曲线。3 种试样在pH=12 的NaCl 环境中的极化曲线均右移,可见在pH=12 时试样的自腐蚀电位较大。一般来说,自腐蚀电位越大,材料的耐蚀性能越好[21-23],这说明在pH=12 的NaCl 环境中试样的耐蚀性能较好,3 种试样在碱性环境中的耐蚀性能均优于在酸性环境中的;但Q345和0Cu3Cr 在pH=6 环境中的自腐蚀电位略大于pH=8环境中的,而0CuAl 在pH =6 环境中的自腐蚀电位明显小于在pH =8 环境中的,说明Q345 和0Cu3Cr 在pH=6时相对pH=8 时更耐蚀,而0CuAl 在pH =8 时相对更耐蚀。
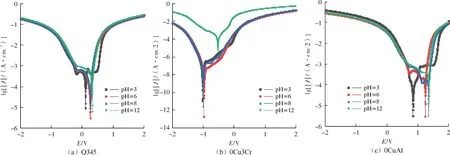
图2 试样在不同pH 值条件下的Tafel 拟合曲线Fig.2 Tafel fitting curves of samples under different pH conditions
对极化曲线采用四点法进行拟合,得到试样在不同环境中的自腐蚀电流密度(Jcorr)、阴极极化曲线的Tafel 斜率(βc)、阳极极化曲线的Tafel 斜率(βa),结果见表2,对拟合结果作图得到图3。一般来说,自腐蚀电流密度越大,材料的耐蚀性越差[24],βc和βa的值可以体现出试样在阴阳极反应的情况。由表2 可知,Q345和0CuAl 在pH=3 的NaCl 环境中的Jcorr值最大,在pH=8 的NaCl 环境中的Jcorr值最小,由此可见Q345 和0CuAl 适合在pH=8 的NaCl 环境中使用,而0Cu3Cr 在pH=12 的NaCl 环境中的Jcorr值最大,在pH=6 的NaCl环境中的Jcorr值最小,说明0Cu3Cr 适合在pH =6 的NaCl 环境中使用。通过观察表2 中3 种试验钢的Tafel曲线的斜率可发现,Q345 在4 种环境中的βc均大于βa,这说明Q345 的腐蚀过程受阴极反应控制,阴极上发生析氢反应[25];而0Cu3Cr 和0CuAl 在4 种环境中的βa均大于βc,说明0Cu3Cr 和0CuAl 在腐蚀的过程中受阳极溶解反应控制[26],这是因为这2 种钢中都含有Cu,Cu 会在阳极表面生成不易溶解的氧化物(CuFeO2),从而阻碍阳极反应,进而降低阳极反应速率。当溶液的pH 值在6 ~8 之间时,有利于形成较为致密的Cu 氧化层,阻挡了腐蚀性离子的扩散,从而使腐蚀速率降低。
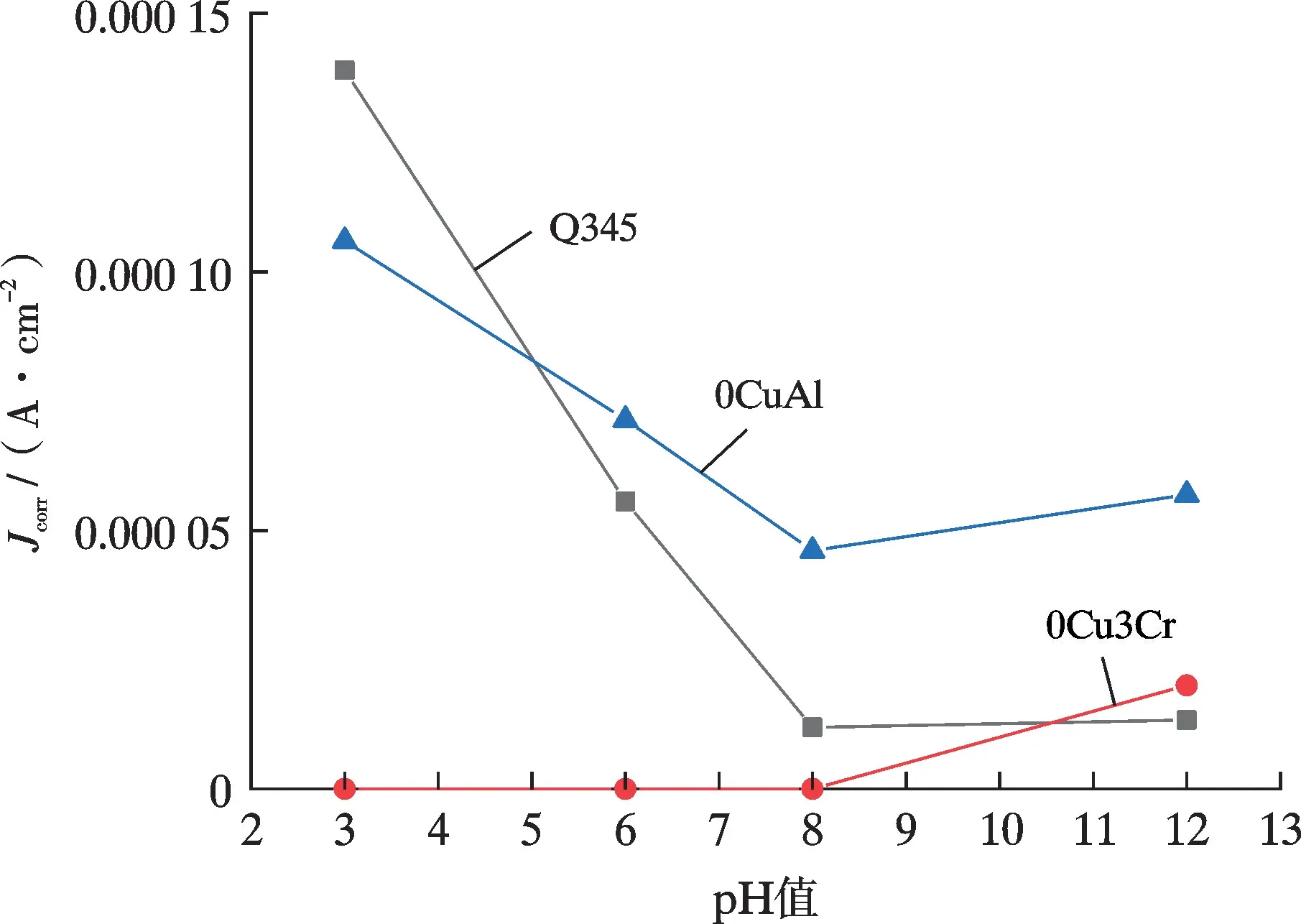
图3 试样在不同pH 值条件下的腐蚀电流密度曲线Fig.3 Corrosion current density curves of samples under different pH conditions
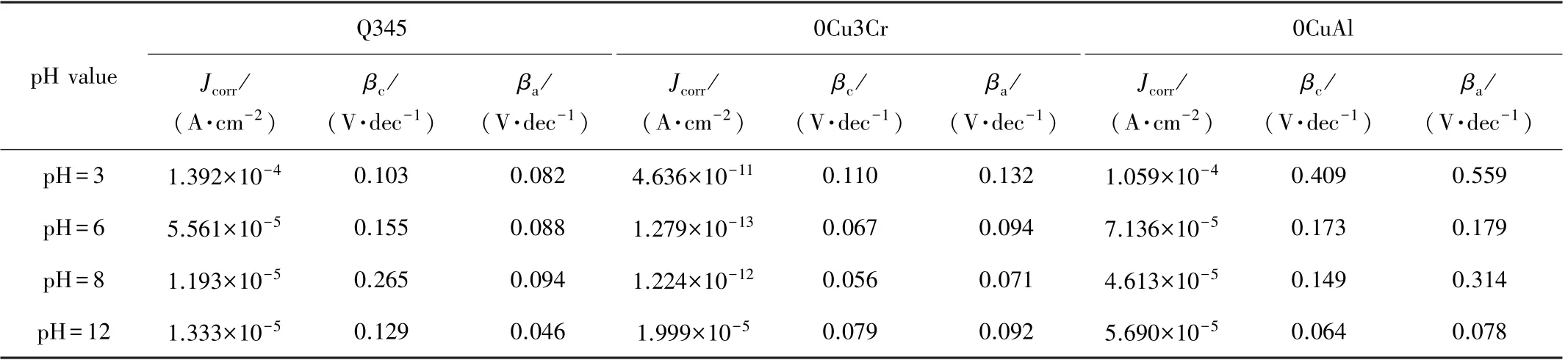
表2 试样在不同pH 值条件下的腐蚀参数Table 2 Corrosion parameters of samples under different pH conditions
2.2 阻抗分析
图4 是3 种试样在pH 值为3、6、8、12 的NaCl 溶液中测得的电化学交流阻抗谱。由图4 可以看出,3 种钢的阻抗谱均为半圆形,说明3 种试样均具有电容特性。由图4 可以看出,3 种试样在pH =12 时的阻抗模值均最大,说明在pH =12 时3 种试样的耐蚀性均较优,在pH=3 时3 种试样的阻抗模值均为最小,说明3种试样在pH=3 时耐蚀性较差,这可能是因为pH =12时试样表面形成了较稳定的钝化膜,腐蚀进行得较慢,而在pH =3 时,H+促进阴极反应,令腐蚀更易发生,使材料的耐蚀性较差。
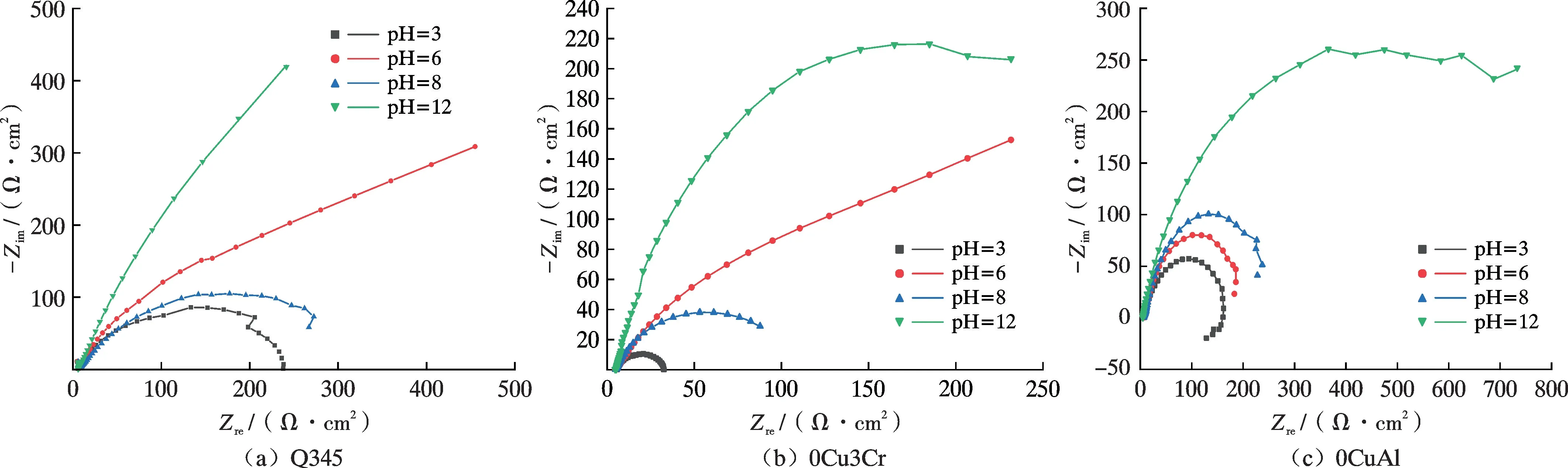
图4 试样在不同pH 值条件下的Nyquist 谱Fig.4 Nyquist spectra of samples under different pH conditions
试样在不同pH 值条件下的Bode 谱见图5。在Bode 谱的f-|Z|曲线中,低频阻抗值对应腐蚀产物层,高频阻抗值对应钝化膜。如图5 所示,pH =12 时,f-|Z|曲线中Q345、0Cu3Cr、0CuAl 的低频阻抗值均相对较大;pH =3 时,f- |Z|曲线中Q345、0Cu3Cr、0CuAl的低频阻抗值均相对较小;pH =8 时,f- |Z|曲线中0CuAl 的低频阻抗值相对较大;pH =6 时,f-|Z|曲线中0Cu3Cr 的低频阻抗值相对较大。结果表明,在pH =12时的锈层致密,腐蚀离子难以渗透,在高频条件下的阻抗值也相对较大,说明在此环境中钝化膜的破坏难度较大。因此,在pH =12 时3 种材料的耐腐蚀性最好。pH=8 时,0CuAl 的低频阻抗值高于其在pH =6 时的,证明了0CuAl 在pH=8 下的耐腐蚀性较好。pH=6 时,0Cu3Cr 的低频阻抗值高于其在pH =8 时的,所以0Cu3Cr 在pH=6 条件下的耐腐蚀性较好
利用ZView 软件对阻抗数据进行拟合。图6 为拟合电路图,Rs和Rp分别代表溶液电阻和电荷转移电阻。试样在不同pH 值条件下的阻抗拟合结果见表3。一般来说,在腐蚀进行的过程中,电荷转移电阻越大,阻碍电荷转移的能力越强,腐蚀进行得越缓慢[27,28]。
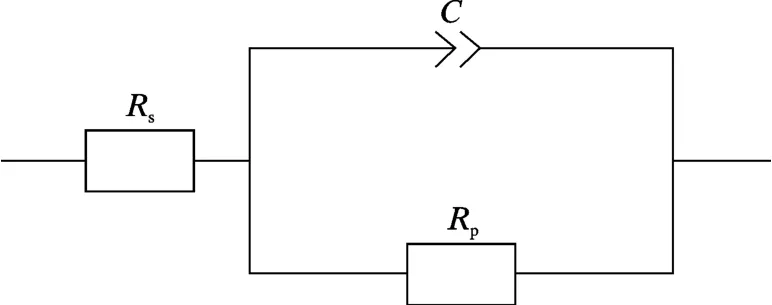
图6 拟合电路图Fig.6 Fitting circuit diagram
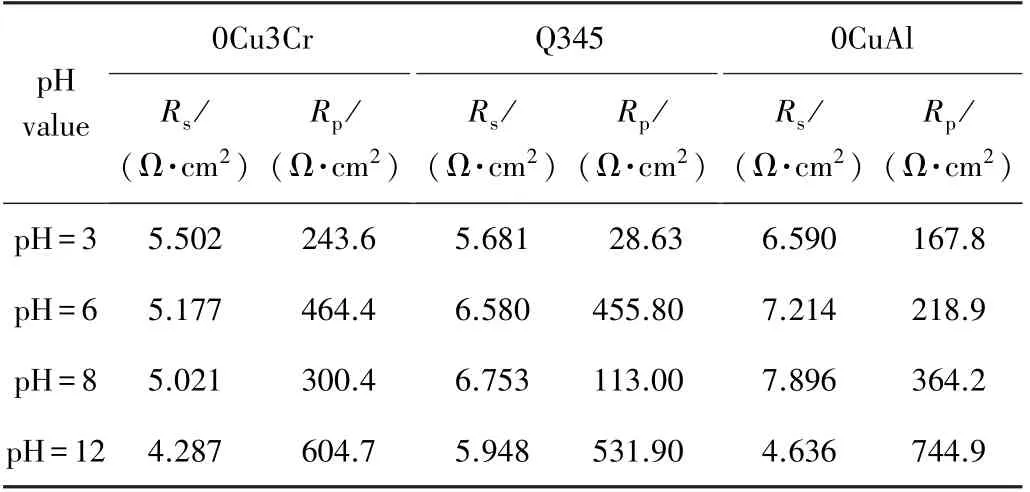
表3 样在不同pH 值条件下的阻抗拟合结果Table 3 Impedance fitting results of samples under different pHconditions
图7 为试样的电荷转移电阻随pH 值的变化趋势。由图7 可知,3 种试样在pH =12 时的耐蚀性均最优异,但0Cu3Cr 和Q345 更适合服役于pH=6 的环境中,0CuAl 更适合服役于pH =8 的环境中,由表3 可知,在pH=6 的NaCl 环境中0Cu3Cr 的电荷转移电阻高于Q345 的,由此可见0Cu3Cr 在pH=6 的环境中更耐蚀。
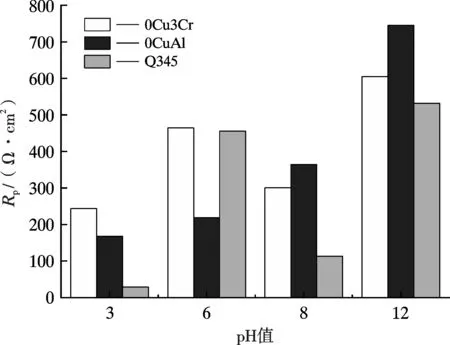
图7 试样的电荷转移电阻随pH 值的变化趋势Fig.7 Change trend of charge transfer resistance of the samples with pH value
由电化学测试结果可得出,0Cu3Cr 更适合在pH=6的环境中应用,0CuAl 更适合在pH=8 的环境中应用。
2.3 金相分析
图8 为电化学腐蚀后试样表面的金相形貌。分析图8 发现,在pH=3 的NaCl 环境中,3 种试样表面出现数量较多的点蚀坑,可见在此环境中3 种试样的腐蚀较为严重,但相对而言在此环境中0Cu3Cr 的点蚀坑数量较少。在pH=12 的NaCl 环境中,3 种试样表面点蚀坑的数量明显减少,基体表面受侵蚀的情况并不严重,可见3 种试样在碱性环境中的耐蚀性更优异。对比0Cu3Cr在不同环境中的金相形貌发现,pH =6 时0Cu3Cr 表面的点蚀坑较小且数量较少,而pH =8 时0Cu3Cr 表面的点蚀坑较大且数量较多。在pH =8 的NaCl 环境中,0CuAl 的耐蚀性较好,这与电化学测试所得结论相同。
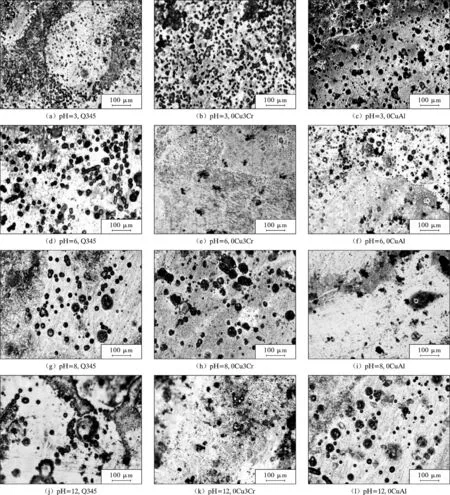
图8 电化学腐蚀后试样表面的金相形貌Fig.8 Metallographic morphology of surfaces of samples after electrochemical corrosion
3 结 论
(1)在NaCl 环境中,3 种试样在碱性环境中的耐蚀性能均优于在酸性环境中的。Q345 在不同pH 值条件下的腐蚀过程中的βc均大于βa,说明Q345 受阴极反应控制;而0Cu3Cr 和0CuAl 在不同pH 值条件下的腐蚀过程中的βa均大于βc,说明0Cu3Cr 和0CuAl 受阳极溶解反应控制,Cu 元素促使钢表面形成致密、不易溶解的氧化膜(CuFeO2),从而提高了钢材的耐蚀性。
(2)电化学试验结果表明,在NaCl 环境中,0Cu3Cr更适合在pH=6 条件下应用,0CuAl 更适合在pH=8 条件下应用,3 种试样在pH=12 条件下的耐蚀性均较好。

