地卷柏的化学成分及其α-葡萄糖苷酶抑制活性研究
姜红宇,吕敬崑,邵金华,陈小明,*
1湖南科技学院化学与生物工程学院;2湖南省银杏工程技术研究中心;3湖南恒伟药业股份有限公司,永州 425100
地卷柏(SelaginellaprostrataH.S.Kung)系卷柏科卷柏属多年生草本植物,常生于海拔1 500~2 500 m的石缝中或林下苔藓石上,在贵州、云南和四川等省份均有分布。地卷柏全草可供药用,将其烘干或烧成炭后研末与茶油调和,外敷可用于止血;炖酒内服,可治损伤、闭经血瘀等症。此外,地卷柏还具有较高的观赏价值,可供栽培观赏[1,2]。
卷柏属植物种类繁多、资源丰富,全世界约有700种,主产于热带地区。其中,我国约有70余种,且广泛分布于全国各地,兖州卷柏、江南卷柏等20余种植物作为民间传统用药已被广泛应用[3-5]。作为官方用药的有卷柏和垫状卷柏,两者均被收录于2020年版《中华人民共和国药典》,具有化瘀止血、活血通经的功效,可用于跌扑损伤、经闭痛经、吐血以及崩漏等疾病的治疗[6-8]。现代研究表明,卷柏属植物含有黄酮类、木脂素类、炔酚类和萜类等多种化学成分,具有降血糖、抗氧化、抗衰老、抗肿瘤、抗炎以及抗菌等作用[9-14]。目前,国内外对卷柏属植物的研究主要集中在卷柏、中华卷柏和江南卷柏等几种植物上,对该属其他植物的研究较少[15,16]。地卷柏隶属卷柏属植物,迄今为止有关其化学成分以及药理活性的研究尚未见有文献报道。为了进一步阐明和发掘地卷柏的药用价值和活性物质基础,本文对地卷柏的95%乙醇提取物进行化学成分研究,并对分离获得的化合物进行体外酶抑制活性评价,以期为地卷柏植物资源的合理开发利用奠定科学基础。
1 材料与方法
1.1 试剂与仪器
Bruker 400 MHz和600 MHz核磁共振谱仪(德国Bruker公司);Agilent 6545 Q-TOF液质联用仪,Cary 3500紫外可见分光光度计(美国安捷伦公司);Tensor 37傅里叶变换红外光谱仪(布鲁克光谱仪器公司);ELX-800酶标仪(美国宝特公司);依利特P3700半制备液相色谱仪(大连依利特分析仪器有限公司);200~300目柱层析硅胶及硅胶GF254薄层板(青岛海洋化工有限公司);RP-18反相柱色谱硅胶和YMC-Pack Pro C18色谱柱:5 μm,250 mm × 10 mm(日本YMC公司);Sephadex LH-20葡聚糖凝胶(德国Merck公司);色谱乙腈、甲醇(美国Tedia公司);水为实验室自制超纯水;二氯甲烷、甲醇等分析纯试剂均为西陇化工股份有限公司产品;α-葡萄糖苷酶(美国Sigma公司,批号:SLBT8587)、4-硝基苯基-β-D-吡喃葡萄糖苷(纯度≥98.0%,上海源叶生物科技有限公司,批号K22J9B64113);阿卡波糖(纯度≥98.0%,上海源叶生物科技有限公司,批号S25M11X109783)。
1.2 植物材料
地卷柏于2021年7月在中国云南省彝良县采集,经湖南科技学院姜红宇副教授鉴定为卷柏科卷柏属植物地卷柏(SelaginellaprostrataH.S.Kung)的全草,植物样品标本(2021-PS-0701)存放于湖南省银杏工程技术研究中心。
1.3 实验方法
1.3.1 提取与分离
取地卷柏的干燥全草10 kg,粉碎后用95%乙醇加热回流提取3次,每次3 h,合并提取液浓缩得到粗浸膏1.2 kg。粗浸膏用水混悬后,依次用二氯甲烷、乙酸乙酯和正丁醇进行萃取,浓缩萃取液分别得到二氯甲烷部位148 g、乙酸乙酯部位426 g、正丁醇部位220 g和水部位406 g。
乙酸乙酯萃取部位经硅胶柱色谱分离,二氯甲烷:甲醇(100∶1→5∶1)梯度洗脱,得到9个流分(E1~E9)。其中,流分E3经Sephadex LH-20凝胶柱(甲醇)分离,得到6个亚流分E3.1~E3.6。亚流分E3.3经薄层制备和半制备型HPLC(甲醇:水,30:70,2 mL/min)分离得到化合物1(tR=36.2 min,10.4 mg)和4(tR=9.9 min,6.7 mg)。亚流分E3.4经硅胶柱分离,二氯甲烷:甲醇(80∶1→3∶1)梯度洗脱得到化合物2(8.0 mg)和3(4.5 mg)。流分E4经ODS柱分离,甲醇:水(20∶80→100∶0)梯度洗脱,得到7个亚流分E4.1~E4.7。亚流分E4.2经Sephadex LH-20凝胶柱(甲醇)得到化合物7(10.3 mg)。亚流分E4.3经Sephadex LH-20凝胶柱(甲醇)和半制备HPLC(乙腈∶水,25∶75,2 mL/min)分离得到化合物5(tR=37.3 min,15.7 mg)和6(tR=45.8 min,9.2 mg)。流分E6经反复硅胶柱色谱和凝胶柱色谱等手段分离纯化,得到化合物8(19.8 mg)、9(24.6 mg)和10(15.9 mg)。
1.3.2α-葡萄糖苷酶体外抑制活性测试
参照文献方法[17],以阿卡波糖为阳性对照,准确依次移取50 μL的磷酸盐缓冲液(pH=6.8)、20 μL不同浓度的待测样品溶液(终质量浓度为0.2、0.1、0.05、0.025 mg/mL)、10 μL的α-葡萄糖苷酶溶液(1 U/mL)和20 μL对硝基苯基-α-D-吡喃葡萄糖苷溶液(2.5 mmol/L)置于96孔板中,并在37 ℃条件下孵育15 min,然后加入150 μL的Na2CO3溶液终止反应。用酶标仪在405 nm处测定吸光度(A),设定样品组和空白组,平行操作3次,取平均值。按公式计算抑制率:抑制率=[1-(A样品-A样品空白)/A空白]×100%。
2 结果
2.1 结构鉴定
化合物1无色油状液体;(+)-HR-EI-MS:m/z275.161 8[M+Na]+(calcd for C15H24O3Na,275.161 8),确定其分子式为C15H24O3,不饱和度为4;IR(KBr)νmax3 342、2 931、2 875、1 626、1 568、1 412、1 332、1 131、1 045、1 015、886 cm-1,上述特征吸收峰提示化合物结构中可能存在羟基和碳碳双键官能团;化合物1的1H NMR谱(见表1)显示存在2个烯氢信号δH5.65(1H,m)、5.32(1H,br s),2个连氧次甲基信号δH5.12(1H,br s)、3.96(1H,m),1个连氧亚甲基信号δH4.15(1H,br s)、4.13(1H,br s),2个亚甲基信号δH2.21(1H,ddd,J=12.4,4.4,2.0 Hz)、1.84(1H,ddd,J=12.4,4.4,2.0 Hz)、1.54(1H,overlapped)、1.21(1H,overlapped)和4个甲基信号δH1.59(3H,s)、1.44(3H,s)、1.21(3H,s)、1.15(3H,s);13C NMR谱(见表1)显示该化合物共有15个碳信号,结合DEPT 135和HSQC谱可归属为4个烯烃碳信号(δC154.4、138.3、128.0、121.2),2个连氧次甲基碳信号(δC89.5、66.2),3个亚甲基碳信号(δC59.3、51.0、50.8),4个甲基碳信号(δC31.2、27.5、27.3、12.0)和2个季碳信号(δC89.3、34.2),上述数据表明化合物1可能为倍半萜类化合物。通过比较核磁数据发现,化合物1和文献[18,19]报道的已知倍半萜类化合物(3S,5R,8S)-5,8-epoxy-6-megastigmadien-3,9-diol具有相似的母核结构,两者结构上的主要差异在于C-8位所连的侧链基团不同。采用2D NMR实验对化合物1的结构进行确证,在1H-1H COSY谱中H-3/H-2、H-3/H-4、H-7/H-8、H-10/H-11之间的相关信号表明存在CH2-CH-CH2、CH-CH、CH-CH2结构单元(见图1)。
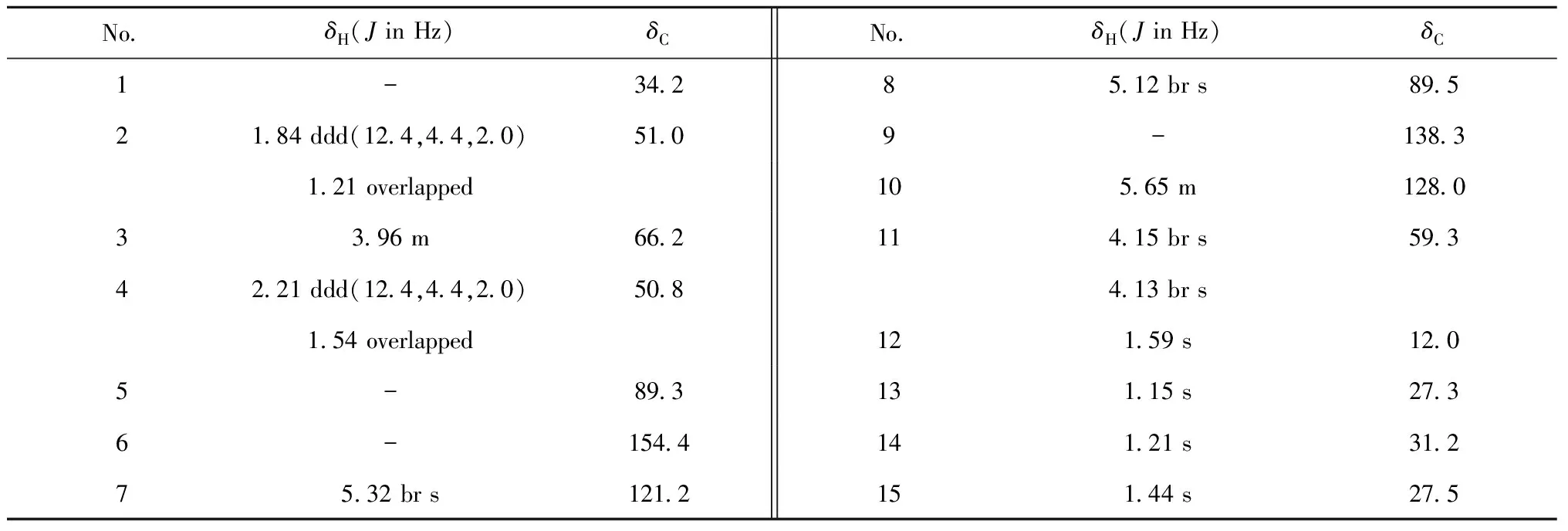
表1 化合物1的氢谱和碳谱数据(400和100 MHz,CD3OD)
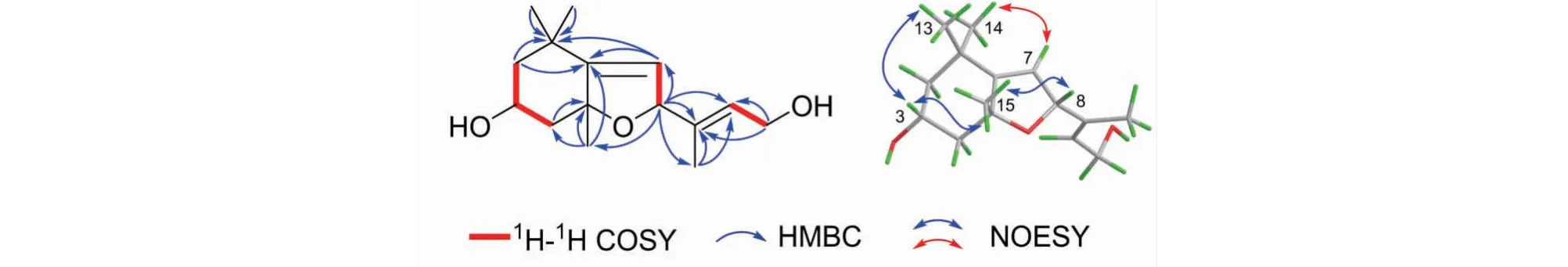
图1 化合物1的主要1H-1H COSY、HMBC和NOESY相关
结合HMBC谱中H-11、H3-12与C-9、C-10相关;H-7与C-1、C-6相关;H-8与C-7、C-9、C-10、C-12、C-15等相关信号可以确定化合物1的平面结构,其主要的2D NMR相关信号如图1所示。化合物1的相对构型是通过NOESY谱来确定的,H3-13/H-3、H-3/H3-15、H3-15/H-8之间的NOESY相关信号表明H-3、H-8、Me-13和Me-15位于环系的同侧,将其定为β构型(见图1)。由于在NOESY谱中未观察到H3-12与H-10之间明显的相关信号,可以确定C9处的碳碳双键构型为E。Uehelhart等[20]曾报道:该类型倍半萜C-8位的立体构型为R时,在ECD谱中于210 nm左右可以观察到明显的正Cotton效应,反之当C-8的立体构型为S时,于210 nm左右可以观察到明显的负Cotton效应。在化合物1的实测圆二色谱图中(见图2),于208 nm处观察到正的Cotton效应,因此初步确定C-8的立体构型为R。为了进一步确定化合物1的绝对构型,采用GAUSSIAN 09程序在B3LYP/6-311 G(d,p)基组水平上使用TD-DFT方法对该化合物的ECD光谱进行了计算。通过比较发现,化合物1的实验ECD光谱与3R,5R,8R构型的计算ECD光谱吻合(见图2),由此确定化合物1的绝对构型为3R,5R,8R。经SciFinder检索,确定化合物1为新的倍半萜类化合物(见图3),并将其命名为seprostrataoid A。化合物1的详细结构鉴定数据原始图谱可从本刊官网免费下载(www.trcw.ac.cn)。
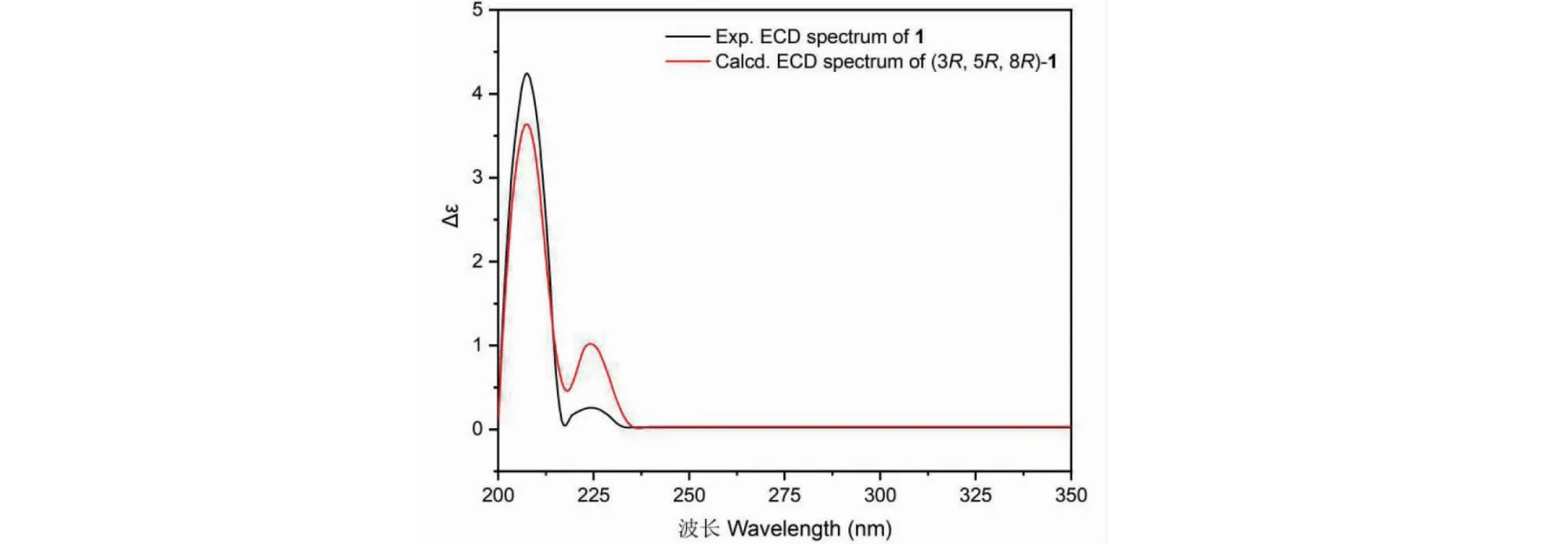
图2 化合物1的实验和计算ECD谱图
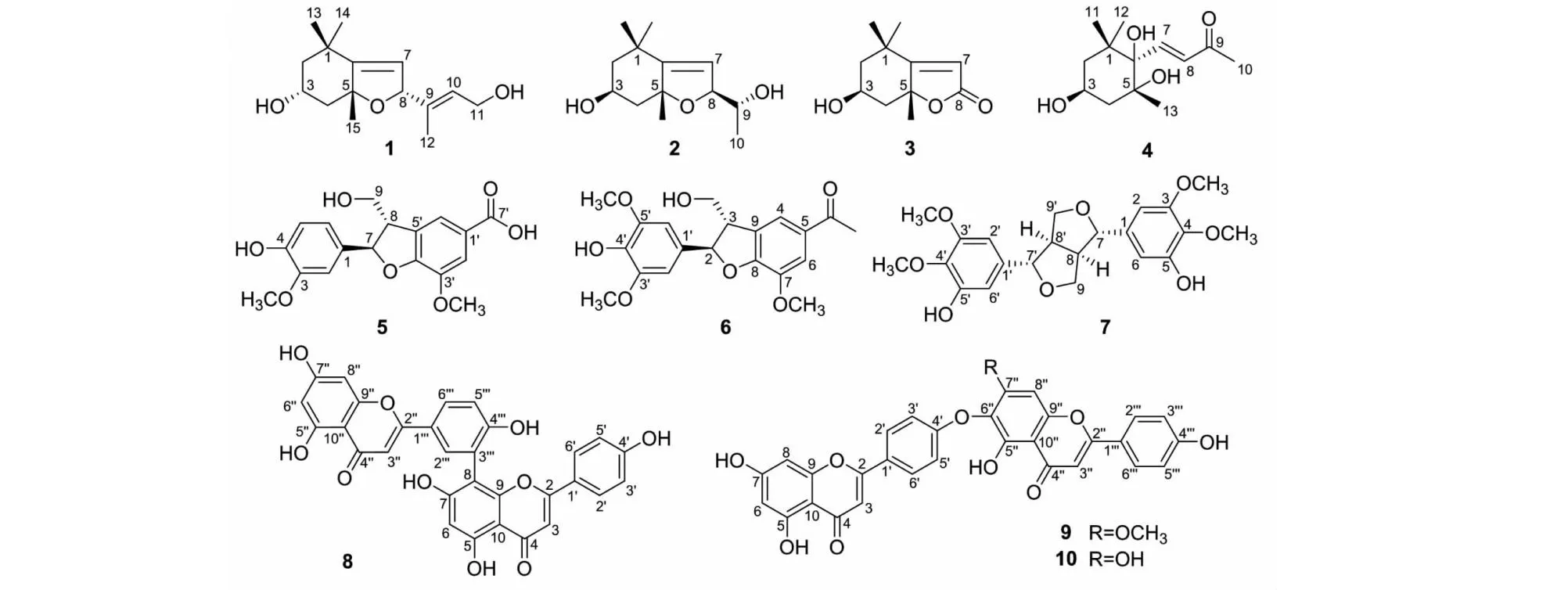
图3 化合物1~10的化学结构
化合物2无色油状物;HR-EI-MS:m/z227.165 0[M+H]+(calcd for C13H23O3,227.164 2);1H NMR(400 MHz,CD3OD)δ:5.75(1H,s,H-7),4.75(1H,br d,J=7.2 Hz,H-8),4.50(1H,m,H-3),3.92(1H,m,H-9),2.60(1H,br d,J=14.0 Hz,H-4b),2.04(1H,br d,J=14.0 Hz,H-2b),1.99(1H,dd,J=13.6,3.2 Hz,H-4a),1.93(3H,s,H-13),1.50(1H,dd,J=13.6,3.2 Hz,H-2a),1.42(3H,d,J=6.6 Hz,H-10),1.40(3H,s,H-11),1.12(3H,s,H-12);13C NMR(100 MHz,CD3OD)δ:34.2(C-1),51.1(C-2),66.4(C-3),51.0(C-4),89.4(C-5),154.5(C-6),119.8(C-7),88.4(C-8),71.2(C-9),19.0(C-10),27.5(C-11),31.2(C-12),27.4(C-13)。以上数据与文献[18,19]报道基本一致,故鉴定化合物2为(3S,5R,8S)-5,8-epoxy-6-megastigmadien-3,9-diol。
化合物3白色粉末;HR-EI-MS:m/z197.116 9[M+H]+(calcd for C11H17O3,197.117 2);1H NMR(400 MHz,CD3OD)δ:5.74(1H,s,H-7),4.22(1H,m,H-3),2.44(1H,ddd,J=13.2,2.8,2.4 Hz,H-4b),1.96(1H,ddd,J=14.4,2.8,2.4 Hz,H-2b),1.78(3H,s,H-11),1.76(1H,dd,J=13.2,4.0 Hz,H-4a),1.55(1H,dd,J=14.4,3.6 Hz,H-2a),1.46(3H,s,H-10),1.32(3H,s,H-9);13C NMR(100 MHz,CD3OD)δ:37.4(C-1),48.0(C-2),67.5(C-3),46.5(C-4),89.2(C-5),185.9(C-6),113.7(C-7),174.5(C-8),31.5(C-9),27.0(C-10),27.4(C-11)。以上数据与文献[21]报道基本一致,故鉴定化合物3为(-)-黑麦草内酯。
化合物4白色粉末;HR-EI-MS:m/z243.159 9[M+H]+(calcd for C13H23O4,243.159 1);1H NMR(600 MHz,CD3OD)δ:7.40(1H,d,J=16.2 Hz,H-7),6.38(1H,d,J=16.2 Hz,H-8),4.09(1H,m,H-3),2.30(3H,s,H-10),1.80(1H,m,H-4β),1.72(1H,m,H-4α),1.68(1H,t,J=12.0 Hz,H-2β),1.25(3H,s,H-11),1.12(1H,m,H-2α),1.12(3H,s,H-13),0.85(3H,s,H-12);13C NMR(150 MHz,CD3OD)δ:41.2(C-1),46.2(C-2),65.0(C-3),45.5(C-4),77.7(C-5),80.0(C-6),132.2(C-7),152.8(C-8),201.2(C-9),26.4(C-10),27.5(C-11),26.9(C-12),27.2(C-13)。以上数据与文献[22]报道基本一致,故鉴定化合物4为(3S,5R,6R,7E)-3,5,6-三羟基-7-巨豆烯-9-酮。
化合物5白色粉末;HR-EI-MS:m/z347.113 8[M+H]+(calcd for C18H19O7,347.112 5);1H NMR(400 MHz,CD3OD)δ:7.65(1H,br s,H-6′),7.57(1H,br s,H-2′),6.98(1H,br s,H-2),6.86(1H,br s,H-6),6.79(1H,br s,H-5),5.62(1H,d,J= 6.0 Hz,H-7),3.90(3H,s,3′-OCH3),3.82(2H,m,H-9),3.81(3H,s,3-OCH3),3.58(1H,m,H-8);13C NMR(100 MHz,CD3OD)δ:124.1(C-1′),114.0(C-2′),143.9(C-3′),55.3(3′-OCH3),152.5(C-4′),129.0(C-5′),119.5(C-6′),169.0(C-7′),132.8(C-1),109.3(C-2),147.6(C-3),55.0(3-OCH3),146.5(C-4),114.8(C-5),118.5(C-6),88.7(C-7),53.1(C-8),63.3(C-9)。以上数据与文献[23,24]报道基本一致,故鉴定化合物5为(7R,8S)-ceplignan。
化合物6淡黄色油状物;HR-EI-MS:m/z397.125 8[M+Na]+(calcd for C20H22O7Na,397.125 8);1H NMR(400 MHz,(CD3)2CO)δ:7.62(1H,br s,H-4),7.52(1H,br s,H-6),6.74(2H,s,H-2′,H-6′),5.64(1H,d,J=7.2 Hz,H-2),3.93(2H,m,CH2OH),3.90(3H,s,7-OCH3),3.80(6H,s,3′-OCH3,5′-OCH3),3.66(1H,m,H-3),2.50(3H,s,COCH3);13C NMR(100 MHz,Acetone-d6)δ:89.6(C-2),53.8(C-3),119.6(C-4),130.2(C-5),113.0(C-6),144.8(C-7),153.4(C-8),132.0(C-9),132.2(C-1′),104.2(C-2′,C-6′),148.6(C-3′,C-5′),136.0(C-4′),197.1(COCH3),26.4(COCH3),63.7(CH2OH),56.5(3′-OCH3,5′-OCH3),56.2(7-OCH3)。以上数据与文献[25]报道基本一致,故鉴定化合物6为(2R,3S)-二氢-2-(3′,5′-二甲氧基-4′-羟基苯基)-3-羟甲基-7-甲氧基-5-乙酰基苯骈呋喃。
化合物7淡黄色粉末;HR-EI-MS:m/z441.153 5[M+Na]+(calcd for C22H26O8Na,441.152 0);1H NMR(600 MHz,CDCl3)δ:7.24(2H,d,J=1.8 Hz,H-6,H-6′),7.16(2H,d,J=1.8 Hz,H-2,H-2′),4.75(2H,d,J=4.2 Hz,H-7,H-7′),4.27(2H,dd,J=9.0,7.2 Hz,H-9a,H-9′a),3.98(6H,s,3-OCH3,3′-OCH3),3.92(6H,s,4-OCH3,4′-OCH3),3.88(2H,dd,J=9.0,4.2 Hz,H-9b,H-9′b),3.12(2H,t,J=4.2 Hz,H-8,H-8′);13C NMR(150 MHz,CDCl3)δ:132.9(C-1,C-1′),103.8(C-2,C-2′),152.5(C-3,C-3′),146.3(C-4,C-4′),149.1(C-5,C-5′),109.1(C-6,C-6′),86.1(C-7,C-7′),54.4(C-8,C-8′),71.9(C-9,C-9′),56.3(3-OCH3,3′-OCH3),61.2(4-OCH3,4′-OCH3)。以上数据与文献[26]报道基本一致,故鉴定化合物7为5,5′-二甲氧基木香酚 A。
化合物8黄色粉末;HR-EI-MS:m/z539.098 8[M+H]+(calcd for C30H19O10,539.097 3);1H NMR(400 MHz,DMSO-d6)δ:8.10(1H,d,J=2.4 Hz,H-2′′′),8.05(1H,dd,J=8.4,2.4 Hz,H-6′′′),7.65(2H,d,J=8.4 Hz,H-2′,H-6′),7.25(1H,d,J=8.4 Hz,H-5′′′),6.86(2H,d,J=8.4 Hz,H-3′,H-5′),6.76(1H,s,H-3″),6.68(1H,s,H-3),6.57(1H,d,J=2.4 Hz,H-8″),6.48(1H,s,H-6),6.25(1H,d,J=2.4 Hz,H-6″);13C NMR(100 MHz,DMSO-d6)δ:164.2(C-2),103.0(C-3),182.1(C-4),162.9(C-5),99.2(C-6),160.6(C-7),104.5(C-8),160.0(C-9),103.8(C-10),121.5(C-1′),128.4(C-2′,C-6′),115.8(C-3′,C-5′),161.1(C-4′),163.8(C-2″),103.0(C-3″),181.7(C-4″),161.5(C-5″),98.8(C-6″),164.0(C-7″),94.2(C-8″),159.7(C-9″),103.8(C-10″),121.7(C-1′′′),131.3(C-2′′′),121.0(C-3′′′),161.3(C-4′′′),120.4(C-5′′′),128.2(C-6′′′)。以上数据与文献[27]报道基本一致,故鉴定化合物8为穗花衫双黄酮。
化合物9土黄色粉末;HR-EI-MS:m/z553.112 2[M+H]+(calcd for C31H21O10,553.112 9);1H NMR(400 MHz,DMSO-d6)δ:13.10(1H,s,5-OH),12.90(1H,s,5″-OH),10.85(1H,s,7-OH),10.42(1H,s,4″′-OH),8.02(2H,d,J=8.4 Hz,H-2′,H-6′),8.00(2H,d,J=8.4 Hz,H-2′′′,H-6′′′),7.12(1H,s,H-8″),7.04(2H,d,J=8.4 Hz,H-3′,H-5′),6.97(2H,d,J=8.4 Hz,H-3′′′,H-5′′′),6.94(1H,s,H-3),6.88(1H,br s,H-3″),6.50(1H,d,J=2.0 Hz,H-8),6.20(1H,d,J=2.0 Hz,H-6),3.90(3H,s,7″-OCH3);13C NMR(100 MHz,DMSO-d6)δ:164.3(C-2),103.8(C-3),181.8(C-4),161.5(C-5),98.8(C-6),164.2(C-7),94.0(C-8),157.2(C-9),103.8(C-10),124.2(C-1′),128.5(C-2′,C-6′),115.2(C-3′,C-5′),160.4(C-4′),163.2(C-2″),102.9(C-3″),182.2(C-4″),152.5(C-5″),124.8(C-6″),158.1(C-7″),92.0(C-8″),154.1(C-9″),104.0(C-10″),121.0(C-1″′),128.5(C-2″′,C-6″′),116.0(C-3″′,C-5″′),161.5(C-4″′),56.8(7″-OCH3)。以上数据与文献[28]报道基本一致,故鉴定化合物9为异柳杉双黄酮。
化合物10土黄色粉末;HR-EI-MS:m/z539.098 4[M+H]+(calcd for C30H19O10,539.097 3);1H NMR(400 MHz,DMSO-d6)δ:8.02(2H,d,J=8.4 Hz,H-2′,H-6′),7.97(2H,d,J=8.4 Hz,H-2‴,H-6‴),7.05(2H,d,J=8.4 Hz,H-3′,H-5′),6.94(2H,d,J=8.4 Hz,H-3′,H-5′),6.88(2H,s,H-3,H-3″),6.75(1H,s,H-8″),6.50(1H,d,J=2.0 Hz,H-8),6.22(1H,d,J=2.0 Hz,H-6);13C NMR(100 MHz,DMSO-d6)δ:164.3(C-2),103.9(C-3),181.7(C-4),160.5(C-5),99.0(C-6),163.0(C-7),94.6(C-8),157.0(C-9),104.0(C-10),124.2(C-1′),128.2(C-2′,C-6′),115.4(C-3′,C-5′),161.2(C-4′),164.2(C-2″),102.7(C-3″),182.0(C-4″),153.0(C-5″),124.8(C-6″),157.5(C-7″),94.0(C-8″),153.8(C-9″),104.3(C-10″),121.0(C-1′),128.5(C-2‴,C-6‴),116.0(C-3‴,C-5‴),161.4(C-4‴)。以上数据与文献[29]报道基本一致,故鉴定化合物10为扁柏双黄酮。
化合物1~10的结构见图3。
2.2 α-葡萄糖苷酶抑制活性测试结果
α-葡萄糖苷酶抑制活性测试结果表明,化合物8具有明显的α-葡萄糖苷酶抑制活性,其IC50值为42.68±1.54 μmol/L,活性强度与阳性对照阿卡波糖(IC50=40.25±1.08 μmol/L)基本相当。化合物7、9和10表现出中等程度的α-葡萄糖苷酶抑制活性,IC50值分别为72.14±2.67、61.26±4.32、55.43±2.17 μmol/L。其他化合物对α-葡萄糖苷酶均未表现出明显的抑制活性。
3 结论
本文利用多种现代色谱分离技术和波谱学方法,对地卷柏的化学成分以及生物活性进行研究,从地卷柏全草的95%乙醇提取物中分离鉴定了10个化合物,包括4个倍半萜、3个木脂素和3个双黄酮。其中,化合物1为新的倍半萜类化合物,化合物2~10为首次从地卷柏中分离得到。采用PNPG法测试了所有化合物的α-葡萄糖苷酶抑制活性,结果显示双黄酮类化合物8~10具有较好的α-葡萄糖苷酶抑制活性,据此推测双黄酮类化合物可能是地卷柏发挥降血糖活性的重要物质基础。本文首次揭示了地卷柏中抑制α-葡萄糖苷酶的活性成分,研究结果丰富了地卷柏的化学成分,为该植物资源进一步的开发利用提供参考和科学依据。

