尖尾芋石油醚部位化学成分及其乳腺癌细胞毒活性研究
王 鹏,陈 娅,彭兰淳,郑青竹,彭江丽,2,彭求贤,3*
1湖南中医药大学药学院;2湖南省中药活性物质筛选工程技术研究中心;3湘产大宗药材品质评价湖南省重点实验室,长沙410208
天南星科海芋属植物尖尾芋Alocasiacucullata(Lour.)Schott 以其干燥根茎入药,最早记载于《广西实用中草药新选》,其味辛、微苦,性寒,有毒,归肺经,具有清热解毒,消肿镇痛的功效[1,2]。尖尾芋根茎在民间多用于高热不退、流感、钩端螺旋体病、肠伤寒、瘰疬以及肺结核;外用治疗疔疮、烫火伤、毒蛇咬伤和毒蜂蜇伤[2]。尖尾芋有毒,需久煎6 h以上方可内服,误食尖尾芋时,民间用醋加生姜汁少许共煮,内服或含漱以解毒,临床上通过肌注苯海拉明及静注葡萄糖盐水以解毒[3]。现代研究表明尖尾芋水提物、醇提物具有显著的药理活性,如抗炎[4]、抗肿瘤[5-8]及脾保护作用[9]等,但尖尾芋的药效物质基础研究比较薄弱,特别是其石油醚部位化学成分研究仅局限于GC-MS分析。因此,本文以尖尾芋石油醚部位为研究对象,采用硅胶、Sephadex LH-20等色谱方法进行分离纯化,并采用紫外光谱、一维核磁共振谱等各种波谱学技术鉴定尖尾芋石油醚部位化学成分,探究其石油醚部位药效物质基础,同时以人乳腺癌MDA-MB-231、MCF-7细胞及小鼠乳腺癌4T1细胞为筛选模型,对分离得到的单体化合物进行乳腺癌细胞毒活性研究。以期为尖尾芋的深入研究和开发利用提供依据。
1 材料与方法
1.1 仪器与材料
INOVA-600MHz核磁共振波谱仪(瑞士Bruker公司);HR-ESI-TOF-MS光谱仪(美国Agilent公司);TC-20全自动细胞计数仪(美国Bio-rad公司);Sephadex LH-20葡聚糖凝胶填料(瑞典GE Healthcare公司);GF254薄层色谱硅胶(青岛海洋化工厂分厂);石油醚、乙酸乙酯、丙酮、氯仿、乙醇及甲醇等试剂均为分析纯(湖南汇虹试剂有限公司);阳性对照品顺铂(批号:115583,MedChemexpress公司);二甲基亚砜(99%生物技术级)(批号:C14637730,上海麦克林生化科技有限公司);CCK-8试剂盒(批号:AK13974,武汉伊莱瑞特生物科技有限公司);DMEM高糖培养基、PBS磷酸缓冲液、0.25%胰蛋白酶溶液、胎牛血清(批号:WHB823G111、WH0021G221、WHAB23Z251、SA211028,武汉普诺赛生命科技有限公司)。人乳腺癌细胞MDA-MB-231、MCF-7、小鼠乳腺癌细胞4T1(武汉普诺赛生命科技有限公司)。
尖尾芋于2021年11月购于广西钦州,由湖南中医药大学刘塔斯鉴定为尖尾芋Alocasiacucullata(Lour.) Schott,凭证标本(2021113)保存于湖南中医药大学湘产大宗药材品质评价湖南省重点实验室。
1.2 实验方法
1.2.1 提取与分离
本实验称取尖尾芋根茎50 kg,粉碎,分为两份,每份各24.58 kg。70%乙醇回流提取3次,每次2 h,减压浓缩后得到密度为1.37的浸膏8.65 kg。浸膏经蒸馏水混悬后,使用石油醚萃取20次,每次2 L,最终得到石油醚部位浸膏233.0 g。
称取101.5 g尖尾芋石油醚部位浸膏,干法上样于100~200目硅胶柱进行粗分(石油醚-乙酸乙酯,50∶1→30∶1→10∶1→5∶1→2∶1→1∶1;乙酸乙酯;甲醇)。将所收集部分经薄层色谱分析后合并同类后得到9个组分,分为9段(Fr.1~Fr.9),每段粗分后均先以300~400目硅胶柱细分,再通过凝胶柱纯化(填料为Sephadex LH-20),除Fr.9的洗脱体系为氯仿-甲醇(1∶1)外,其余组分的洗脱体系均为石油醚-氯仿-甲醇(4∶5∶1)。Fr.1(3.7 g)经细分(石油醚-乙酸乙酯,50∶1)和纯化后得到化合物7(15.3 mg)。Fr.2(4.2 g)经细分(石油醚-乙酸乙酯,50∶1)和纯化后得到化合物6(7.4 mg)。Fr.5(3.6 g)经细分(石油醚-乙酸乙酯,10∶1→5∶1→1∶1)后得到化合物3(8.3 mg)。Fr.6(6.9 g)经细分(石油醚-乙酸乙酯,10∶1)和纯化后得到化合物8(8.6 mg)和9(6.4 mg)。Fr.7(5.2 g)经细分(石油醚-乙酸乙酯,5∶1)和纯化后得到化合物2(14.3 mg)。Fr.8(7.2 g)经细分(石油醚-丙酮,10∶1)后得到化合物1(10.4 mg)。Fr.9(30.8 g)经细分(石油醚-乙酸乙酯,3∶1)后得到化合物10(6.4 mg)和11(4.1 mg);经细分(石油醚-乙酸乙酯,1∶1)和纯化后得到化合物4(10.1 mg)和5(9.6 mg);经细分(石油醚-丙酮,3∶1→1∶1)后得到化合物12(5.7 mg)、13(4.5 mg)和14(4.8 mg);经细分(氯仿-甲醇,3∶1)后得到化合物15(6.7 mg)。
1.2.2 细胞毒性实验
采用CCK-8法测试化合物1~15对人乳腺癌细胞MDA-MB-231、MCF-7及小鼠乳腺癌细胞4T1的增殖抑制作用[10]。将处于对数生长期的3种乳腺癌细胞用含10%胎牛血清的DMEM培养基稀释成密度为1×106个/mL的单细胞混悬液,按照每孔100 μL接种于96孔板中,在37 ℃、5% CO2恒温培养箱中孵育24 h,再将15个化合物依次用DMSO溶解后,加入不含胎牛血清的DMEM培养基稀释成6种不同浓度(3.125、6.25、12.5、25、50、100 μmol/L)的剂量组,以顺铂作为阳性对照药物[11],设置5个复孔,孵育24 h后移弃上层培养液,每孔加入100 μL 0.1% CCK-8进行染色,孵育2 h后在酶标仪OD 450 nm测量各孔的吸光值(A),重复三次,计算IC50。
2 结果
2.1 结构鉴定
化合物1白色针晶(CHCl3);ESI-MS:m/z145.2[M+Na]+。1H NMR(600 MHz,CDCl3)δ:7.82(2H,d,J= 8.7 Hz,H-2,H-6),6.98(2H,d,J= 8.6 Hz,H-3,H-5);13C NMR(150 MHz,CDCl3)δ:130.0(C-1),132.7(C-2,C-6),116.2(C-3,C-5),161.7(C-4),191.4(C-7)。基于以上数据及文献[12]鉴定该化合物为对羟基苯甲醛。
化合物2白色针晶(CHCl3);ESI-MS:m/z123.0[M+H]+。1H NMR(600 MHz,CDCl3)δ:8.14(2H,d,J= 7.0 Hz,H-2,H-6),7.49(2H,t,J= 7.9 Hz,H-3,H-5);13C NMR(150 MHz,CDCl3)δ:129.5(C-1),130.4(C-2,C-6),128.6(C-3,C-5),134.0(C-4),172.5(C-7)。基于以上数据及文献[13]鉴定该化合物为苯甲酸。
化合物3白色粉末状固体;ESI-MS:m/z197.0[M+H]+。1H NMR(600 MHz,CDCl3)δ:7.65(1H,dd,J= 8.3,1.9 Hz,H-6),7.55(1H,d,J= 2.0 Hz,H-2),6.93(1H,d,J= 8.3 Hz,H-5),5.99(1H,s,H-4),4.35(2H,q,J= 7.1 Hz,H-8),3.95(3H,s,H-10),1.38(3H,t,J= 7.1 Hz,H-9);13C NMR(150 MHz,CDCl3)δ:124.3(C-1),111.8(C-2),146.3(C-3),150.0(C-4),114.1(C-5),122.8(C-6),166.6(C-7),60.9(C-8),14.5(C-9),56.3(C-10)。基于以上数据及文献[14]鉴定该化合物为香草酸乙酯。
化合物4无色针晶(CHCl3);ESI-MS:m/z199.0[M+H]+。1H NMR(600 MHz,CDCl3)δ:7.08(2H,s,H-2,H-6),1.37(3H,t,J= 7.1 Hz,H-9);13C NMR(150 MHz,CDCl3)δ:121.6(C-1),109.9(C-2,C-6),146.2(C-3,C-5),139.5(C-4),168.5(C-7),61.5(C-8),14.6(C-9)。基于以上数据及文献[15]鉴定该化合物为没食子酸乙酯。
化合物5淡黄色粉末;ESI-MS:m/z184.7[M+Na]+。1H NMR(600 MHz,CD3OD)δ:6.79(1H,dd,J= 8.5,2.3 Hz,H-6),6.71(1H,d,J= 2.4 Hz,H-8),6.18(1H,d,J= 9.4 Hz,H-3);13C NMR(150 MHz,CD3OD)δ:163.2(C-2),112.3(C-3),146.1(C-4),130.7(C-5),114.5(C-6),163.7(C-7),103.4(C-8),157.3(C-9),113.1(C-10)。基于以上数据及文献[16]鉴定该化合物为7-羟基香豆素。
化合物6淡黄色油状物;ESI-MS:m/z243.2[M+H]+。1H NMR(600 MHz,CDCl3)δ:3.66(3H,s,H-15),2.29(2H,t,J= 7.6 Hz,H-2),1.61(2H,p,J= 7.5 Hz,H-13),1.30~1.23(20H,m,H-3,H-4,H-5,H-6,H-7,H-8,H-9,H-10,H-11,H-12);13C NMR(150 MHz,CDCl3)δ:174.5(C-1),34.3(C-2),25.1(C-3),29.8(C-4,C-5,C-6,C-7,C-8,C-9,C-10,C-11),32.1(C-12),22.8(C-13),14.3(C-14),51.6(C-15)。基于以上数据及文献[17]鉴定该化合物为肉豆蔻酸甲酯。
化合物7淡黄色油状物;ESI-MS:m/z411.2[M+H]+。1H NMR(600 MHz,CDCl3)δ:5.17~5.09(6H,m,H-3,H-7,H-11,H-14,H-18,H-22),2.09(8H,td,J= 9.5,5.0 Hz,H-5,H-9,H-16,H-20),2.08~1.97(12H,m,H-4,H-8,H-12,H-13,H-17,H-21),1.69~1.68(6H,m,H-1,H-25),1.61~1.60(18H,m,H-24,H-26,H-27,H-28,H-29,H-30);13C NMR(150 MHz,CDCl3)δ:25.8(C-1,C-25),131.4(C-2,C-23),124.6(C-3,C-22),26.9(C-4,C-21),39.9(C-5,C-9),135.0(C-6,C-19),124.5(C-7,C-11),26.8(C-8,C-17),135.3(C-10,C-15),28.4(C-12,C-13),124.4(C-14,C-18),39.9(C-16,C-20),17.8(C-24,C-26),16.2(C-27,C-28),16.1(C-29,C-30)。基于以上数据及文献[18]鉴定该化合物为角鲨烯。
化合物8白色粉末状固体;ESI-MS:m/z457.4[M+H]+。1H NMR(600 MHz,CDCl3)δ:5.28(1H,t,J= 3.7 Hz,H-12),1.17~1.12(3H,s,H-27),1.00~0.94(3H,s,H-23),0.77(3H,s,H-24);13C NMR(150 MHz,CDCl3)δ:38.5(C-1),27.3(C-2),79.2(C-3),38.9(C-4),55.3(C-5),18.4(C-6),32.7(C-7),39.4(C-8),47.8(C-9),37.2(C-10),23.1(C-11),122.8(C-12),143.7(C-13),41.7(C-14),27.8(C-15),23.7(C-16),46.7(C-17),41.1(C-18),46.0(C-19),30.8(C-20),33.9(C-21),32.6(C-22),28.2(C-23),15.7(C-24),15.5(C-25),17.3(C-26),26.1(C-27),183.4(C-28),33.2(C-29),23.5(C-30)。基于以上数据及文献[19]鉴定该化合物为齐墩果酸。
化合物9白色粉末状固体;ESI-MS:m/z457.4[M+H]+。1H NMR(600 MHz,CD3OD)δ:5.23(1H,t,J= 3.7 Hz,H-12),3.15(1H,dd,J= 11.6,4.6 Hz,H-18),1.04~0.98(3H,s,H-23)0.78(3H,s,H-24);13C NMR(150 MHz,CD3OD)δ:40.8(C-1),27.9(C-2),79.7(C-3),40.4(C-4),56.7(C-5),19.5(C-6),34.3(C-7),40.4(C-8),48.6(C-9,C-17),39.8(C-10),24.1(C-11,C-27),126.9(C-12),139.7(C-13),43.2(C-14),28.8(C-15),25.3(C-16),54.4(C-18),40.0(C-19),38.1(C-20),31.8(C-21),38.1(C-22),29.2(C-23),16.0(C-24),16.4(C-25),17.7(C-26),181.8(C-28),17.8(C-29),21.6(C-30)。基于以上数据及文献[19]鉴定该化合物为熊果酸。
化合物10白色粉末状固体;ESI-MS:m/z331.2[M+Na]+。1H NMR(600 MHz,CDCl3)δ:5.22(1H,d,J= 17.3 Hz,H-15),5.03(1H,d,J= 10.7 Hz,H-15′),1.28~1.22(3H,m,H-16),1.19~1.11(3H,m,H-17),0.86(3H,s,H-20),0.78(6H,s,H-18,H-19);13C NMR(150 MHz,CDCl3)δ:39.8(C-1),18.6(C-2),42.1(C-3),33.4(C-4),56.2(C-5),19.3(C-6),44.6(C-7),24.7(C-8),61.7(C-9),39.4(C-10),20.7(C-11),45.1(C-12),74.9(C-13),146.1(C-14),111.4(C-15),21.6(C-16),27.6(C-17),33.5(C-18),24.4(C-19),15.5(C-20)。基于以上数据及文献[20]鉴定该化合物为香紫苏醇。
化合物11白色粉末状固体;ESI-MS:m/z251.2[M+H]+。1H NMR(600 MHz,CDCl3)δ:2.44~2.36(1H,m,H-11),2.23(1H,dd,J= 16.2,6.5 Hz,H-11′),2.07(1H,dt,J= 11.9,3.4 Hz,H-9),1.97(1H,dd,J= 14.8,6.5 Hz,H-7),1.88(1H,dq,J= 14.3,3.2 Hz,H-6);13C NMR(150 MHz,CDCl3)δ:39.6(C-1),18.2(C-2),42.3(C-3),33.3(C-4),56.8(C-5),20.7(C-6),38.9(C-7),86.6(C-8),59.3(C-9),36.2(C-10),28.9(C-11),177.1(C-12),21.7(C-13),33.3(C-14),21.1(C-15),15.2(C-16)。基于以上数据及文献[21]鉴定该化合物为香紫苏内酯。
化合物12灰白色粉末状固体;ESI-MS:m/z139.2[M+H]+。1H NMR(600 MHz,CD3OD)δ:9.69(1H,s,H-7),6.91(1H,d,J= 8.0 Hz,H-5);13C NMR(150 MHz,CD3OD)δ:131.1(C-1),114.8(C-2),146.1(C-3),153.7(C-4),115.8(C-5),126.4(C-6),193.1(C-7)。基于以上数据及与文献[22]鉴定该化合物为原儿茶醛。
化合物13白色针晶(MeOH);ESI-MS:m/z155.1[M+H]+。1H NMR(600 MHz,CD3OD)δ:7.44(1H,s,H-2),6.79(1H,d,J= 8.3 Hz,H-5);13C NMR(150 MHz,CD3OD)δ:122.9(C-1),117.6(C-2),145.8(C-3),151.2(C-4),115.6(C-5),123.8(C-6),170.1(C-7)。基于以上数据及文献[22]鉴定该化合物为原儿茶酸。
化合物14白色粉末状固体;ESI-MS:m/z411.7[M+H]+。1H NMR(600 MHz,CDCl3)δ:3.64(2H,t,J= 7.7 Hz,H-1),1.27~1.22(52H,brs,26×CH2);13C NMR(150 MHz,CDCl3)δ:63.3(C-1),33.0(C-2),25.9(C-3),29.9~29.5(22×CH2),32.1(C-26),22.8(C-27),14.3(C-28)。基于以上数据及文献[23]鉴定该化合物为二十八烷醇。
化合物15白色针晶(MeOH);ESI-MS:m/z193.1[M+Na]+。1H NMR(600 MHz,CD3OD)δ:7.06(2H,s,H-2,H-6);13C NMR(150 MHz,CD3OD)δ:121.7(C-1),110.2(C-2,6),146.0(C-3,5),139.3(C-4),170.2(C-7)。基于以上数据及文献[15]鉴定该化合物为没食子酸。
化合物1~15结构见图1。
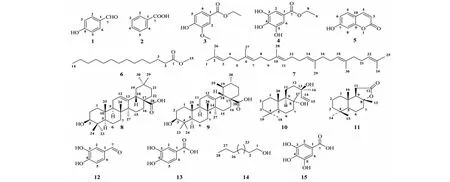
图1 化合物1~15的化学结构
2.2 细胞毒活性
实验结果表明,在100 μmol/L浓度下化合物1~3、5~7、10~15对MDA-MB-231、MCF-7和4T1三种乳腺癌细胞增殖的抑制率均低于50%。化合物4、8和9对上述3种乳腺癌细胞的增殖均有一定的抑制作用,结果见表1。
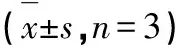
表1 化合物1~15体外抗乳腺癌细胞活性的IC50
3 结论
本课题组前期研究[8]发现尖尾芋醇提物石油醚部位具有良好的抗乳腺癌活性,其机制与抑制MAPKs通路p-ERK/ERK的表达有关,但尖尾芋醇提物石油醚部位抗乳腺癌药效物质基础尚不明确。因此,本研究从尖尾芋根茎石油醚部位中分离得到16个化合物,这些化合物包括酯类(肉豆蔻酸甲酯、香草酸乙酯)、萜类(角鲨烯、齐墩果酸、熊果酸、香紫苏醇、香紫苏内酯)、苯丙素类(对羟基苯甲醛、7-羟基香豆素)、多酚类(没食子酸乙酯、原儿茶醛、原儿茶酸)、芳香酸类(苯甲酸)、脂肪醇类(二十八烷醇)以及酚酸类(没食子酸),其中化合物2~15为海芋属首次分离得到,所有化合物均为尖尾芋首次分离得到。体外抑制乳腺癌细胞增殖实验结果表明,化合物4、8、9对人乳腺癌MDA-MB-231、MCF-7细胞及小鼠乳腺癌4T1细胞增殖均有一定的抑制作用。研究发现[24-27],齐墩果酸、熊果酸及没食子酸乙酯能够抑制多种肿瘤细胞的增殖和扩散,诱导肿瘤细胞凋亡,其抗肿瘤作用可能与其调节PI3K/Akt、MAPK、Wnt/β-catenin等信号通路有关,与本课题组前期研究的尖尾芋石油醚部位抗乳腺癌机制相符合。综上,本研究进一步丰富了尖尾芋石油醚部位化学成分组成,并筛选出其体外抑制乳腺癌细胞增殖的活性成分,为研究尖尾芋石油醚部位抗乳腺癌药效物质基础提供了一定的实验依据。

