基于干细胞与生物3D打印技术的皮肤组织工程研究与应用进展
李 玲, 丁 文, 刘 明
(1)黑龙江省黑河市疾病预防控制中心 检验科, 黑龙江 黑河 164300;2)浙江工业大学 材料科学与工程学院,材料成形与控制工程研究所, 杭州 310014;3)浙江省肿瘤医院 中国科学院杭州医学研究所, 细胞治疗技术研究与工程实验室, 杭州 310022)
皮肤作为具有大表面人体最外层的器官,大约占人体重的15%,其平铺开的面积约1.7 m2[1,2]。近年来,与皮肤相关的炎症、衰老和糖尿病伤口愈合等问题是临床和研究中的难题[3]。迄今为止,最常用的治疗皮肤缺损的方法是自体皮肤移植。然而,供体部位的缺乏、继发性损伤和感染风险限制了自体皮肤移植的应用。与传统的治疗方法相比,组织工程皮肤(tissue engineering skin , TES)为治疗皮肤缺陷提供了一种新的方法[4,5]。Naik团队首次发现当人体有病原菌入侵时,诱发的炎症会使上皮干细胞中负责损伤和修复的AIM2基因,从而当病原体再次入侵相同部位时,带有“记忆”的上皮干细胞会快速分泌损伤与修复蛋白,召集大量的免疫细胞和上皮干细胞快速消灭病原菌。他们证明了皮肤中上皮干细胞会对炎症反应产生记忆,这种皮肤“记忆”能力将可能改变我们对多种自身免疫疾病和癌症的认识[6]。Yu团队报道基于可穿戴交联聚合物(wearable crosslinked polymer layer,XPL)凝胶系统人工皮肤可以模拟正常的皮肤性质,XPL可以局部应用,在皮肤界面快速固化,XPL的发现可能为皮肤功能屏障受损、药物传送和损伤修复方面提供先进的解决方案[7]。目前的研究在皮肤炎症、衰老和皮肤修复上取得一定的进步,但在创建功能性齐全的皮肤上仍然存在局限。
皮肤是人体内非常复杂器官,主要由3层结构组成包括表皮、真皮和皮下组织,表皮主要由角质形成细胞和黑素细胞组成,物理屏障、免疫防御和感受器的作用;真皮主要由成纤维细胞、胶原纤维、血管、神经、毛囊和汗腺组成,为皮肤提供氧气和营养物质,调节体温促进伤口愈合,支持和保护的作用;皮下组织作为皮肤的最内层,主要由成纤维细胞、脂肪细胞和巨噬细胞组成,避免寒冷和剧烈的创伤,储存能量促进伤口的修复[8,9]。为了构建用于药物筛选、化妆品测试和可以移植的仿生皮肤模型,皮肤结构的复杂性需要更加可控的成型技术来实现。如:3D生物打印。
生物打印工程技术提供了一个完全自动化和先进的平台,可以利用计算机辅助设计通过一层一层的打印工艺,实现活细胞、生物材料和生长因子的沉积,具有高度的灵活性和可重复性[10,11]。3D生物打印技术有助于高度自动化地构建复杂的组织构建物,可以同时沉积多种细胞类型和生物材料,以增强与天然皮肤结构的相似性。目前主要的生物打印包括微滴喷墨式生物打印[12]、挤出式生物打印[13]、激光式生物打印[14]立体光刻式生物打印技术[15],并且对于皮肤的打印也已经实现了便携式生物打印机的构建[9]。三维生物打印在TES制备方面具有一些优势,包括:(1)根据创面的形状和深度,计算机扫描成像技术可以快速打印出与伤口匹配的植皮,具有及时性、高通量重复性高的特点。(2)有多种生物墨水的可用性。它们可以灵活、准确地沉积不同的生物制剂(包括活细胞、核酸、生长因子、预明胶化溶液等),构建组织结构,其形态和生理学表现出相似的正常皮肤。(3)利用逐层沉积的原理,可以在伤口表面原位打印皮肤组织。(4)具有互联的孔隙和一定的表面积,支持细胞附着、生长、细胞间通信以及气体和营养物质的交换,在过去的十年中,3D生物打印技术已被用于各个领域的生物组织的制造,如血管系统、心、骨骼、软骨、皮肤和肝[1,4,14]。
细胞来源是生物打印的重要组成成分。大规模的工业化细胞培养是生物打印应用的必要条件,使用干细胞可能提供潜在的解决方案来克服细胞数量的局限性[7,10]。自2006年日本科学家山中伸弥团队将4个转录因子的组合转入到皮肤纤维母细胞中得诱导多能干细胞(induced pluripotent stem cells, iPSCs)后,多能干细胞的增殖和分化方向得到广泛重视[16]。近年来,有多研究致力于iPSCs分化来的角质细胞和成纤维细胞以及其他皮肤相关细胞,减少了移植后产生的排斥反应[17]。另外,脂肪来源的间充质干细胞(mesenchymal stromal cells, MSCs)和毛囊干细胞(hair follicle stem cells,HFSC)分化来的汗腺和毛囊附属器等也备受关注,而3D生物打印的MSCs被证实具有更好的细胞增殖和表达生物因子的能力,种子细胞的来源解决了皮肤组织工程对于细胞数量的需求[7,18]。干细胞技术方面的突破使我们能够建立更可靠、更复杂的生理或病理体外皮肤模型。
Yu等人以3D生物打印技术为基础,详细的介绍了体外输送各种类型的干细胞及其抗生素促进伤口愈合等进展[19]。Ishack等人介绍了3D生物打印的基本原理,3D生物打印皮肤的应用[13]。目前,国内外更多的研究集中在干细胞、3D生物打印和皮肤结构构建上,但从皮肤的应用需求到下游应用的综述却少。本文综述介绍4种3D生物打印技术,并与来源于干细胞的皮肤细胞最新进展进行详细的介绍,重点讨论了不同的3D生物打印工艺构建皮肤的特点和皮肤种子细胞的来源,并剖析了皮肤构建物的下游应用需求,为本领域在体外生理或病理模型构建、药物筛选、再生医学和临床等研究提供参考。
1 皮肤的应用需求
皮肤是人体内非常复杂的组织,通过执行关键功能来确保生存,如保护、体温调节、排泄、吸收、代谢功能、感觉、蒸发管理和美学。开展皮肤相关问题的研究及应用对于高仿生皮肤构建有着广泛的需求。
1.1 化妆品及药物筛选需求:化妆品、疫苗、膏药、皮肤病药物
根据ISO 10993《医疗器械生物相容性标准》,皮肤刺激是生物风险评估中必须考虑的3个毒理学实验之一[20]。Akagi等利用逐层细胞包被技术构建人表皮模型进行刺激物验证,并从化学物品中分离出了有效的药物或化妆品成分。皮肤表皮层的建立已经取得了大的进展,但是化妆品及药物筛选的需求对于仿生的皮肤构建物要求越来越严格[21]。随着科技的不断进步,细胞和分子生物学方法被引入到现代毒理学研究,新的检测方法亦随之出现。如体外培养的永生化细胞、组织器官再生、计算机预测毒性等新的体外检测方法替代传统的动物实验检测方法。近年来,欧洲联盟完全禁止对化妆品进行动物试验,这就需要开发试验应用的替代模型[22]。不同的跨国公司和3D打印公司之间正在不断的增加研发合作,凸显了对于3D生物打印应用于工程化皮肤构造方面的重视。
1.2 皮肤移植:糖尿病、烧伤、皮肤病(大疱性表皮松懈症、牛皮藓)
因静脉淤滞、糖尿病或其他疾病引起的皮肤溃疡等疾病正在日益增加,因此人们对于皮肤修复的需求越来越多。Jackw团队通过基因编辑(CRISPR-associated protein 9,CRISPR/Cas9)介导的同源定向修复技术(homology directed repair,HDR)来靶向来源于大疱性表皮松懈症患者成纤维细胞诱导的iPSC,矫正了突变基因COL7A1,从基因修复后的iPSCs分化为成纤维细胞和角质形成细胞,且在皮肤创伤的治疗过程中不会产生免疫排斥。这项重要研究将会给皮肤溃烂的大疱性表皮松懈症患者带去福音[23,24]。基因编辑的出现改变了一些遗传性疾病带来的困扰,但仍存在基因突变风险评估。随着科技的进步,在患者来源细胞和动物模型中基因编辑疗法为其在遗传性皮肤病的临床应用提供了进一步的可能[25]。3D打印技术不仅可以形成仿生的皮肤构建物,并且可以摆脱基因突变和新伤口炎症等困扰,为皮肤移植和临床应用打下良好的基础。
1.3 仿生层次的需求:色素、毛囊、神经、汗腺
皮肤构建包含多种功能结构,除了表皮和真皮外,皮肤还有其他附属结构包括毛囊、神经汗腺等,它们对于皮肤功能发挥非常重要的作用,通过执行关键功能来确保生存,如保护、体温调节、排泄、吸收、代谢、感觉、蒸发管理和美学等[22,26]。目前,传统的皮肤构建物已经为烧伤或慢性创伤患者提供了有益替代物,但现有的生物工程构建物在色素沉着、毛囊和汗腺再生等功能结构重建方面仍远远不够理想[7,9,27]。生物打印方法有助于高度自动化地构建复杂的皮肤构建物,其在生物学、材料学和计算机设计领域的潜力将有望使全功能皮肤结构得以实现。
2 3D生物打印技术
生物打印技术是从3D打印技术发展而来的,目前主要包括喷墨式生物打印、挤出式生物打印、激光辅助式生物打印和立体光刻式生物打印。3D生物打印技术有潜力直接创建梯度宏观结构,以更好地模拟自然细胞外基质,从而同时增加多种类型细胞的附着和增殖,为高仿生皮肤的制备提供了可能。
2.1 喷墨式生物打印皮肤
由于喷墨式生物打印技术简单、灵活、多功能性并能良好控制沉积模式,使其在皮肤组织构建中得到广泛的应用。Ng等利用喷墨式生物打印来源不同供体的角质形成细胞、黑色素细胞和纤维母细胞,所形成的表皮区域厚度从51.6±3.4 μm(第1周)增加到143.5±6.7 μm(4周),并且在气液相界面(air-liquid interface , ALI)培养2周,表皮区域的细胞形态显示了角质细胞分化的早期迹象,这对黑素体吸收至关重要。通过上述打印方式,他们成功的构建了色素沉着的皮肤构建物,且表现出与人类皮肤类似的色素沉着,并与传统手工铸造的含有色素皮肤构建体相比发现,存在明显的表皮层和一层连续的基底膜蛋白[27]。3D生物打印技术的发展促进了三维体外皮肤着色技术的发展。Kim团队开发了一种混合3D细胞打印系统,可以同时使用喷墨式生物打印和挤出式生物打印构建含有真皮的皮肤模型。首先,通过使用挤出式打印系统将聚己内酯材料构建成一个网状基层,然后利用喷墨式打印系统均匀的分配含有角质形成细胞的胶原材料。所构建的组织模型在ALI条件下培养14天,通过HE染色切片发现成纤维细胞被拉伸,并且与在天然真皮细胞拉伸情况相似,这一现象也表明角化细胞在第14天分化。层状表皮厚度(97±3 μm)也保持在75 ~ 150 μm的正常范围内。混合系统构建的皮肤模型显示了良好的生物学特性,如稳定存在的纤维生长因子以及成熟的表皮层[28,29]。同时使用基于喷墨式和挤出式系统或者其他分配模块,为构建仿生的生理或病理模型奠定了良好基础。
2.2 挤出式生物打印皮肤
挤出式生物打印是生物打印方法中较简单的一种。价格低廉、打印速度快扩充性强,对细胞的损伤较低,是进行皮肤构建较好的打印方式[30]。Huang团队使用明胶和海藻酸钠对真皮组织进行了3D生物打印,他们创建了附有小鼠上皮祖细胞的真皮,并且发现负载细胞的真皮结构至少可以保持3周。在培养7天后,发现细胞良好的附着在生物材料上,表现出明显的活力。在体外,将小鼠足底真皮和表皮生长因子同步加入细胞外基质模拟物中,为表皮祖细胞创造了良好的微环境,维持细胞活力,促进细胞扩散和基质形成,实现了特异性细胞分化。在体内,直接将生物打印细胞外基质移植到小鼠烧伤的爪子中,恢复了汗腺的功能[31]。Albanna带领团队开发了可移动的皮肤生物打印系统,促进了自体或异体成纤维细胞和角质形成细胞直接进入损伤区域,形成表皮和真皮的分层结构。在6周的时间内对小鼠伤口面积进行评估,发现与未接受皮肤打印的小鼠相比,伤口愈合速度更快。将负载自体成纤维细胞和角质形成细胞的水凝胶载体孵育在猪的切除性伤口,促进了伤口快速闭合、增加收缩并加速了再上皮化大规模的发展[32]。应用挤出式3D打印技术构造的皮肤构建物在形态和功能上与人体皮肤组织相似,为再生医学移植探索了新的方法[32]。
2.3 激光辅助式生物打印皮肤
激光辅助生物打印能够将活细胞按照预设计的模式排列,实现功能性皮肤构建物的体外制造[33]。Koch等利用激光辅助生物打印实现成纤维细胞、角质形成细胞和人源间充质干细胞(human mesenchymal stem cell,hMSC )的有序排列,实现真皮组织打印。打印后几天皮肤细胞和间充质干细胞的存活率分别为98%±1%和90%±10%,保持其增殖能力。此外,皮肤细胞和hMSC显示出细胞凋亡或DNA断裂的增加,且细胞表型不变[34,35]。此发现可能会制造出更仿生的皮肤替代物改善糖尿病或烧伤病人的损伤。Koch等还利用激光辅助生物打印将成纤维细胞、角质形成细胞和胶原蛋白材料,构造打印形成仿真的表皮皮肤模型,细胞之间处于分层状态且不易发生混合。打印后10 d,细胞定位和增殖分析发现在成纤维细胞与角质形成细胞之间形成了层黏连蛋白[36]。可见,激光式生物打印技术为产生具有完整血管网络的组织提供了巨大的潜力,激光辅助生物打印技术甚至可能实现打印完整器官的长期目标。
2.4 立体光刻式生物打印皮肤
立体光刻式生物打印进行皮肤组织打印的研究少,更多应用于打印微针阵列,用于胰岛素经皮给药[37]。Economidou等利用立体光刻打印光聚合树脂连续聚合形成微针,通过喷墨打印在针的表面形成了薄层胰岛素和糖醇或二糖载体。打印工艺的优化使得3D打印微针的透皮能力优于金属阵列,最小的作用力变化范围在2~5 N。并且与皮下注射相比,胰岛素包被3D打印阵列显示出显著的稳态降糖效果,促进了血中胰岛素浓度的迅速增加,血浆中葡萄糖水平迅速下降。胰岛素作用快,低血糖控制良好,在60 min内血糖水平降低,且稳定血糖超过4 h[38]。立体光刻打印技术精准打印的结构微针被视为皮下注射针优良的微创替代物,它可以穿过皮肤角质层但不会对表皮下区的神经末梢造成干扰,因此不会引起疼痛。Yadav等利用微立体光刻打印技术,构建了平均长度、宽度和厚度分别为13.05±0.11 mm、13.07±0.15 mm和3.50±0.05 mm微针阵列,实现了利福平的透皮递送,在移除微针阵列后穿透痕迹在45内完全消失[39]。微立体光刻生物医学应用是一个有吸引力的制造技术,尤其是对微米尺寸制造,是一种潜在的治疗皮肤癌的方法。4种生物3D打印方式在再生组织医学的研究具有前景(见Fig.1)。
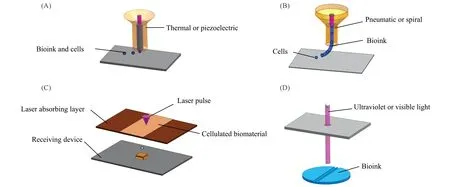
Fig.1 Summary of four 3D bioprinting approaches. (A) Principle of inkjet bioprinting. (B) Principle of extrusion-based bioprinting. (C) Principle of laser-assisted bioprinting. (D) Principle of stereolithography bioprinting
2.5 便携式3D打印机
随着3D打印技术的发展,手持式皮肤打印机的出现使伤口部位的皮肤组织原位修复成为可能。Hakimi等人的杰出工作代表了便携式3D生物打印机的发展(重量< 0.8 kg),在体外,他们发现包埋在纤维蛋白基质中的人真皮成纤维细胞培养10天后的存活率为90%。在体内,使用微流控打印机对皮肤组织进行了原位生物打印。研究表明,在直径8 mm的小鼠切除伤口上原位形成了生物聚合物纤维阵列,同时沉积在弯曲和柔顺的伤口表面上。沉积的条纹片状或条纹阵列牢固地附着在伤口上,并周期性地跟随呼吸周期或人工组织变形。皮肤的原位形成是使用生物墨水中的特异性皮肤细胞直接治疗的结果[5,40]。这种便携式3D打印机在目前的医疗保健市场是革命性的创新,因为病人不必等待实验室培养的细胞再进行皮肤移植。另外,该技术也用于烧伤或外伤等紧急情况,并在救护车上进行实时治疗。一般来说,伤口敷料根据其在伤口愈合中的作用分为被动敷料和主动敷料。理想的创伤敷料不仅要保护创面不受微生物感染,允许气体交换,吸收多余的渗出物,还要保持湿润的环境,促进上皮的再生。近年来,电纺纳米纤维聚合物已显示出作为伤口愈合敷料的巨大潜力[5,9]。Dong等首次提出一种抗菌且生物相容的诱导型聚集排放物(aggregation-induced emission,AIE)的纳米纤维敷料,通过人脐带静脉内皮细胞(human umbilical vein endothelial cells,HUVEC)和小鼠胚胎成纤维细胞在纳米纤维敷料上粘附牢固并且复制能力增强。同时他们利用手持式静电纺丝装置完成了AIE纳米纤维敷料的原位沉积,电纺后在对其基本性能如表面形貌、结构、热稳定性和疏水性进行表征发现AIE纳米纤维敷料对沙门氏菌具有高效的抗菌活性,在皮肤伤口模型的体内研究中,沉积的AIE纳米纤维敷料能够消除多药耐药细菌感染并促进伤口愈合[41]。这种个性化纳米纤维敷料经济、耐用可以无痛去除,还能防止细菌渗透。电纺个性化敷料是一个理想的和安全的解决方案,满足伤口治疗的临床需要。
3 皮肤种子细胞的来源
为了构建仿生的皮肤模型,细胞的选择是非常重要的环节,皮肤干细胞是三维皮肤模型和皮肤再生的首选细胞来源,其以自我更新和多向分化能力,易于收集和免疫原性弱的特点,在皮肤重建中得到了广泛应用。
3.1 间充质干细胞
间充质干细胞如骨髓来源的MSCs(bone marrow-derived mesenchymal stem cells, BM-MSCs)和脂肪来源的干细胞(adipose-derived mesenchymal stem cells, Ad-MSCs)已被广泛研究用于烧伤的创面修复和瘢痕缓解。多项研究表明,MSCs通过分泌独特的细胞因子和生长因子促进血管生成和加速伤口愈合,通过抑制肌成纤维细胞活动和减少胶原沉积,进而减少增生性瘢痕[42,43]。Bian团队利用高糖诱导创建了人类真皮衰老模型,并发现来源于子宫蜕膜的间充质干细胞(decidua-derived mesenchymal stem cells, dMSC)形成的小细胞囊泡(small extracellular vesicles,sEVs)不仅能显著促进人类真皮成纤维的增殖、迁移和分化,还能改善其衰老状态。此外,体内发现dMSC-sEVs局部应用加速胶原沉积,促进糖尿病小鼠创面愈合[44]。同年,Yao等利用挤出式生物打印创建了汗腺(sweat gland,SG)样基质,介导间充质干细胞转化为功能性的汗腺,并促进了小鼠SG的恢复[45]。Ge团队从miR-132基因过表达的脂肪干细胞(miR-132-overexpressing adipose stem cells,miR-132-exo)中获取工程外泌体,在体外,证实了其对HUVECs的增值和迁移的促进作用,在体内,基于核因子KB蛋白信号通路介导的miR-132-exo可以有效减轻炎症反应,显著提高皮瓣存活率,促进糖尿病创伤的愈合。可见,间充质干细胞已经成为一种有潜力的治疗皮肤损伤的的来源种子[46]。间充质干细胞经三维打印基质包封后,可提供一个仿生的微环境,促使细胞分化为组织所需的细胞,使其具备再生医学的重要应用价值。
3.2 毛囊干细胞
新毛囊是由位于毛囊突起区的毛囊干细胞及其继发胚芽中的子代驱动再生的,组织依靠干细胞来维持自身平衡和修复伤口[47]。Gur-Cohen等发现在适当的刺激下静息态的毛囊干细胞可以被激活,驱动生长期开始,并开始一个新的毛发周期。在皮肤中,淋巴毛细血管作为关键的干细胞生态成分可以在干细胞周围形成密集网络[48]。并有研究表明Wnt信号通路对毛囊干细胞的维持、激活和分化具有重要作用,其失调将导致毛囊干细胞失去干性或不能被正常激活。Xu等通过在裸鼠伤口原位生物打印表皮干细胞(epidermal stem cells,Epi-SCs)和皮肤多能干细胞(skin-derived precursors,SKPs)促进了毛囊的再生过程,4周,成功观察到表皮、真皮、血管和皮脂腺的形成。此外,研究发现打印后的表皮干细胞和皮肤多能干细胞依然分别表达高水平的CD49f基因和BMP6基因,证实了原位打印细胞依旧保持高的细胞活力和增殖能力[49]。Abaci团队通过使用3D打印再现毛囊微环境,演示了在人类皮肤构建物中生成人类毛囊的仿生方法。另外,Lef-1基因在真皮乳头细胞(dermal papilla cells,DPCs)中的过表达显著提高了人类皮肤构建物中毛囊分化的效率。此外,在移植前对有毛的皮肤构建物进行血管化,使免疫缺陷小鼠的毛发有效生长[50]。从培养的人类细胞中再生整个毛囊的能力将对不同类型的脱发和慢性伤口的医疗管理产生革命性的影响,这迎合了现阶段皮肤损伤修复领域迫切的医疗需求。
3.3 多能干细胞(iPSCs)
iPSCs的研究是再生医学的重大突破,特异性iPSC的建立为在培养系统中模拟生理和病理模型创造了机会,并有可能迅速促进药物的发现。iPSCs是一类具有自我更新和分化功能的细胞,在皮肤细胞的分化中得到广泛的应用[51]。Abaci团队利用iPSC来源的内皮细胞在3D打印技术下构建了灌注的血管网络,并证实带血管化的人体皮肤移植物可以形成强健的表皮和建立内皮屏障,从而允许药物的局部和全身递送的再现[52]。同样,iPSC不仅可以分化为内皮细胞,还可以分化出皮肤附属器其他细胞包括黑色素细胞[53]、神经细胞和施万细胞[54]。为了建立一个受神经支配的组织工程皮肤模型,Muller等利用iPSCs分化成感觉神经元和施万细胞构建了工程皮肤组织,施万细胞是神经元功能和轴突迁移的主要细胞,当受到诱导神经肽刺激时,来自iPSCs的神经元释放P物质和降钙素基因相关的肽。这种独特的人体神经细胞模型对于皮肤神经炎症的研究非常有用[54]。同时,脐带血单个核细胞(cord blood mononuclear cells,CBMCs)已成为再生医学的潜在细胞来源。Kim等利用CBMCs-iPSCs分化而成的角化形成细胞和成纤维细胞发育成表皮层和真皮层。将表皮层叠加于真皮层上,形成复杂的三维皮肤类器官,该类器官移植入皮肤受损的小鼠模型中,改善了皮肤损伤[55]。iPSCs是很有吸引力的候选细胞,因为它们除了在伦理上被接受外,还可以分化成任何所需要的细胞。在重编程过程中,它们是根据患者的基因定制的,干细胞技术的发展可能有助于为皮肤打印提供合适的细胞源替代品,根据种子细胞的来源及其病理性作用见Table 1。
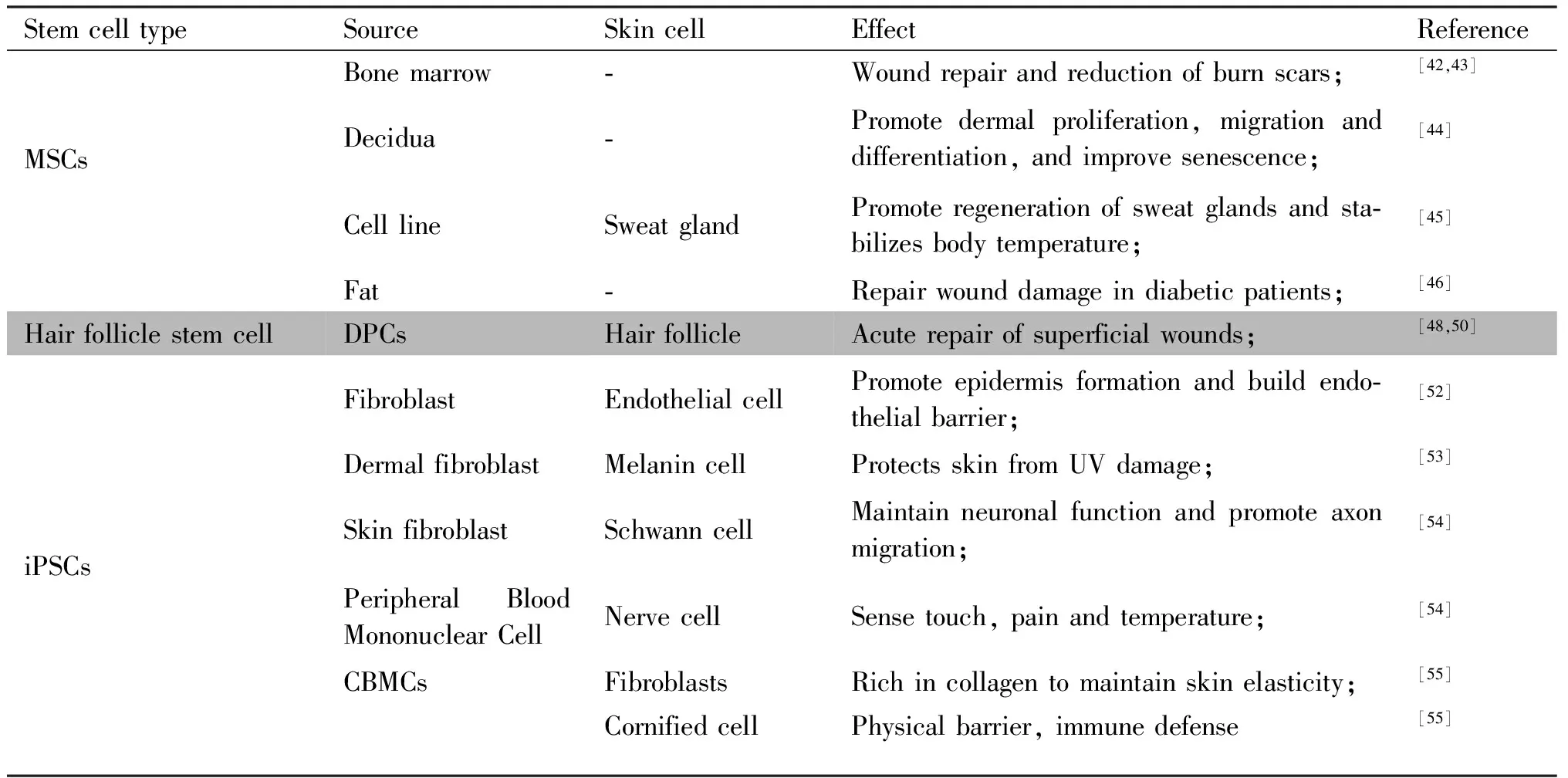
Table 1 Stem cell types and differentiated skin cell types and roles
4 3D生物打印与相关的下游应用
生物3D打印能够很大程度重建天然皮肤的宏观结构和微观特征,保障了高仿生皮肤制备的可能性,为化妆品及药物应用、皮肤移植和仿生层次等下游应用提供了条件。
4.1 化妆品及药物应用
Episkin®是法国欧莱雅旗下子公司Episkin体外重建的表皮模型,是用人胶原I型蛋白 和胶原III 型蛋白做底部基质支架,然后在其上涂一层胶原IV型蛋白,干燥后形成IV胶原的薄膜,将人正常角质细胞接种到覆有IV型胶原的支架上,经过13的气液相培养形成一种类似人表皮的具有分层结构的体外重建表皮模型[56]。EpiSkin®模型不仅可以作为表皮替代物,还在化妆品领域内可用于透皮吸收分析、皮肤腐蚀性验证、皮肤刺激性分析、光毒性分析UV暴露及保护分析[56,57]。SkinEthic®模型同样可进行形态学的分析,培养基中细胞因子,炎症因子等水平检测及基因方面的分析,相较于 Episkin®模型其优势在于使用化学限定培养基培养,与血清培养基相比,培养基中各组成成分及浓度都是确定的,有利于表达通路中某些特定上调或下调的因子。作为表皮替代物,在化妆品领域内可用于透皮吸收分析、皮肤刺激性分析、皮肤致敏性分析、光毒性分析、UV暴露及保护分析美白/美黑作用分析[57,58]。此外,Strat-M®模型也是一种模拟人体皮肤多层结构的合成膜替代品,在体外渗透中,其优异的多孔结构和疏水性再现了皮肤的扩散屏障机制,在不含渗透增强剂的制剂中,间苯二酚的稳态通量对于水溶液为42±5 μg/cm2h,水凝胶为42±6 μg/cm2h,以及水包油乳液为40±6 μg/cm2h,这更接近于离体皮肤(5±3、9±2、13±6 μg/cm2h)的渗透指标。Strat-M®模型作为一种可靠的人类皮肤替代品在化妆品研发过程用作快速筛选潜在亲水活性分子的高效益工具[59]。
4.2 皮肤移植应用
含有异体细胞的多层皮肤替代物已被用于治疗非愈合性皮肤溃疡。Xie等利用3D生物打印制作了植入的多层血管化皮肤移植物。该移植物使用的生物墨水含有人包皮纤维细胞、脐带血人内皮细胞和人类胎盘周细胞,并将这些细胞悬浮在鼠尾I型胶原上来形成一层真皮。第二层生物墨水含有人类包皮角质细胞来形成表皮。当这些3D打印的移植物被移植到免疫缺陷小鼠的背侧时,人的内皮细胞与小鼠创面上的微血管相融合,并促进了表皮网的形成,促进了伤口的修复和愈合[60,61]。Dai等利用人成纤维细胞、内皮祖细胞和明胶建立了皮肤真皮层结构,利用聚氨酯和角质形成细胞作为生物墨水,形成皮肤表皮结构。当植入体内时,双层皮肤构建物在裸鼠模型中,28天后达到90%的伤口愈合率,并且有76%的表皮层出现上皮化[62]。在使用基质蛋白或异种来源的成分生产出的皮肤替代品中,较高的过敏反应免疫排斥风险一直是皮肤移植领域中的难点。Baltazar 团队利用生物打印的皮肤替代品成功实现了人内皮细胞、成纤维细胞、周细胞和角质形成细胞的无异源分离、扩增和冷冻保存。含有人胶原蛋白质和纤连蛋白质的无异源生物墨水经过分层在接种到人角质形成细胞以形成表皮层。这一双层皮肤移植物的制造,为皮肤组织工程的无异种移植提供了可行性[63]。在皮肤移植领域,皮肤的软组织和分层结构使其较其它生物材料的沉积更为容易,3D打印技术能够为患者提供更加定制化和生物相容性的移植皮肤。通过构建与患者本身相匹配的组织,移植的成功率和效果得以显著提升。这对于烧伤患者、先天性皮肤病患者以及其他需要皮肤移植的患者来说是一项重大的医学进步。
4.3 皮肤附属器的应用
3D生物打印含有色素、毛囊、神经和汗腺的皮肤模型,为药物开发、化妆品测试、生理或病理模型和皮肤移植开创新的策略。色素沉着皮肤模型可以通过3D打印黑素细胞来实现。Min等利用3D打印技术成功构建了含有色素沉着的皮肤模型。利用包括成纤维细胞的胶原水凝胶构建真皮层,将黑素细胞和角质形成细胞打印到真皮层的顶端进行培养诱导色素沉着,在表皮层和真皮连接处观察到雀斑样的色素形成[64]。利用3D打印技术结合干细胞培养,实现人工皮肤更加真实的外观。生发研究员、头发修复外科医生以及制药和化妆品行业对3D技术的应用将对含有毛囊的人体皮肤组织维护和再生产生重大影响[49];Motter Catarino团队在含有成纤维细胞的预凝胶真皮层中印刷DPCs和HUVECs诱导的球状体,并结合角质形成细胞和黑素细胞的迁移条件,成功在成熟组织中发育毛囊样结构,其形态和组成与天然皮肤组织基本一致,作为毛发的移植模型用来测试化妆品的安全性,这对再生医学的研究无疑会产生巨大的推动性[65]。针对含有神经细胞特定疾病皮肤模型,并分析这些模型在瞬时受体电位阳离子通道A1激动剂刺激下,神经肽释放后感觉神经的潜在影响。这种模型特别适合于银屑病的建模,以探明由皮肤神经支配调节的疾病发生机制,且这种免疫功能皮肤模型具有很强的个性化药物治疗潜力[54];挤出式生物打印技术已被应用在构建来自iPSCs的皮质神经元和神经胶质前体产生的神经构建体,经过进一步分化,表达了神经元和胶质细胞标志物,这为 3D生物打印构建更为复杂的人类神经系统奠定了坚实基础[66]。此外,胚胎干细胞(embryonic stem cells,ESCs)是SG再生的种子细胞,鉴于细胞外基质中的真皮成分和生长因子对于上皮胚胎干细胞命运发挥着重要作用,将ESCs和表皮生长因子同时加入到明胶和海藻酸钠的混合物中制成生物墨水,打印并构建体外生态模型培养14 h后成功观察到SG细胞,依靠生物材料支架为细胞分化提供结构空间和附着位点,能够准确诱导细胞定向分化以实现SG细胞的增殖[45,67]。这对于基于干细胞的3D打印在临床应用和治疗中是有价值的。
5 问题与展望
3D生物打印具有高分辨率、操作灵活、可重复打印高通量输出等优点。然而,所有的技术,包括3D生物打印,都受到一定的限制和挑战。首先,3D皮肤模型代表了一种全层结构,缺乏免疫细胞、血管分布、神经和汗腺。尽管3D生物打印皮肤有部分临床成功的,但患者和临床医生越来越多的要求解决现有的局限性,如改善表面感觉和再生[1]。在3D打印皮肤诱导的新组织形成过程中,神经再生依赖于新形成的血管。由于缺乏血液供应,神经再生几乎被完全抑制[1,61]。其次,在生物墨水中仍存在一些关键的技术问题需要解决:(1)人体皮肤具有独特的物理力学特性,这对于与皮肤组织特征相对应的生物材料要求很高。(2)所选的打印材料必须与3D打印材料相兼容,由于这些材料在打印后的收缩或强度下降,它们不能满足3D生物打印的使用要求。(3)三维生物打印水凝胶的机械强度不足,压缩后的结构稳定性保持困难。因此,确定一种优越的凝胶方法,在不影响细胞活力的情况下快速稳定的预凝胶溶液是很重要的[68]。另外,3D生物打印需要在打印阶段进行优化,[8]。最后,种子细胞也是三维生物打印技术中需要考虑的一个重要方面。干细胞作为组织工程种子细胞的重要来源,已经引起了广泛的关注。近年的研究表明,干细胞可以在促进皮肤附属物再生、伤口愈合和组织重建方面发挥重要作用。干细胞在TES领域具有巨大的潜力,但伦理问题、成本和技术要求阻碍了干细胞的充分利用[68,69]。
三维生物打印技术在组织修复和再生领域的应用仍是可行的。施旺细胞作为皮肤感觉神经再生的关键细胞成分,在体外可以添加到3D打印支架中,是3D打印皮肤感觉神经再生的良好方法。在未来,可以考虑在TGS中加入施旺细胞,以促进神经纤维的定向生长,增殖和聚集形成类似于“神经导管”的管状结构,促进神经再生[1]。另外,3D生物打印的研究现状表明,一种理想的生物墨水仍有待确定。在未来,生物墨水的材料组成可以进一步优化,如通过引入纳米材料,以提高组织或器官的再生。此外,随着皮肤老化模型,细胞衰老的概念仍在研究中,对于再现与年龄相关的皮肤模型至关重要。这两个领域都相对较新,在获得最优模型之前需要进一步的研究。到目前为止,该领域的研究表明,3D生物打印将允许精确地放置所有各种类型的天然皮肤细胞,并精确地并可重复地制造结构来替代受伤皮肤。然而,复制天然皮肤的结构完整性和功能,以允许伤口修复、温度控制和感觉有待实现。随着相关技术的进步和多学科合作的探索,三维生物打印有望克服这些障碍,在生物工程和皮肤仿生学中发挥重要作用。

