妊娠早期巨细胞病毒感染和产前诊断案例分析
邱佩绵,梁雪雁,温瑛梦,李雪梅,刘彦慧
巨细胞病毒(cytomegalovirus,CMV)是人类感染中最常见的病原体,而妊娠期CMV 原发感染可导致胎儿多发畸形或流产、死胎等[1]。但在临床上长期存在误诊或过度干预等现象,尽管中华医学会制定了相关专家共识[2-3],但在妊娠期筛查时间、筛查次数和间隔时间、IgM 和IgG 是否同时检测、感染时间和感染类型判断、产前诊断时机、超声影像学检查以及妊娠结局评估等方面尚未达成共识。因此,需要积累更多的病例进行深入探讨。本研究对810 例孕妇进行CMV 筛查、诊断和产前诊断,结果提示妊娠期CMV筛查和诊断对出生缺陷防控非常重要,而科学规范的妊娠期CMV 检测是核心所在。
1 对象与方法
1.1 研究对象随机选取2021 年1—12 月在惠州市中心人民医院(我院)妇产科门诊进行常规妊娠期检查的孕妇810 例,年龄17~44 岁,平均(29±4)岁;孕周9~12 周,平均(11±1)周。
1.2 研究方法
1.2.1 孕妇CMV 筛查和诊断所有纳入对象均在妊娠12周内采集外周血,分离血清,采用罗氏cobase 602 电化学发光免疫分析仪同时进行CMV 的IgG 和IgM 定量检测,间隔1~2 周复查1 次。结合2 次抗体定量结果,根据表1 判断孕妇是否感染和感染类型。

表1 根据妊娠早期2 次CMV 的IgG 和IgM 检测结果判断母体感染类型[3]
1.2.2 宫内感染CMV 诊断孕妇确诊为原发感染或再感染后,采用荧光定量聚合酶链反应(fluorescence quantitative polymerase chain reaction,qPCR)检测其外周血和尿液中CMV DNA,结果为阳性者7 周后再进行羊膜腔穿刺,检测羊水细胞中CMV DNA,若羊水DNA 为阳性且大于2.5×105拷贝/mL即可诊断为宫内感染[4-5]。
1.2.3 超声影像学检查孕妇确诊为原发感染或再感染后,用超声检查胎儿是否存在侧脑室增宽、颅内钙化、室管膜下囊肿、小头畸形、肠管回声增强和胎儿生长受限等情况,必要时进一步进行磁共振成像检查[6]。
1.2.4 胎儿组织病理学诊断对于确诊CMV DNA 宫内感染且超声影像学发现明显异常的胎儿引产后,引产胎儿家属签订知情同意书,进行病理诊断。先天性CMV 感染的胎儿一般在胸腺上皮、心肌纤维、肺泡干细胞、中枢神经元细胞及多个器官间质血管内皮细胞见典型细胞病毒感染改变,细胞核内见圆形紫红色巨细胞包涵体,细胞质内见嗜碱性包涵体颗粒,多个脏器间质伴有炎性反应,可见淋巴滤泡浸润等[7]。
2 结果
2.1 妊娠期CMV 感染的筛查和诊断810 例妊娠早期无症状孕妇中确诊CMV 原发感染和复发感染各1 例,原发感染率和复发感染率均约为0.1%;未感染共9 例(1.1%);IgM 持续阳性共16 例(2.0%);既往感染783 例(96.7%),见表2。

表2 810 例妊娠早期无症状孕妇CMV 感染状况
2.2 产前诊断和妊娠结局妊娠期CMV 复发感染1 例,签订知情同意书后,于孕20+6周进行羊膜腔穿刺,确诊为宫内感染,超声显示胎儿腹腔见稍强回声团,范围1.8 cm×1.6 cm,边界欠清(见图1);腹腔见前后径0.4 cm 积液暗区(见图2),孕妇选择终止妊娠。CMV 原发感染1 例,拒绝产前诊断,妊娠中期胎儿超声未见异常,足月顺产,新生儿表型及新生儿筛查等均未见明显异常。
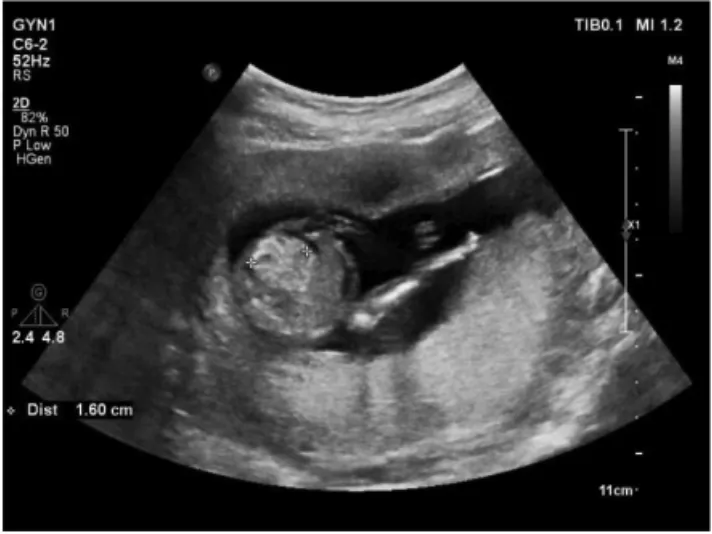
图1 胎儿超声腹腔稍强回声团
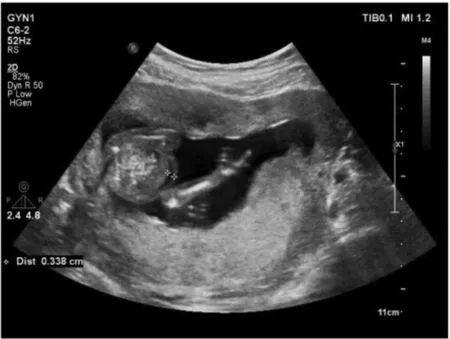
图2 胎儿超声腹腔积液
2.3 引产胎儿病理解剖复发感染的孕妇妊娠12周(2021 年7 月2 日)CMV 抗体定量检测结果为IgM 1.89 COI 和IgG 67.96 U/mL,2021 年7 月16 日第2 次检测结果IgM 1.64 COI 和IgM 143.2 U/mL,尿CMV DNA 为4.85×104拷贝/mL,诊断为妊娠期复发感染。签订知情同意书后,于妊娠20+6周(2021 年9 月2 日)行羊膜腔穿刺,羊水CMV DNA 为2.38×107拷贝/mL,确诊为宫内感染。孕妇要求终止妊娠且同意做胎儿病理解剖。病理可见胎儿肺泡及支气管黏膜上皮、胸腺上皮、心肌纤维、肝细胞及胆管上皮、肾小管上皮及中枢神经元细胞等多个器官间质血管内皮细胞呈典型CMV 感染改变,其中以肺泡上皮细胞表现最为突出,细胞核内见圆形紫红色巨细胞包涵体,细胞质内见嗜碱性包涵体颗粒,多个脏器间质伴有炎性反应,可见淋巴细胞浸润(见图3~5)。病理诊断为播散性先天性CMV 感染。
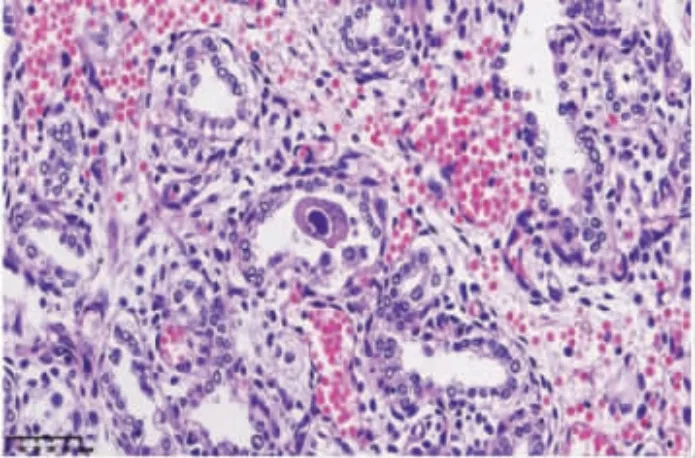
图3 肺泡上皮细胞病毒包涵体(HE 染色×100)
3 讨论
CMV 是引起妊娠早期感染的主要病原体,可导致胎儿先天性多发畸形、流产、死胎及神经性耳聋等非遗传性神经系统异常[8-9]。国外文献显示,CMV 的全球血清流行率高达83%以上[10],妊娠期孕妇原发感染率约为1%~4%,进而将病毒传播给胎儿的风险约为30%~50%,在受感染的胎儿中,在婴儿期出现CMV 感染症状的风险估计为5%~15%[11]。但在国内,临床上通过产前诊断确诊的病例并不多。目前国内对CMV 的感染筛查仍普遍只检测IgM,并以阳性或者阴性报告结果。单纯检测IgM 有局限性,感染CMV 后IgM、IgG 呈动态变化,仅凭单次筛查结果无法确定被检者是否感染或区分其感染类型。同时在检测中,IgM 约有3%~5%的假阳性[12],会导致过度干预,引起孕妇焦虑等不良后果。相关文献明确提出,IgM、IgG 的动态定量分析可排查IgM 假阳性、避免临床困扰和错误干预[12-14]。
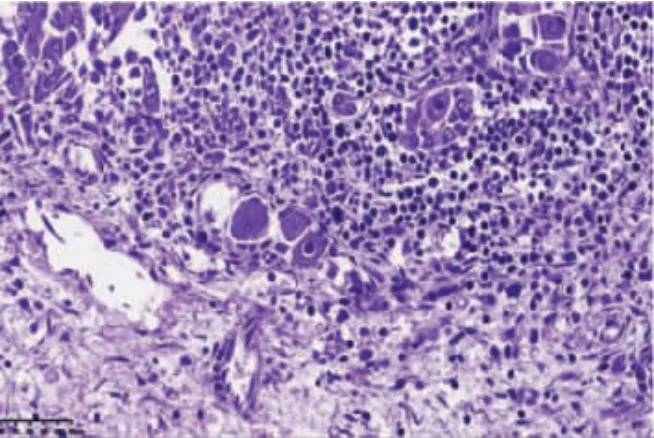
图4 肝细胞上皮细胞病毒包涵体及淋巴细胞浸润(HE 染色×100)
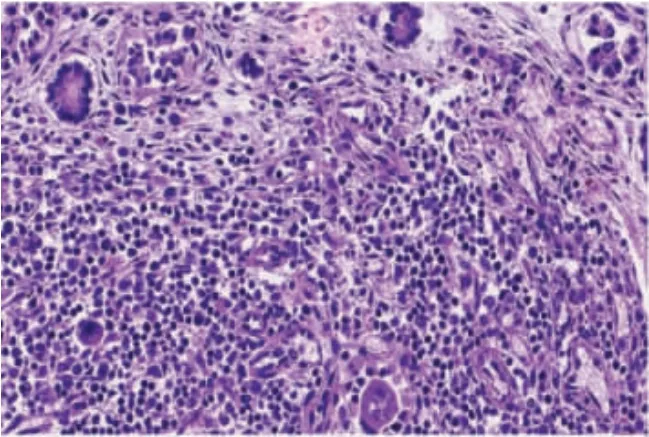
图5 胰腺上皮细胞病毒包涵体(HE 染色×100)
本研究随机选择810 例孕妇,在妊娠12 周前连续2 次检测CMV 的IgG 和IgM,间隔2 周,结果显示,CMV 既往感染率为96.7%,原发感染率和复发感染率均仅为0.1%(各1 例);妊娠早期连续2 次CMV抗体均为阴性者约占1.1%(9 例),即无感染,这类孕妇实际上是妊娠期发生原发感染的高风险人群,建议每间隔2~4 周复查1 次CMV 抗体;此外,值得注意的是孕妇2 次CMV-IgM 检测均显示阳性,而IgG滴度亦无明显变化,该结果提示IgM 为持续阳性,不会导致宫内感染,本次共检出16 例,约占2.0%。提示在妊娠早期CMV 检测时,必须进行2 次连续检测,单次的抗体检测易误诊为原发感染。这是因为在CMV 感染机体的5~7 d 即产生IgM,因此IgM 被认为是早期感染和原发感染的指标,但随后的抗体滴度迅速下降至检测线以下,间隔2 周IgM 检测均为阳性不符合规律,故认为是IgM 持续阳性,不会引起宫内感染。
文献显示,妊娠早期CMV 原发感染和复发感染的孕妇,其新生儿CMV 感染的概率相近[15],因此,均应建议羊膜腔穿刺进行产前诊断。本次诊断为原发感染和复发感染的孕妇各1 例,前者拒绝羊膜腔穿刺,三维超声跟踪检查,未发现胎儿存在明显异常,足月顺产,新生儿表型无明显异常。另1 例复发感染的孕妇于孕20+6周进行了羊膜腔穿刺,羊水和孕妇尿液CMV DNA 检测均为阳性,超声显示腹腔见1.8 cm×1.6 cm 稍强回声团,并可见0.4 cm 积液暗区,孕妇选择终止妊娠,引产胎儿经病理解剖诊断为播散性先天性CMV 感染[6]。
综上所述,CMV 既往感染率高达96.7%,复发感染一般无感冒、咳嗽和发热等症状,比较隐匿。孕妇在妊娠早期CMV 原发感染或复发感染均有可能导致宫内感染,进而导致胎儿多发畸形。但本研究样本量较小,尚需要更多病例进行深入探讨。妊娠早期感染CMV 致畸风险明显高于妊娠中、晚期感染[3]。因此必须坚持在妊娠早期进行CMV 筛查,为确定孕妇基础免疫状态,最理想的是前移到妊娠前进行筛查,而且需要IgG 和IgM 同时检查,并需要连续检查2 次,间隔2 周,然后根据表1 的方法进行综合判断[2]。在对胎儿进行评估时,任何一项检查结果不能作为判读胎儿去留的唯一依据,而要根据筛查、诊断、产前诊断以及超声影像学指标进行综合评估[3]。

